HPV - Condiloma Anal
➧Etiologia do papilomavírus humano (causa do condiloma anal)
➧Transmissão do papilomavírus humano (HPV)
➧Epidemiologia e fatores de risco para o papilomavírus humano (HPV)
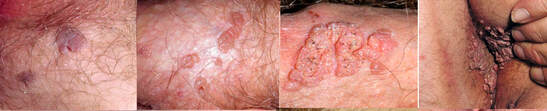
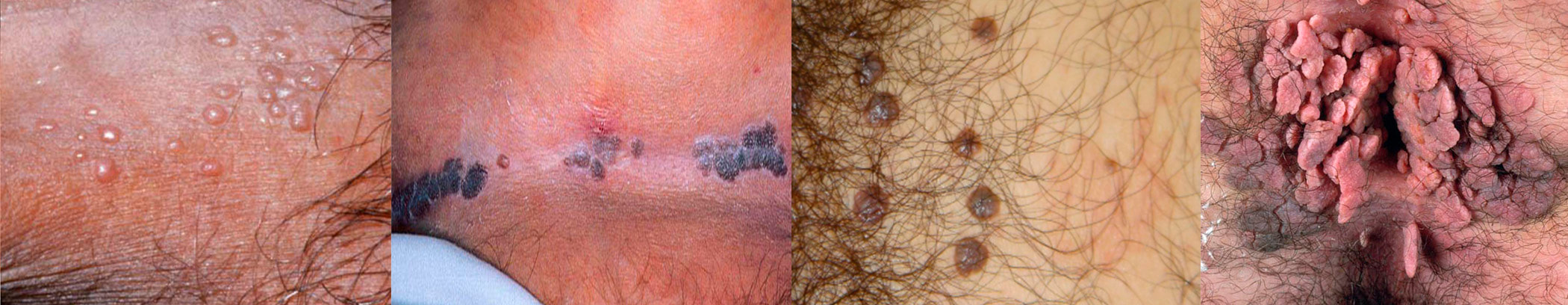
➧Sinais e sintomas causados pelo papilomavírus humano (HPV)
➧História natural e curso clínico da infecção pelo papilomavírus humano (HPV)
➧Papilomavírus humano (HPV) associado ao câncer anal e orofaríngeo
➧Diagnóstico clínico do papilomavírus humano (HPV)
➧Biópsia no diagnóstico do papilomavírus humano (HPV)
➧Gerenciamento dos parceiros sexuais do paciente com HPV
➧Diagnóstico diferencial da infecção pelo papilomavírus humano (HPV)
➧Vacina contra papilomavírus humano (HPV)
➧Tratamento do condiloma acuminado (verrugas anogenitais) - tratamento do papilomavírus humano (HPV)
➧Neoplasia Intraepitelial Anal (NIA) associada a infecção pelo papilomavírus humano (HPV)
|
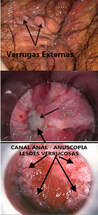
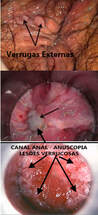
●Envolvimento do canal anal - O exame proctológico (toque retal e anuscopia) examina o canal anal e deve ser realizado em todos os pacientes com verrugas perianais ou externas, exceto naqueles com lesões muito grande e/ou extensas devido a dor e trauma dos exames. Não existe risco em levar o vírus para dentro do canal anal, uma vez que a infecção pelo HPV é de campo, e provavelmente todo e segmento já está comprometido. A relação anal é, provavelmente, o principal meio para a disseminação do HPV para o canal anal, mas não o único; outros tipos de contato também podem transmitir, como os dedos ou brinquedos ou outros órgãos genitais infectados pelo HPV.
|
|
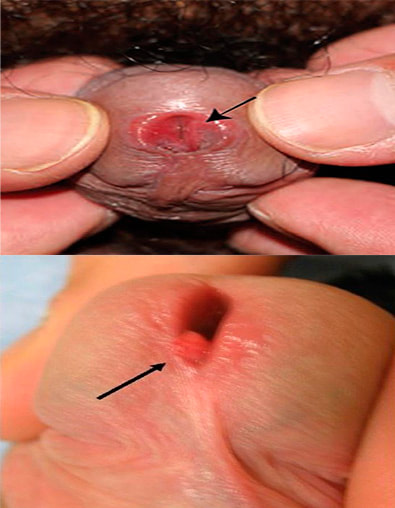
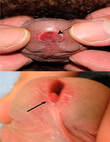
●Envolvimento da uretra masculina - A condiloma uretral ocorre ocasionalmente e é mais comumente encontrada no meato externo e na uretra distal, mas também pode se desenvolver em locais mais proximais dentro da uretra. A obstrução da bexiga é uma complicação rara. O exame físico deve incluir uma avaliação visual do orifício uretral. Pacientes com verrugas na uretra e/ou sintomas uretrais (dor ou ardência) devem ser encaminhados ao urologista para avaliação adicional.
|
Parceiros sintomáticos devem ser encaminhados ao seu médico para avaliação e possível tratamento.
Estudos descobriram que duas doses da vacina em indivíduos jovens têm imunogenicidade semelhante em comparação com três doses, tanto para a proteção contra os cânceres quanto para as verrugas genitais.
Pessoas vivendo com HIV/Aids deverão receber a vacina independentemente do CD4 e preferencialmente em terapia antirretroviral.
Os indivíduos a serem submetidos a transplantes de órgãos sólidos devem receber a vacinação HPV no pré-transplante, seguindo o esquema de três doses (0, 2 e 6 meses) entre as faixas etárias de 9 e 26 anos de idade, em homens e mulheres. Contudo pode-se completar o esquema após o transplante, devendo seguir um período de 6 a 12 meses subsequente a este procedimento médico.
|
D1 para D2
1 mês (30 dias) |
D2 para D3
4 meses (120 dias) |
D1 para D3
6 meses (180 dias) |
Pessoas sexualmente ativas devem ser vacinados de acordo com as indicações específicas por idade. A infecção pelo HPV detectada pelo Papanicolaou, presença de verrugas genitais e outros exames NÃO é contra indicação à vacinação contra o HPV. No entanto, a imunização é menos eficaz para aqueles que já foram infectados com um dos tipos de HPV presentes na vacina.
Dor no local da aplicação, edema e eritema de intensidade moderada.
Cefaleia;
Febre de 38ºC ou mais;
Síncope (ou desmaio);
Reações de hipersensibilidade.
A partir de 2017 – vacinação de 80% das meninas de 12 a 13 anos;
De 2007 a 2009 – vacinação de 65% das meninas de 13 a 18 anos;
De 2007 a 2009 – vacinação de 50% das mulheres de 18 a 26 anos;
Mulheres mais velhas e homens, tanto heterossexuais como homossexuais, não foram vacinados.
|
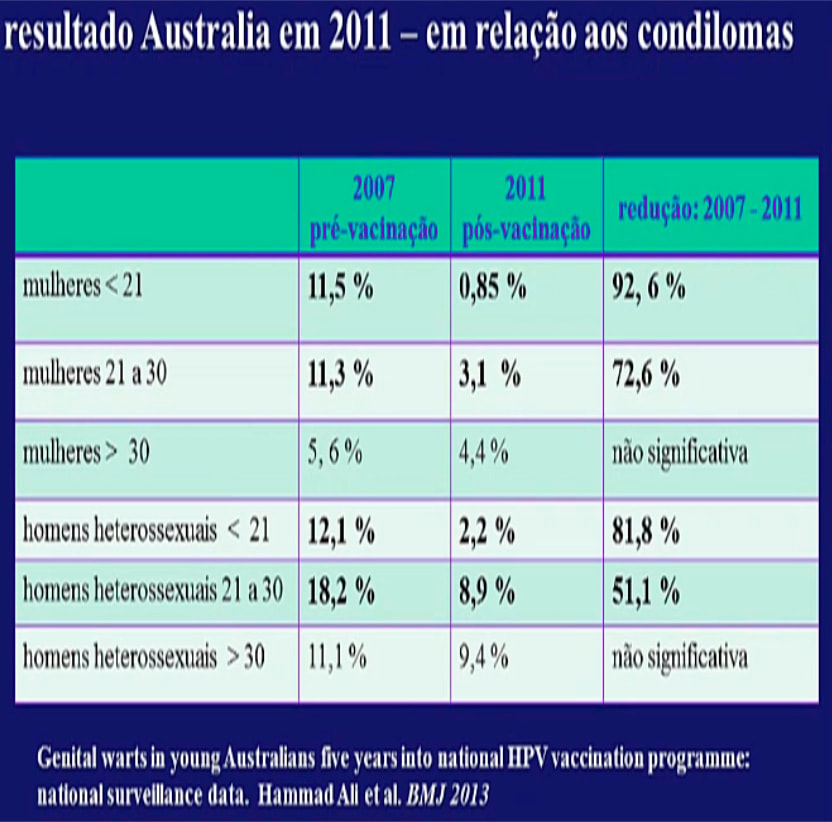
1- Mulheres examinadas 3 anos depois obtiveram uma redução de 92% da incidência dos condilomas, sendo que os 0,8% com condilomas não haviam sido vacinadas. Portanto em 2011, nenhuma das mulheres vacinadas com menos de 21 anos desenvolveram os condilomas, eficácia de 100%.
2- Já nas mulheres de 21 a 30 anos, que nem todas foram vacinadas, a redução foi significativa, embora menor. 3- Mulheres acima de 30 anos não foram vacinadas e não houve redução. 4- Homens não foram vacinados, mas os com menos de 21 anos tiveram uma redução de 82% devido ao efeito rebanho. Os homens que mantiveram relação com mulheres vacinadas não contraíram a infecção pelo HPV. |
6- Homens que mantiveram relação com grupos de mulheres não vacinadas, não houve redução.
2- As verrugas anogenitais aparecem semanas a muitos meses após o contato transmissível. Na maioria das pessoas o momento da infecção não pode ser determinado. Portanto, o aparecimento das verrugas anogenitais não garante infidelidade dentro do relacionamento sexual atual.
3- Pacientes com verrugas anogenitais apresentam um risco maior de estar com outras infecções sexualmente transmissíveis.
4- Pessoas com verrugas anogenitais podem transmitir o HPV aos parceiros sexuais, portanto devem informar aos parceiros sexuais atuais sobre seu diagnóstico. Parceiros sexuais podem se beneficiar de uma avaliação de verrugas anogenitais e outras infecções sexualmente transmissíveis. Os pacientes devem evitar o contato sexual com novos parceiros até que as verrugas sejam tratadas com sucesso.
5- Há uma variedade de tratamentos eficazes para verrugas anogenitais. Sem tratamento, as verrugas anogenitais podem desaparecer espontaneamente, persistir ou progredir. Estima-se que aproximadamente um terço das verrugas anogenitais regridem sem tratamento dentro de quatro meses, mas não é possível prever quais verrugas anogenitais desaparecerão sem tratamento.
6- A infecção pelo HPV pode permanecer após a remoção completa das verrugas anogenitais e podem ser transmitidas a outras pessoas, mesmo quando não sejam visíveis. Não está claro se a erradicação das verrugas anogenitais diminui a transmissão futura do HPV.
7- O uso de preservativo reduz a transmissão das verrugas anogenitais; no entanto, a infecção pelo HPV pode ser transmitida através do contato com a pele infectada que não é coberta pelo preservativo.
|
Envolvimento do canal anal - O exame proctológico (toque retal e anuscopia) examina o canal anal e deve ser realizado em todos os pacientes com verrugas perianais ou externas, exceto naqueles com lesões muito grande e/ou extensas devido a dor e trauma dos exames. Não existe risco em levar o vírus para dentro do canal anal, uma vez que a infecção pelo HPV é de campo, e provavelmente todo e segmento já está comprometido. A relação anal é, provavelmente, o principal meio para a disseminação do HPV para o canal anal, mas não o único; outros tipos de contato também podem transmitir, como os dedos ou brinquedos ou outros órgãos genitais infectados pelo HPV.
|
|
Envolvimento uretral - A condiloma uretral ocorre ocasionalmente e é mais comumente encontrada no meato externo e na uretra distal, mas também pode se desenvolver em locais mais proximais dentro da uretra. A obstrução da bexiga é uma complicação rara. O exame físico deve incluir uma avaliação visual do orifício uretral. Pacientes com verrugas na uretra e/ou sintomas uretrais (dor ou ardência) devem ser encaminhados ao urologista para avaliação adicional.
|
➧Podofilina;
➧Imiquimode;
➧Podofilotoxina.
➧Ácido tricloroacético;
➧Remoção cirúrgica (excisão ou eletrocauterização);
➧Crioterapia.
1- Remover as verrugas para reduzir a carga viral, permitindo que a imunidade consiga eliminar o restante ou facilitar o tratamento das lesões residuais com outro tratamento.
2- Melhorar os sintomas (se presentes) e os aspectos psicossociais.
3- Não existe um tratamento ideal para todos os pacientes ou todas as verrugas.
1- As verrugas anogenitais pequenas ou únicas (por exemplo, <1 cm) podem ser tratadas com qualquer um dos tratamentos de primeira linha tanto pelo paciente ou quanto pelo médico. Os tratamentos usados pelo médico são as de escolha, porque proporcionam resultados mais rápidos. Tanto a crioterapia quanto a eletrocauterização proporcionam bons resultados, mas podem resultar em discromia na pele (manchas claras ou escuras).
2- As verrugas extensas e/ou grandes pode ser melhor gerenciada com excisão cirúrgica ou eletrocauterização. Agentes tópicos são comumente usados no tratamento complementar de doença residual ou inicial para reduzir a carga viral.
3- Verrugas localizadas na região perianal e canal anal são tratadas de modo diferente das verrugas localizadas na zona de transição ou pectínea.
Alguns pacientes preferem tratar as verrugas em casa, enquanto outros preferem os resultados rápidos dos tratamentos administrados pelo médico.
O custo do tratamento com imiquimode pode ser proibitivo para alguns pacientes, enquanto o custo da podofilina é bem menor.
As reações inflamatórias locais são efeitos colaterais comuns da podofilina, podofilotoxina e imiquimode. Os efeitos colaterais sistêmicos também podem ocorrer no tratamento com imiquimode e podofilina. Os tratamentos ablativos usados pelo médico podem resultar em cicatrizes e discromias.
Procedimentos como crioterapia, excisão cirúrgica e eletrocauterização requerem médicos treinados para executar o procedimento e equipamento apropriado.
É frequente combinar o tratamento aplicado pelo médico e pelo próprio paciente (por exemplo, uso de tratamento tópico aplicado pelo paciente entre as sessões do tratamento aplicado pelo médico), na tentativa de aumentar a resposta ao tratamento. No entanto, os dados sobre a eficácia e segurança dessa abordagem são limitados.
O tratamento dos pacientes imunocomprometidos não difere da abordagem dos pacientes imunocompetentes. No entanto, o tratamento das verrugas é menos eficaz nos pacientes imunocomprometidos, podendo ser necessário tratamentos mais prolongados e um acompanhamento mais próximo.
|
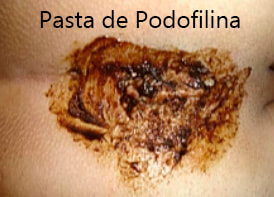
1- Podofilina a 25% em vaselina sólida - 1 frasco de 20 g (exclusivamente manipulado)
➧O próprio paciente aplica a pasta de podofilina nas áreas anogenitais e canal anal externo com verrugas. ➧Após a primeira aplicação, lavar após trinta a quarenta minutos. ➧Nas aplicações subsequentes, enxaguar após uma a quatro horas (não extrapolar seis horas). Repetir a aplicação, semanalmente, por até quatro a seis semanas. |
Pacientes grávidas ou em lactação, crianças e diabetes. Uso concomitante com corticosteroides. Distúrbios circulatórios ou em verrugas que sangram. Hipersensibilidade a podofilina.
Evitar usar em áreas extensas ou em mucosas (como a intra-anal na linha pectínea ou acima). Evitar contato com rosto, olhos, pele normal e feridas abertas.
Irritação local, (a área tratada sempre fica avermelhada, queimando, ardendo e coçando em graus variáveis podendo ferir após o término de cada ciclo), pode-se aplicar talco sobre a área onde foi aplicada a podofilina e como alternativa ou de forma conjunta pode-se usar também o creme hidratante com alta concentração de pró-vitamina B5, aplicando no local 1 a 3 vezes por dia iniciando no dia seguinte ao uso da podofilina, até melhorar do ardor.
Podem ocorrer após aplicações excessivas: náusea, vômito, dor abdominal, diarreia, paralisia do íleo, taquicardia, hipotensão, leucopenia transitória, trombocitopenia, insuficiência renal, hepatotoxicidade, neurotoxicidade tardia, incluindo alucinações visuais e auditivas, desorientação, confusão e delírio.
Uma caixa vem com 12 envelopes. Média de tratamento – 4 caixas (16 semanas).
Os pacientes devem aplicar o creme com imiquimode 5% diretamente sobre a área afetada pelas verrugas anogenitais e no canal anal externo, três vezes por semana (por exemplo, segunda, quarta e sexta-feira) até que as verrugas desapareçam ou por um período máximo de 16 semanas. Caso esqueça, use assim que se lembrar e então continue no esquema regular.
|
1- Antes de se deitar, lave as mãos e a área a ser tratada com água e sabonete neutro. Seque bem a área limpa. Abra um sachê novo de Imiquimode. Esprema-o, a fim de liberar o creme na ponta de seu dedo indicador.
2- Aplique uma camada fina de Imiquimode sobre a região afetada e esfregue suavemente até o creme desaparecer. 3- Após a aplicação, jogue fora o sachê e lave as mãos com água e sabão. 4- Deixe o creme agir por 6 a 10 horas sobre as verrugas genitais externas e no canal anal externo. Durante este período, evite qualquer banho ou ducha. 5- Após este período, lave a região tratada com água e sabonete suave. 6- Abra sempre um novo sachê a cada aplicação do produto. Após o uso, jogue-o fora. Nunca guarde a sobra do sachê para usá-la posteriormente. |
Estudos demonstraram que o imiquimode é superior ao placebo para alcançar regressão completa ou parcial das verrugas anogenitais, mas não identificaram superioridade em relação as taxas de recorrência ou desenvolvimento de novas verrugas.
O uso do medicamento obteve 46% de resposta completa, 44% de resposta parcial e 10% sem qualquer resposta em até 16 semanas de tratamento. A taxa de recidiva atingiu 11% em 24 semanas de seguimento. Efeitos adversos foram relatados por 45% dos pacientes, sendo ardor leve a moderado (25%), ardor intenso (7%), dermatite ulcerativa (8%) e efeitos sistêmicos (5%). O desbastamento (poda) das verrugas maiores e/ou extensas aumenta as taxas de sucesso do imiquimode.
Reações inflamatórias no local leve a moderadas como vermelhidão, irritação, edema e descamação, são comuns com o uso de imiquimod 5% de creme, mas não acarreta a suspensão do tratamento. Na presença de úlceras, erosões e vesículas pode ser necessário suspender temporariamente por vários dias, se necessário, de acordo com o desconforto do paciente ou gravidade da reação. O tratamento pode ser reiniciado quando a reação melhorar. Curativos não-oclusivos (por exemplo, gaze ou roupa íntima de algodão) podem ser usados no tratamento de reações cutâneas.
Além disso, pode ocorrer despigmentação no local do tratamento. Sintomas semelhantes aos da gripe ocorrem com pouca frequência.
Taxas de sucesso de 43 a 70% com o uso de creme com podofilotoxina a 0,15% por quatro semanas. As taxas de recorrência variam muito dependendo dos critérios usados para avaliar os intervalos de recaída e acompanhamento.
Os pacientes devem aplicar podofilotoxina duas vezes ao dia por três dias consecutivos e depois suspender o uso por quatro dias consecutivos. Este curso de uma semana pode ser repetido até quatro vezes até que as verrugas não sejam mais visíveis.
A área total de tratamento não deve exceder 10 cm2 e o volume total de podofilotoxina deve ser limitado a 0,5 ml por dia. A área na qual a podofilotoxina é aplicada não deve conter lesões ou feridas abertas. A podofilotoxina deve ser lavada uma a quatro horas após a aplicação, a fim de minimizar a irritação local. Se possível, o médico deve aplicar o primeiro tratamento para demonstrar os locais corretos de aplicação e a técnica adequada. A relação sexual deve ser evitada enquanto a podofilotoxina estiver na pele.
Os efeitos adversos locais foram principalmente leves ou moderados e não aumentaram durante o período de tratamento.
As reações graves ocorreram com mais frequência durante as duas primeiras semanas de tratamento.
Os efeitos adversos comuns incluem dor local, inflamação, erosões, queimação ou coceira.
A aplicação excessiva pode contribuir para efeitos adversos. O efeito adverso sistêmico mais comum relatado durante os estudos clínicos foi dor de cabeça.
O ácido tricloroacético deve ser aplicado com cuidado, pois uma aplicação excessiva pode causar danos aos tecidos adjacentes.
A retirada cirúrgica, com tesoura ou bisturi, das lesões grandes (> 1 cm) seguido de sutura pode ser associada à eletrocauterização. Excisões mais extensas sob anestesia geral podem ser necessárias para remover verrugas extensas ou volumosas.
Os possíveis efeitos colaterais após o tratamento incluem formação de bolhas, despigmentação e cicatrizes. Pode ocorre aumento ou diminuição da sensibilidade no local após a crioterapia, mas são quase sempre temporárias.
2- Anuscopia de alta resolução (colposcopia anal) aos 6 meses.
3- A parir daí, exame proctológico convencional a cada 6 meses.
4- Após 1 ano e meio sem lesões, fazer anuscopia de alta resolução (colposcopia anal), se normal encerrar o seguimento.
5- Nos pacientes HIV positivos ou HIV negativos de alto risco (grande número de parceiros sexuais) fazer acompanhamento anual sempre.
Os pacientes devem ser instruídos a retornar para avaliação clínica se novas verrugas se desenvolverem após o tratamento.
2- Ácido tricloroacético a 90% nas verrugas internas ao nível ou acima da linha pectínea.
3- Sessões semanais durante 4 a 6 semanas.
4- Após o tratamento eficaz (cerca de 40%) realiza-se o seguimento como descrito acima. Tem a opção do reforço com o imiquimode para aumentar a imunidade local no intuito de diminuir as recorrências.
5- No tratamento não eficaz (40% com redução significativa e apenas 20% sem qualquer resposta), pode-se tentar novo ciclo de tratamento com a podofilina e o ácido tricloroacético ou indica-se a cirurgia (eletrocauterização na maioria e às vezes a excisão com tesoura).
6- Na recidiva após o tratamento cirúrgico ou mesmo antes, tem a opção de usar o imiquimode (imunoterapia). Alguns têm usado o imiquimode após a erradicação das verrugas para melhorar a imunidade local reduzindo as recorrências. Também é opção como tratamento primário, substituindo a podofilina e o ácido tricloroacético, com resultados um pouco melhores. Vantagem de ser aplicado pelo próprio paciente em casa. A desvantagem é o seu alto custo.
7- Alguns médicos tem a rotina de recomendar a vacina para todos os pacientes, objetivando evitar a coinfecção por outros tipos de HPV.
➧NIA de alto grau – NIA com displasia moderada, grau II ou com displasia acentuada (severa), grau III.
➧Infecção latente - Ocorre após a infecção pelo HPV, isto é, antes de qualquer evidência clínica da infecção (pode durar oito meses ou mais, mas alguns indivíduos nunca desenvolverão lesões clinicamente aparentes);
➧Infecção com lesões assintomáticas no canal anal - Geralmente lesões planas que podem ser difíceis de identificar na anuscopia convencional; e
➧Lesões sintomáticas condilomatosas típicas no canal anal - Verrugas ou placas isoladas ou confluentes.
Algumas pessoas, particularmente HIV-positivos, podem estar infectados por dois ou mais subtipos de HPV, o que está associado ao aumento do risco de desenvolver a NIA de baixo grau e posteriormente a de alto grau.
➧A infecção pelo HPV no canal anal, número e tipo de HPV(s) presente(s) e comportamento sexual de risco são os fatores de risco que se associam significativamente à presença da NIA.
➧A prevalência da infecção anal pelo HPV em HSH é alta (50 e 60%), mas estável nas idades entre 18 e 50 anos. A estabilidade da prevalência é consistente com as observações de que a infecção pelo HPV é transitória e que os indivíduos permanecem em risco de desenvolver novas infecções pelo HPV se o comportamento de alto risco continuar.
➧Entre as mulheres HIV negativas, as taxas inicialmente altas de HPV nas faixas etárias mais jovens não se sustentam a longo prazo. Entre as mulheres que vivem com HIV, a infecção anal por HPV parece ser pelo menos tão comum quanto a infecção do colo de útero por HPV. A prevalência da infecção anal pelo HPV na mulher com neoplasia intraepitelial no colo do útero, chega a 90%. Apresentam portanto, um risco aumentado de neoplasia intraepitelial anal simultâneo. Toda paciente com HPV ou NIA no colo uterino devem ser examinadas pelo coloproctologista.
➧É importante reforçar que a relação anal receptiva não é o único fator de risco para a aquisição da infecção anal por HPV em mulheres; alguns dados sugerem que a limpeza de frente para trás após a evacuação está associada a taxas mais altas de infecção anal pelo HPV do que dar tapinhas ou limpar na outra direção.
➧Os fatores de risco envolvidos no aumento da prevalência da infecção pelo HPV, neoplasia intraepitelial anal e câncer anal em HSH HIV positivos incluem: comportamento sexual de alto risco, infecção por vários subtipos de HPV e maior frequência do comprometimento do canal anal.
➧A terapia antirretroviral não parece alterar a prevalência da neoplasia intraepitelial anal, e ainda, pode estar associada ao aumento da incidência de progressão da neoplasia intraepitelial anal de alto grau para câncer anal devido ao aumento da expectativa de vida das pessoas infectadas pelo HIV.
Nas mulheres incluem história de câncer do colo do útero, câncer vulvar, neoplasia intraepitelial do colo do útero de alto grau ou neoplasia intraepitelial vulvar, infecção no colo do útero pelo HPV 16 em mulheres HIV negativas com idade superior a 45 anos e imunossupressão iatrogênica (como após o transplante de órgão sólido).
A maioria das NIAs de baixo grau são provocadas pelos subtipos de HPV de baixo risco que não progridem diretamente para a NIA de alto grau. Embora, as NIAs de baixo grau estejam associadas ao risco aumentado da presença das NIAs de alto grau em um local diferente no ânus devido aos fatores de riscos compartilhados, como infecção pelo HPV (especificamente a presença simultânea de subtipos de HPV oncogênicos). Portanto, não está claro se as lesões de baixo grau progridem diretamente para o alto grau ou é apenas um marcador de risco aumentado para as NIAs de alto grau incidente em um local diferente.
O diagnóstico da neoplasia intraepitelial anal requer, em última análise, exame histopatológico das amostras citológicas e da biópsia anal.
A avaliação de indivíduos assintomáticos com risco aumentado de neoplasia intraepitelial anal começa pela anamnese abrangente, exame físico e proctológico.
• História de doenças provocadas pelo papilomavírus humano (HPV) e outras infecções sexualmente transmissíveis;
• História sexual, incluindo investigação específica sobre relações sexuais receptivas desprotegidas;
• Sorologia para HIV e marcadores de infecção (CD4 e carga viral);
• Sintomas anorretais (dor, coceira, sangramento, corrimento, irritação e tenesmo);
• História de tabagismo; e
• Uso de medicamentos associados à imunossupressão.
• Inspeção visual da pele perianal;
• Exame digital;
• Exame dos linfonodos inguinais e de alta resolução (anuscopia) do canal anal; e
• Se a citologia anal for planejada, ela deve ser realizada antes do exame digital e da anuscopia sem o uso de lubrificante.
• Mulheres HIV negativas com mais de 45 anos com HPV cervical sorotipo 16;
• Homens e mulheres HIV positivos;
• Imunossupressão iatrogênica (por exemplo, receptores de transplante de órgão sólido, corticosteroides orais a longo prazo);
• Mulheres com histórico de displasia ou câncer cervical, vulvar ou vaginal de alto grau; e
• Pessoas com história de verrugas anais (condiloma anal).
• Estes grupos também pode se beneficiar da triagem com a citologia anal: homens HIV positivos que fazem sexo com mulheres, mesmo sem histórico de relações sexuais anal; mulheres HIV positivas; e mulheres HIV negativa com mais de 45 anos de idade que têm HPV cervical 16.
• Outros grupos de risco também podem ser considerados para a triagem da neoplasia intraepitelial anal de alto grau, caso a caso.
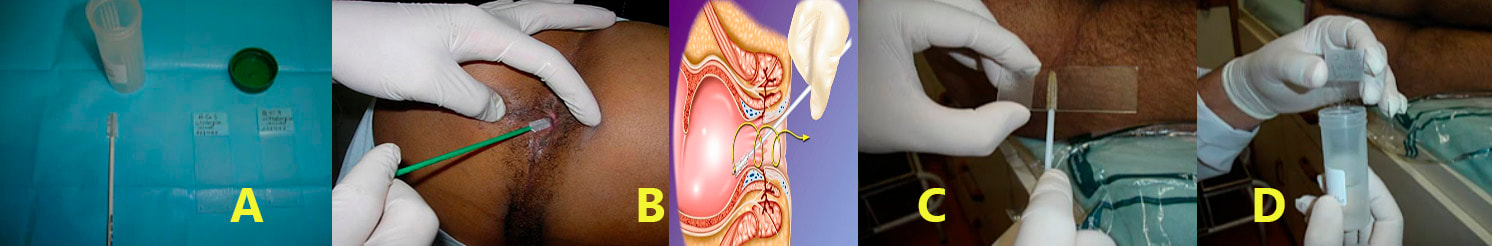
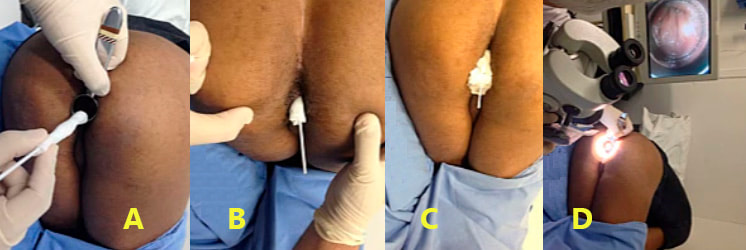
B- Com o paciente na posição genupeitoral ou em decúbito lateral esquerdo, a zaragatoa é gentilmente inserida no ânus até ultrapassar o canal anal. Para então ser retirado com pressão lateral em espiral para pegar amostras de toda a circunferência do canal anal. Deste modo são coletadas amostradas celulares do reto inferior, zona de transição escamo-colunar e canal anal.
C- Após a remoção, a amostra pode ser espalhada na lâmina e fixada convencionalmente em etanol ou usar a técnica em citologia líquida. O último método é preferível, quando disponível, pois parece produzir melhores resultados.
D- A sensibilidade da citologia anal para detectar neoplasia intraepitelial anal comprovado por biópsia em HSH HIV positivos e negativos é de 81 e 50%, respectivamente. Semelhante à citologia cervical para a detecção de doença do colo uterino.
Alternativamente, pessoas consideradas de alto risco para neoplasia intraepitelial anal, como HSH HIV positivos, pode ser encaminhados diretamente para anuscopia de alta resolução e biópsia, dada a alta prevalência bem documentada neoplasia intraepitelial anal nesses indivíduos.
• No entanto, os pacientes com NIA de baixo grau podem optar por fazer algum tratamento por vários motivos, incluindo sintomas (queimação, coceira e sangramento) ou sofrimento psicológico. Pacientes com NIA de baixo grau que não são tratados devem ser acompanhados a cada seis meses devido à alta taxa de progressão para NIA de alto grau.
• Resumindo: NIA de baixo grau – seguimento, mas o tratamento é recomendado quando sintomática (geralmente quando comprometem mais de 1/3 da circunferência do canal anal) e/ou na presença de verrugas ou pelo desejo do paciente.
• Para lesões comprometem mais de 1/3 da circunferência do canal anal, o tratamento pode ser a eletrocauterização, mas para evitar estenose, recomenda-se escalonar o tratamento, cauterizando no máximo 1/3 da circunferência do canal anal por sessão. Alternativamente, pode-se usar o imiquimode a 5% creme dentro do canal anal, uma vez que pode resultar na resolução completa das lesões ou na redução do tamanho permitindo assim, o uso da eletrocauterização. Com a vantagem de que o imiquimode pode ser aplicado pelo próprio paciente.
• Resumindo: NIA de alto grau – tratamento combinado (infecção de campo) tópico (imiquimode) com a cirúrgica (excisão e eletrocauterização sob anestesia local e sedação).
• Lesões discretas e pequenas podem ser tratadas com destruição local ou cirúrgica (excisão ou eletrocauterização), enquanto lesões mais extensas podem ser abordadas inicialmente com aplicação do imiquimode a 5% creme, além de observação atenta e contínua, antes de considerar a intervenção cirúrgica.
• Os tratamentos iniciais envolvem medidas mais conservadoras que, novamente, dependem da extensão e tamanho da(s) lesão(s).
• Não há estudos randomizados comparando diferentes modalidades, e a seleção da modalidade é amplamente empírica.
• Aplicado no canal anal pelo médico.
• Opção para lesões pequenas (base <1 cm2).
• A aplicação local do ácido tricloroacético (TCA) a 90% é geralmente bem tolerada, mas pode ocasionalmente ser dolorosa.
• Em estudos, 60 a 80% das lesões evoluíram para epitélio normal ou NIA de baixo grau após uma única sessão de tratamento, e apenas duas lesões (2%) necessitaram de mais de duas sessões de tratamentos.
• Aplicado no canal anal pelo próprio paciente, de acordo com o preconizado (ver acima).
• Pode resultar na resolução patológica da NIA de alto grau anal em homens HIV-positivos que fazem sexo com homens (HSH), quando combinado com a terapia antirretroviral (TARV). Essa abordagem parece ser ainda melhor nos pacientes com doença multifocal disseminada.
• Em uma série relatada, 28 homens com NIA de alto grau foram tratados com imiquimode aplicado no canal anal três vezes por semana durante quatro meses. Dos 28 pacientes que receberam imiquimod, quatro tiveram resolução completa e oito tiveram o NIA de alto grau rebaixado para NIA de baixo grau. Apenas 1 dos 25 pacientes que receberam placebo tiveram resolução do NIA de alto grau. Em um acompanhamento médio de três anos, 61% dos pacientes mantiveram a ausência sustentada da NIA de alto grau.
Existem muitos, incluindo: eritema, ulceração e sangramento com sintomas associados de irritação, queimação e dor, e ocasionais sintomas sistêmicos semelhantes aos da gripe com imiquimode. No entanto, a maioria das terapias locais é muito bem tolerada, com apenas sintomas mínimos experimentados pelo paciente
• A ablação por eletrocautério também é frequentemente usada para tratar a NIA de alto grau, baixo grau e verrugas da região perianal e do canal anal.
• A eficácia foi abordada em uma análise retrospectiva de 330 pacientes com NIA de alto grau que foram seguidos com vigilância pós-tratamento com a anuscopia de alta resolução e biópsia das lesões suspeitas. Em uma média de 12 meses após a ablação, aproximadamente 45% dos participantes desenvolveram recorrência local, enquanto 60% desenvolveram recorrência geral. Nenhum paciente desenvolveu carcinoma espinocelular invasivo (CEC).
• Resultados semelhantes foram observados em uma série de 232 homens tratados com eletrocautério. A probabilidade de controle da doença das lesões iniciais após um único tratamento foi de aproximadamente 80%. A doença recorrente ocorreu em homens HIV negativos e HIV positivos (53 e 6%, respectivamente).
• Pacientes com lesões muito grandes e/ou extensas, a combinação do tratamento cirúrgico (eletrocauterização ou excisão cirúrgica) para as lesões maiores, deixando as menores para o tratamento tópico pelo médico ou pelo próprio paciente, parece ser uma opção viável.
• A alta taxa de recorrência local, mesmo em pacientes inicialmente considerados completamente tratados com um único procedimento, exige vigilância cuidadosa após o tratamento. No entanto, a maioria dessas recorrências pode ser gerenciada com sucesso com tratamento local.
A abordagem cirúrgica pode envolver ressecção local ampliada das lesões com fechamento primário da pele, retalhos de avanço (V-Y, S, C), enxerto cutâneo ou anoplastia.
• É importante ressaltar que o maior problema deste tratamento é a alta morbidade e apresenta taxas de recorrência (ou persistência) das NAI de alto grau entre 10 e 25%, mesmo quando se utiliza minucioso mapeamento pré-operatório. Assim, as terapias ablativas locais como a eletrocauterização constituem alternativas com menor morbidade que vêm ganhando muitos adeptos como alternativa às excisões ampliadas.