Abordagem Sindrômica das IST
A abordagem sindrômica consiste em incluir as IST dentro de síndromes pré-estabelecidas, baseada em sinais e sintomas, para simplificar a identificação da causa e assim, iniciar o tratamento imediatamente, mesmo na ausência dos resultados de exames confirmatórios, como também o aconselhamento e a orientação ao paciente e seu parceiro, além de incluir a oferta da sorologia para sífilis, HIV e hepatite B e C na data correta para a detecção dos anticorpos específicos.
➧ Introdução
➧ História clínica dos pacientes com suspeita de IST
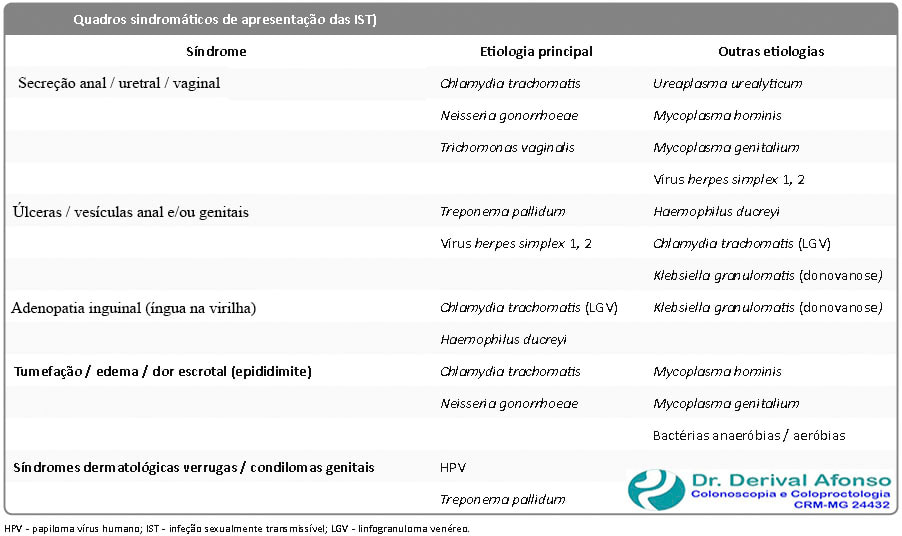
➧ Síndrome de secreção (corrimento) anal (masculino e feminino), uretral (masculino) e/ou vaginal (feminino)
➧ Síndrome de ulceração anal e/ou genital e/ou vesículas anal e/ou genital
➧ Verrugas e/ou condilomas anal e/ou genitais
➧ Outros sinais e/ou sintomas
➧ Exames laboratoriais para confirmar a suspeita clínica das IST
➧ Tratamento empírico com base no quadro sindrômico das IST
➧ Seguimento após o início do tratamento sindrômico das IST
➧ Fatores de mau prognóstico do tratamento sindrômico das IST
√ Nem toda a infecção anogenital é uma IST e nem todas as IST se manifestam por doença do trato anal e genital;
√ Pode coexistir mais do que uma síndrome na mesma pessoa, devendo-se tratar adequadamente todas as possibilidades;
√ A presença de uma IST aumenta o risco de infecção pelo vírus da imunodeficiência humana (HIV);
√ A infecção por HIV, a hepatite viral B e C, a doença inflamatória pélvica, a escabiose e a pediculose púbicas estão fora da abordagem sindrômicas das IST.
√ Pode coexistir mais do que uma síndrome na mesma pessoa, devendo-se tratar adequadamente todas as possibilidades;
√ A presença de uma IST aumenta o risco de infecção pelo vírus da imunodeficiência humana (HIV);
√ A infecção por HIV, a hepatite viral B e C, a doença inflamatória pélvica, a escabiose e a pediculose púbicas estão fora da abordagem sindrômicas das IST.
A consulta dos pacientes com (suspeita de) IST implica criar um ambiente de confiança para que ele(a) possa falar da sua vida pessoal e sexual. Deve ser confidencial, personalizada, sem juízos de valor, em linguagem compreensível, com formulação de perguntas inicialmente abertas e posteriormente fechadas.
Sinais e sintomas das IST
√ Sinais e sintomas específicos: disúria (dor ao urinar), dispareunia (dor na relação sexual), corrimentos anal, uretral e vaginal, dor abdominal, dor pélvica, adenopatias (ínguas), lesões anogenitais.
√ Sinais e sintomas inespecíficos / constitucionais: perda de peso, anorexia (perda de apetite), astenia (fraqueza), exantema (manchas na pele), dermatite, alopecia (queda de cabelo), artrite.
√ Data de início dos sinais e sintomas.
√ Evolução dos sinais e sintomas.
√ Data do provável contágio.
√ Uso de antibióticos até dois meses antes.
√ Sinais e sintomas inespecíficos / constitucionais: perda de peso, anorexia (perda de apetite), astenia (fraqueza), exantema (manchas na pele), dermatite, alopecia (queda de cabelo), artrite.
√ Data de início dos sinais e sintomas.
√ Evolução dos sinais e sintomas.
√ Data do provável contágio.
√ Uso de antibióticos até dois meses antes.
Antecedentes pessoais
√ História de IST anterior e/ou se já está em tratamento de outra;
√ Uso atual de medicamentos;
√ Data de início da vida sexual ativa (VSA);
√ Orientação sexual;
√ Data das últimas relações sexuais desprotegidas ou não;
√ Número de parceiros(a) sexuais nos últimos 60 dias;
√ Métodos de contracepção (não esquecer o preservativo);
√ Vacinação: papiloma vírus humano (HPV) e hepatite B (VHB).
√ Uso atual de medicamentos;
√ Data de início da vida sexual ativa (VSA);
√ Orientação sexual;
√ Data das últimas relações sexuais desprotegidas ou não;
√ Número de parceiros(a) sexuais nos últimos 60 dias;
√ Métodos de contracepção (não esquecer o preservativo);
√ Vacinação: papiloma vírus humano (HPV) e hepatite B (VHB).
Antecedentes familiares
√ IST;
√ História social e ambiente familiar.
√ História social e ambiente familiar.
Exame físico geral e específico
√ Boca: procurar placas esbranquiçadas e/ou úlceras;
√ Cabeça, pescoço, axilas e virilhas: pesquisar adenopatias (ínguas);
√ Pele do tronco e dos membros: observar se erupção cutânea;
√ Púbis: pesquisar parasitas;
√ Períneo, ânus e genitais: pesquisar secreção uretral (em ambos os sexos) e/ou colo do útero, úlceras, vesículas, outras lesões anogenitais, sinais inflamatórios anogenitais e alterações na cor da pele e mucosas;
√ No escroto: pesquisar irregularidades, edema, espessamento/tumefação e sensibilidade dos testículos e do epidídimo;
√ Palpação abdominal superficial e profunda;
√ Exame proctológico e ginecológico, se viáveis.
√ Cabeça, pescoço, axilas e virilhas: pesquisar adenopatias (ínguas);
√ Pele do tronco e dos membros: observar se erupção cutânea;
√ Púbis: pesquisar parasitas;
√ Períneo, ânus e genitais: pesquisar secreção uretral (em ambos os sexos) e/ou colo do útero, úlceras, vesículas, outras lesões anogenitais, sinais inflamatórios anogenitais e alterações na cor da pele e mucosas;
√ No escroto: pesquisar irregularidades, edema, espessamento/tumefação e sensibilidade dos testículos e do epidídimo;
√ Palpação abdominal superficial e profunda;
√ Exame proctológico e ginecológico, se viáveis.
➧No homem e mulher pode acompanhar-se de tenesmo (vontade constante de evacuar, mesmo que não haja necessidade), dor anal, disúria (dor, ardor, ou desconforto ao urinar) e polaciúria (urinar pouca quantidade muitas vezes ao dia).
➧Na mulher pode acompanhar-se de prurido vaginal e/ou dispareunia (dor na relação sexual).
➧Na mulher pode acompanhar-se de prurido vaginal e/ou dispareunia (dor na relação sexual).
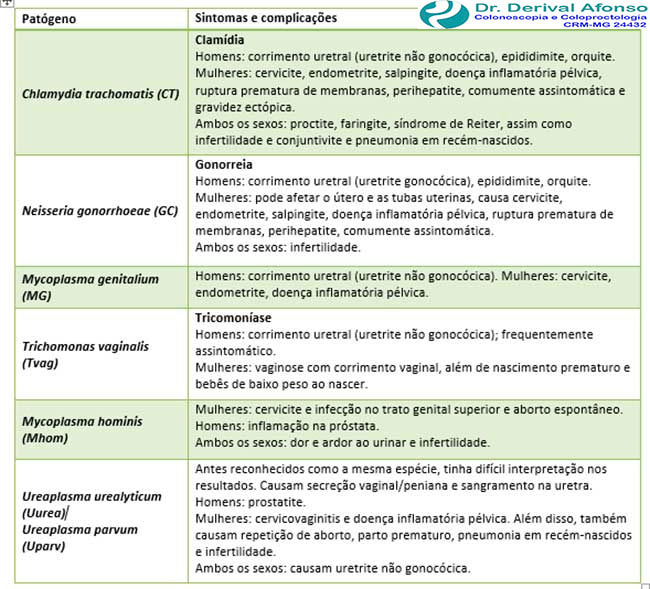
Causas mais frequentes no homem
√ Retite e/ou uretrite gonocócica (N. gonorrhoeae) ou não gonocócica, principalmente por clamídia (C. trachomatis); outras causas são a Mycoplasma genitalium (M. genitalium), Mycoplasma hominis (M. hominis), Trichomonas vaginalis (T. vaginalis) e Ureaplasma urealyticum (U. urealyticum). Vírus herpes simplex (HSV) tipo 2 e/ou tipo 1.
Causas mais frequentes na mulher
√ Retite gonocócica (N. gonorrhoeae) ou não gonocócica principalmente por clamídia (C. trachomatis); outras causas são a outras causas são a Mycoplasma genitalium (M. genitalium), Mycoplasma hominis (M. hominis), Trichomonas vaginalis (T. vaginalis) e Ureaplasma urealyticum (U. urealyticum). Vírus herpes simplex (HSV) tipo 2 e/ou tipo 1.
√ Vaginite por gonorreia (N. gonorrhoeae) ou clamídia (C. trachomatis); outras causas são a T. vaginalis (fluxo profuso e fétido).
√ Outras causas de vaginite
- Vaginose bacteriana: apresenta-se com corrimento vaginal de odor desagradável geralmente de cor branca ou cinza e com aspecto cremoso, mais acentuado após a relação sexual e no período menstrual. Há frequentemente casos de doença assintomática, mas o exame ginecológico revelará corrimento aderido nas paredes da vagina e do vestíbulo).
- Candidíase vaginal: corrimento vaginal brancacento, leitoso, espesso e sem odor, tipo requeijão. Idealmente fazer exame microscópico a fresco de imediato (até 30 minutos) para diagnóstico diferencial.
Estas duas últimas situações não implicam tratar parceiros
√ Vaginite por gonorreia (N. gonorrhoeae) ou clamídia (C. trachomatis); outras causas são a T. vaginalis (fluxo profuso e fétido).
√ Outras causas de vaginite
- Vaginose bacteriana: apresenta-se com corrimento vaginal de odor desagradável geralmente de cor branca ou cinza e com aspecto cremoso, mais acentuado após a relação sexual e no período menstrual. Há frequentemente casos de doença assintomática, mas o exame ginecológico revelará corrimento aderido nas paredes da vagina e do vestíbulo).
- Candidíase vaginal: corrimento vaginal brancacento, leitoso, espesso e sem odor, tipo requeijão. Idealmente fazer exame microscópico a fresco de imediato (até 30 minutos) para diagnóstico diferencial.
Estas duas últimas situações não implicam tratar parceiros
➧Úlcera é uma solução de continuidade parcial ou total na pele e/ou na mucosa.
➧Vesículas correspondem a pequenas bolhas agrupadas e dolorosas; quando apresentam infecção secundária podem aparecer pústulas. Quando as vesículas e/ou pústulas se rompem dão lugar a úlceras superficiais.
➧Vesículas correspondem a pequenas bolhas agrupadas e dolorosas; quando apresentam infecção secundária podem aparecer pústulas. Quando as vesículas e/ou pústulas se rompem dão lugar a úlceras superficiais.
Causas mais frequentes nas úlceras anal
√ Úlcera superficial geralmente é por herpes genital: vírus herpes simplex (HSV) tipo 2 e em alguns casos tipo 1;
√ Úlcera única, indolor, de bordos regulares e de consistência dura ao tato geralmente é por Treponema pallidum (T. pallidum): sífilis;
√ Úlceras múltiplas, dolorosas, de bordos irregulares, fundo sujo e moles ao toque geralmente é por Haemophilus ducreyi (H. ducreyi): cancroide ou cancro mole.
√ Úlcera única, indolor, de bordos regulares e de consistência dura ao tato geralmente é por Treponema pallidum (T. pallidum): sífilis;
√ Úlceras múltiplas, dolorosas, de bordos irregulares, fundo sujo e moles ao toque geralmente é por Haemophilus ducreyi (H. ducreyi): cancroide ou cancro mole.
Causas mais frequentes nas vesículas anal
√ Herpes anal e/ou genital (HSV tipo 2 e, em alguns casos, tipo 1).
Nota:
√ O linfogranuloma venéreo (LGV) (C. trachomatis) pode inicialmente ter úlcera.
√ Neste quadro sindromático, exclui-se o granuloma inguinal (donovanose) Klebsiella granulomatis, pela sua quase inexistência no Brasil.
√ Na mulher, quando o herpes genital apresenta-se como uma úlcera superficial é importante fazer o diagnóstico diferencial com a candidíase genital, com a vulvite inespecífica mais acentuada e com lesões ulceradas não-IST que podem aparecer nas infecções por vírus Epstein-Barr (EBV), citomegalovírus (CMV), micoplasma e outras.
√ O linfogranuloma venéreo (LGV) (C. trachomatis) pode inicialmente ter úlcera.
√ Neste quadro sindromático, exclui-se o granuloma inguinal (donovanose) Klebsiella granulomatis, pela sua quase inexistência no Brasil.
√ Na mulher, quando o herpes genital apresenta-se como uma úlcera superficial é importante fazer o diagnóstico diferencial com a candidíase genital, com a vulvite inespecífica mais acentuada e com lesões ulceradas não-IST que podem aparecer nas infecções por vírus Epstein-Barr (EBV), citomegalovírus (CMV), micoplasma e outras.
Aparecem como lesões elevadas (aspeto de couve-flor) de cor carnosa, muitos vascularizadas e com diferentes graus de queratinização ao nível dos genitais, ânus ou pele circundante.
Causas mais frequentes para verrugas anal
√ O agente causal é o papiloma vírus humano (HPV), sendo os mais frequentes são os subtipos 6 e 11 que representam 90% dos casos; poderá ser necessário fazer o diagnóstico diferencial com o molusco contagioso, que também pode ser transmitido por contato sexual, embora não seja uma IST.
√ Condilomas sifilíticos da fase secundária da sífilis, condiloma plano.
√ Condilomas sifilíticos da fase secundária da sífilis, condiloma plano.
Adenopatia inguinal (íngua na virilha)
Tumefação inguinal dolorosa, a íngua inguinal: pode ser isolada, mas dependendo do agente etiológico pode ser acompanhado de úlcera anal e/ou genital.
Causas mais frequentes da adenopatia inguinal (íngua na virilha)
√ C. trachomatis que afeta os gânglios linfáticos originando o LGV;
√ H. ducreyi responsável pelo cancroide ou cancro mole e que se pode manifestar por adenopatia inguinal,
com ou sem úlcera.
√ Klebsiella granulomatis (granuloma inguinal ou venéreo - Donovanose)
√ C. trachomatis que afeta os gânglios linfáticos originando o LGV;
√ H. ducreyi responsável pelo cancroide ou cancro mole e que se pode manifestar por adenopatia inguinal,
com ou sem úlcera.
√ Klebsiella granulomatis (granuloma inguinal ou venéreo - Donovanose)
Tumefação / edema / dor escrotal
Na presença de dor e/ou inchaço escrotal é importante saber se existem fatores de risco para IST: sem parceiro(a) estável e/ou mais do que um parceiro(a) sexual sem uso de preservativo.
√ Não existe fator de risco para IST, descartar outras etiologias de emergência, como torção testicular e trauma testicular.
√ Sim, existe fator de risco para IST, os agentes etiológicos mais frequentes são a N. gonorrhoeae e a C. trachomatis.
√ Sim, existe fator de risco para IST, os agentes etiológicos mais frequentes são a N. gonorrhoeae e a C. trachomatis.
É recomendado, quando possível, fazer os exames para o diagnóstico específico em todos os quadros sindrômicos de IST, mas essa conduta não deve atrasar o início do tratamento.
➧ PCR – DNA para pesquisa vírus herpes simplex (HSV) tipo 2 e/ou tipo 1 e HPV (casos selecionados) na presença de sintomas ou rastreamento de pacientes assintomáticos com fatores de risco.
➧ PCR – DNA em tempo real BÁSICA para Chlamydia trachomatis, Neisseria gonorrhoeae, Mycoplasma genitalium e PLUS além da básica identifica também a Trichomonas vaginalis, Ureaplasma urealyticum, Ureaplasma parvum e Mycoplasma hominis/genitalium.
Nota: em uma única amostra da secreção pode identificar vários agentes.
➧ Anticorpos anti VIH 1 e 2 - 30 dias após o contato;
➧ Teste rápido para sífilis - 30 dias após o contato e se positivo fazer o VDRL e o FTA-ABS;
➧ Anticorpos anti-vírus da hepatite C (anti-VHC) - 60 dias após o contato;
➧ Antígeno HBs (AgHBs) e anticorpos anti-HBc da hepatite B - 60 dias após o contato;
➧ PCR – DNA em tempo real BÁSICA para Chlamydia trachomatis, Neisseria gonorrhoeae, Mycoplasma genitalium e PLUS além da básica identifica também a Trichomonas vaginalis, Ureaplasma urealyticum, Ureaplasma parvum e Mycoplasma hominis/genitalium.
Nota: em uma única amostra da secreção pode identificar vários agentes.
➧ Anticorpos anti VIH 1 e 2 - 30 dias após o contato;
➧ Teste rápido para sífilis - 30 dias após o contato e se positivo fazer o VDRL e o FTA-ABS;
➧ Anticorpos anti-vírus da hepatite C (anti-VHC) - 60 dias após o contato;
➧ Antígeno HBs (AgHBs) e anticorpos anti-HBc da hepatite B - 60 dias após o contato;
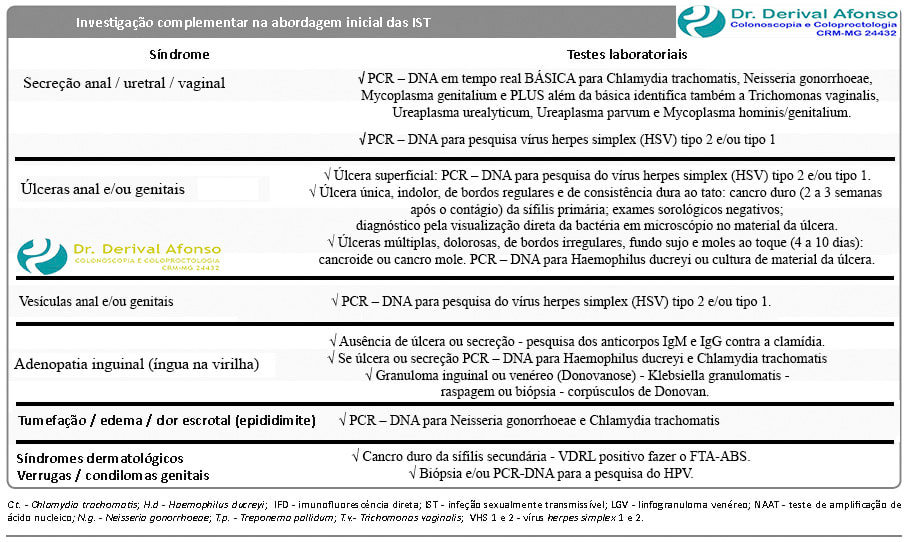
Secreção anal / uretral / vaginal (corrimento anal)
√ PCR – DNA em tempo real BÁSICA para Chlamydia trachomatis, Neisseria gonorrhoeae, Mycoplasma genitalium e PLUS além da básica identifica também a Trichomonas vaginalis, Ureaplasma urealyticum, Ureaplasma parvum e Mycoplasma hominis/genitalium.
√ PCR – DNA para pesquisa vírus herpes simplex (HSV) tipo 2 e/ou tipo 1.
√ PCR – DNA para pesquisa vírus herpes simplex (HSV) tipo 2 e/ou tipo 1.
Úlceras anal e/ou genitais
√ Úlcera superficial: PCR – DNA para pesquisa do vírus herpes simplex (HSV) tipo 2 e/ou tipo 1.
√ Úlcera única, indolor, de bordos regulares e de consistência dura ao tato: cancro duro (2 a 3 semanas após o contágio) da sífilis primária; exames sorológicos negativos; diagnóstico pela visualização direta da bactéria em microscópio no material da úlcera.
√ Úlceras múltiplas, dolorosas, de bordos irregulares, fundo sujo e moles ao toque (4 a 10 dias): cancroide ou cancro mole. PCR – DNA para Haemophilus ducreyi ou cultura de material da úlcera.
√ Úlcera única, indolor, de bordos regulares e de consistência dura ao tato: cancro duro (2 a 3 semanas após o contágio) da sífilis primária; exames sorológicos negativos; diagnóstico pela visualização direta da bactéria em microscópio no material da úlcera.
√ Úlceras múltiplas, dolorosas, de bordos irregulares, fundo sujo e moles ao toque (4 a 10 dias): cancroide ou cancro mole. PCR – DNA para Haemophilus ducreyi ou cultura de material da úlcera.
Vesículas anal e/ou genitais
√PCR – DNA para pesquisa vírus herpes simplex (HSV) tipo 2 e/ou tipo 1.
Adenopatia inguinal (íngua inguinal)
√ Ausência de úlcera e secreção: pesquisa dos anticorpos IgM e IgG contra a clamídia.
√ Se úlcera ou secreção: PCR – DNA para Haemophilus ducreyi e Chlamydia trachomatis
√ Granuloma inguinal ou venéreo (Donovanose) - Klebsiella granulomatis. Raspagem ou biópsia - corpúsculos de Donovan.
√ Se úlcera ou secreção: PCR – DNA para Haemophilus ducreyi e Chlamydia trachomatis
√ Granuloma inguinal ou venéreo (Donovanose) - Klebsiella granulomatis. Raspagem ou biópsia - corpúsculos de Donovan.
Tumefação / edema / dor escrotal (epididimite)
√ Ausência de úlcera e secreção: pesquisa dos anticorpos IgM e IgG contra a clamídia.
√ Se úlcera ou secreção: PCR – DNA para Neisseria gonorrhoeae e Chlamydia trachomatis.
√ Se úlcera ou secreção: PCR – DNA para Neisseria gonorrhoeae e Chlamydia trachomatis.
Síndrome dermatológicas. Verrugas ou condilomas genitais
√ Condiloma plano da sífilis secundária - VDRL positivo fazer o FTA-ABS.
√ Biópsia e/ou PCR-DNA para a pesquisa do HPV.
√ Biópsia e/ou PCR-DNA para a pesquisa do HPV.
O diagnóstico sindrômico inclui o tratamento empírico o mais precoce possível para os agentes etiológicos mais frequentes e extensível ao(s) parceiro(s) sexual(ais). As infecções mistas ocorrem com frequência; consequentemente, os custos com o tratamento em excesso são compensados pelos custos elevados que advirão ao se deixar de tratar pessoas com infecções mistas ou sem os sintomas específicos de uma determinada doença.
O diagnóstico sindrômico apresenta excelentes resultados especialmente nos casos de corrimento anal, uretral e úlcera anal e genital; nos corrimentos vaginais, a maioria dos estudos apresentou resultados apenas satisfatórios, porém, quando comparados com os resultados dos diagnósticos clínicos baseados na experiência pessoal do profissional, passaram a ter outra dimensão. Para esta última síndrome, alguns fluxogramas que sugerem a combinação de critérios de risco para cervicites e a utilização de algumas provas laboratoriais básicas apresentaram bons resultados
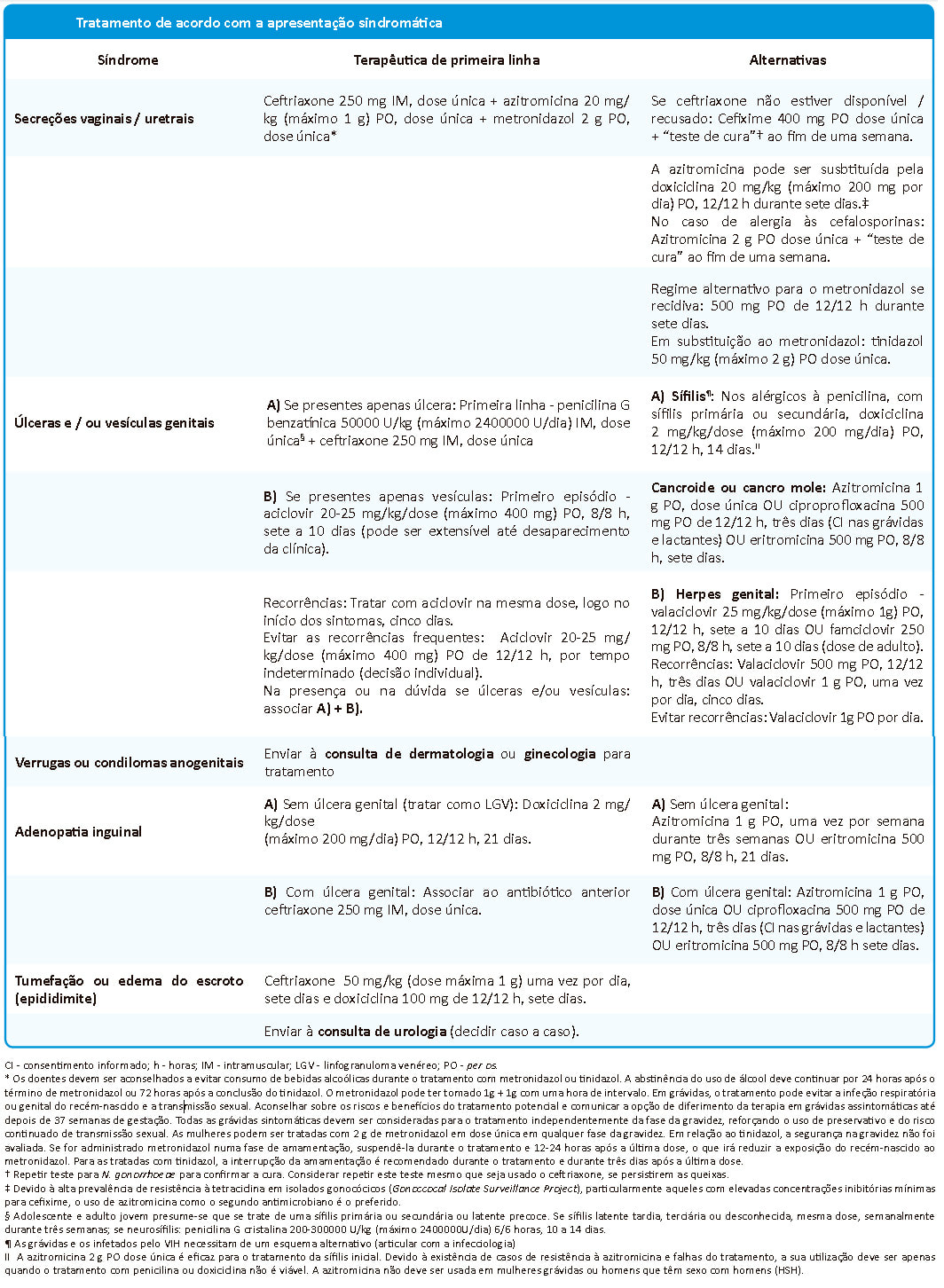
Tratamento de primeira para secreções anais / vaginais / uretrais
√ Ceftriaxone 250 mg IM, dose única + azitromicina 20 mg/kg (máximo 1 g) VO, dose única + metronidazol 2 g VO, dose única*
Tratamento alternativos para secreções anais / vaginais / uretrais
√ Se a ceftriaxone não estiver disponível / recusado: Cefixime 400 mg VO dose única + “teste de cura”† ao fim de uma semana.
√ A azitromicina pode ser substituída pela doxiciclina 20 mg/kg (máximo 200 mg por dia) VO, 12/12 h durante sete dias. ‡
√ No caso de alergia às cefalosporinas: Azitromicina 2 g VO dose única + “teste de cura”† ao fim de uma semana.
√ Regime alternativo para o metronidazol se recidiva: 500 mg VO de 12/12 h durante sete dias.
√ Em substituição ao metronidazol: tinidazol 50 mg/kg (máximo 2 g) VO dose única.
√ A azitromicina pode ser substituída pela doxiciclina 20 mg/kg (máximo 200 mg por dia) VO, 12/12 h durante sete dias. ‡
√ No caso de alergia às cefalosporinas: Azitromicina 2 g VO dose única + “teste de cura”† ao fim de uma semana.
√ Regime alternativo para o metronidazol se recidiva: 500 mg VO de 12/12 h durante sete dias.
√ Em substituição ao metronidazol: tinidazol 50 mg/kg (máximo 2 g) VO dose única.
Tratamento de primeira para úlceras e/ou vesículas anal ou genitais
A) Se presentes apenas úlcera: primeira linha - penicilina G benzatínica 50000 U/kg (máximo 2400000 U/dia) IM, dose única§ + ceftriaxone 250 mg IM, dose única.
B) Se presentes apenas vesículas: primeiro episódio - aciclovir 20-25 mg/kg/dose (máximo 400 mg) VO, 8/8 h, sete a 10 dias (pode ser extensível até o desaparecimento da clínica).
√ Na presença ou na dúvida se úlceras e/ou vesículas: associar A) + B).
Recorrências
√ Tratar com aciclovir na mesma dose, logo no início dos sintomas, cinco dias.
√ Para evitar as recorrências frequentes: aciclovir 20-25 mg/kg/dose (máximo 400 mg) VO de 12/12 h, por tempo
indeterminado (decisão individual).
√ Tratar com aciclovir na mesma dose, logo no início dos sintomas, cinco dias.
√ Para evitar as recorrências frequentes: aciclovir 20-25 mg/kg/dose (máximo 400 mg) VO de 12/12 h, por tempo
indeterminado (decisão individual).
Cancroide ou cancro mole: azitromicina 1 g VO, dose única OU ciproprofloxacina 500 mg VO de 12/12 h, três dias (CI nas grávidas e lactantes) OU eritromicina 500 mg VO, 8/8 h, sete dias.
Tratamento alternativo para úlceras e/ou vesículas anal ou genitais
A) Sífilis¶: nos alérgicos à penicilina, com sífilis primária ou secundária, doxiciclina 2 mg/kg/dose (máximo 200 mg/dia) VO, 12/12 h, 14 dias. II
B) Herpes genital: primeiro episódio - valaciclovir 25 mg/kg/dose (máximo 1g) VO, 12/12 h, sete a 10 dias OU famciclovir 250 mg PO, 8/8 h, sete a 10 dias (dose de adulto).
Recorrências
Valaciclovir 500 mg VO, 12/12 h, três dias OU valaciclovir 1 g VO, uma vez por dia, cinco dias.
Para evitar as recorrências frequentes: valaciclovir 1g VO por dia.
Valaciclovir 500 mg VO, 12/12 h, três dias OU valaciclovir 1 g VO, uma vez por dia, cinco dias.
Para evitar as recorrências frequentes: valaciclovir 1g VO por dia.
Verrugas ou condilomas anogenitais. VEJA DETALHES!
Adenopatia inguinal (íngua inguinal)
A) Sem úlcera genital (tratar como LGV): doxiciclina 2 mg/kg/dose (máximo 200 mg/dia) VO, 12/12 h, 21 dias.
A) Sem úlcera genital: azitromicina 1 g VO, uma vez por semana durante três semanas OU eritromicina 500 mg VO, 8/8 h, 21 dias.
B) Com úlcera genital: associar ao antibiótico anterior ceftriaxone 250 mg IM, dose única.
B) Com úlcera genital: azitromicina 1 g VO, dose única OU ciprofloxacina 500 mg VO de 12/12 h, três dias (CI nas grávidas e lactantes) OU eritromicina 500 mg VO, 8/8 h sete dias.
A) Sem úlcera genital: azitromicina 1 g VO, uma vez por semana durante três semanas OU eritromicina 500 mg VO, 8/8 h, 21 dias.
B) Com úlcera genital: associar ao antibiótico anterior ceftriaxone 250 mg IM, dose única.
B) Com úlcera genital: azitromicina 1 g VO, dose única OU ciprofloxacina 500 mg VO de 12/12 h, três dias (CI nas grávidas e lactantes) OU eritromicina 500 mg VO, 8/8 h sete dias.
Tumefação ou edema do escroto (epididimite)
Ceftriaxone 50 mg/kg (dose máxima 1 g) uma vez por dia, sete dias e doxiciclina 100 mg de 12/12 h, sete dias.
Enviar à consulta de urologia (decidir caso a caso).
Enviar à consulta de urologia (decidir caso a caso).
NOTA
CI - Consentimento informado; h - horas; IM - intramuscular; LGV - linfogranuloma venéreo; VO – via oral.
* Os doentes devem ser aconselhados a evitar consumo de bebidas alcoólicas durante o tratamento com metronidazol ou tinidazol. A abstinência do uso de álcool deve continuar por 24 horas após o término de metronidazol ou 72 horas após a conclusão do tinidazol. O metronidazol pode ter tomado 1g + 1g com uma hora de intervalo.
Em grávidas, o tratamento pode evitar a infecção respiratória ou genital do recém-nascido e a transmissão sexual. Aconselhar sobre os riscos e benefícios do tratamento potencial e comunicar a opção de diferimento da terapia em grávidas assintomáticas até depois de 37 semanas de gestação. Todas as grávidas sintomáticas devem ser consideradas para o tratamento independentemente da fase da gravidez, reforçando o uso de preservativo e do risco continuado de transmissão sexual. As mulheres podem ser tratadas com 2 g de metronidazol em dose única em qualquer fase da gravidez. Em relação ao tinidazol, a segurança na gravidez não foi avaliada.
Amamentação e metronidazol, suspendê-la durante o tratamento e 12-24 horas após a última dose, o que irá reduzir a exposição do recém-nascido ao metronidazol. Para as tratadas com tinidazol, a interrupção da amamentação é recomendada durante o tratamento e durante três dias após a última dose.
† Repetir teste para N. gonorrhoeae para confirmar a cura. Considerar repetir este teste mesmo que seja usado o ceftriaxone, se persistirem as queixas.
‡ Devido à alta prevalência de resistência à tetraciclina em isolados gonocócicos (Gonoccocal Isolate Surveillance Project), particularmente aqueles com elevadas concentrações inibitórias mínimas para cefixime, o uso de azitromicina como o segundo antimicrobiano é o preferido.
§ Adolescente e adultos jovens presume-se que se trate de uma sífilis primária ou secundária ou latente precoce. Se sífilis latente tardia, terciária ou desconhecida, mesma dose, semanalmente durante três semanas; se neurosífilis: penicilina G cristalina 200-300000 U/kg (máximo 2400000U/dia) 6/6 horas, 10 a 14 dias.
¶ As grávidas e os infetados pelo HIV necessitam de um esquema alternativo (articular com a infecciologia)
II A azitromicina 2 g VO dose única é eficaz para o tratamento da sífilis inicial. Devido à existência de casos de resistência à azitromicina e falhas do tratamento, a sua utilização deve ser apenas quando o tratamento com penicilina ou doxiciclina não é viável. A azitromicina não deve ser usada em mulheres grávidas ou homens que têm sexo com homens (HSH).
CI - Consentimento informado; h - horas; IM - intramuscular; LGV - linfogranuloma venéreo; VO – via oral.
* Os doentes devem ser aconselhados a evitar consumo de bebidas alcoólicas durante o tratamento com metronidazol ou tinidazol. A abstinência do uso de álcool deve continuar por 24 horas após o término de metronidazol ou 72 horas após a conclusão do tinidazol. O metronidazol pode ter tomado 1g + 1g com uma hora de intervalo.
Em grávidas, o tratamento pode evitar a infecção respiratória ou genital do recém-nascido e a transmissão sexual. Aconselhar sobre os riscos e benefícios do tratamento potencial e comunicar a opção de diferimento da terapia em grávidas assintomáticas até depois de 37 semanas de gestação. Todas as grávidas sintomáticas devem ser consideradas para o tratamento independentemente da fase da gravidez, reforçando o uso de preservativo e do risco continuado de transmissão sexual. As mulheres podem ser tratadas com 2 g de metronidazol em dose única em qualquer fase da gravidez. Em relação ao tinidazol, a segurança na gravidez não foi avaliada.
Amamentação e metronidazol, suspendê-la durante o tratamento e 12-24 horas após a última dose, o que irá reduzir a exposição do recém-nascido ao metronidazol. Para as tratadas com tinidazol, a interrupção da amamentação é recomendada durante o tratamento e durante três dias após a última dose.
† Repetir teste para N. gonorrhoeae para confirmar a cura. Considerar repetir este teste mesmo que seja usado o ceftriaxone, se persistirem as queixas.
‡ Devido à alta prevalência de resistência à tetraciclina em isolados gonocócicos (Gonoccocal Isolate Surveillance Project), particularmente aqueles com elevadas concentrações inibitórias mínimas para cefixime, o uso de azitromicina como o segundo antimicrobiano é o preferido.
§ Adolescente e adultos jovens presume-se que se trate de uma sífilis primária ou secundária ou latente precoce. Se sífilis latente tardia, terciária ou desconhecida, mesma dose, semanalmente durante três semanas; se neurosífilis: penicilina G cristalina 200-300000 U/kg (máximo 2400000U/dia) 6/6 horas, 10 a 14 dias.
¶ As grávidas e os infetados pelo HIV necessitam de um esquema alternativo (articular com a infecciologia)
II A azitromicina 2 g VO dose única é eficaz para o tratamento da sífilis inicial. Devido à existência de casos de resistência à azitromicina e falhas do tratamento, a sua utilização deve ser apenas quando o tratamento com penicilina ou doxiciclina não é viável. A azitromicina não deve ser usada em mulheres grávidas ou homens que têm sexo com homens (HSH).
Primeira consulta de acompanhamento em uma semana após o início da terapêutica.
1. Confirmar se o tratamento foi realizado corretamente.
2. Confirmar o diagnóstico caso tenha solicitado exames complementares.
3. Ajuste o tratamento de acordo com o teste de sensibilidade aos antibióticos (TSA) e resultados analíticos se necessário.
4. Evitar relações sexuais até que o tratamento termine tanto o paciente e quanto o parceiro(a).
5. No tratamento com azitromicina a relação sexual deve ser evitada por pelo menos sete dias.
6. Educação sexual: Informação e prevenção, afetos e sexualidade, ensino sobre a colocação do preservativo e, se possível, fornecer preservativos.
7. Repetir sorologias para HIV, sífilis (VDRL), hepatite B e C três meses depois.
2. Confirmar o diagnóstico caso tenha solicitado exames complementares.
3. Ajuste o tratamento de acordo com o teste de sensibilidade aos antibióticos (TSA) e resultados analíticos se necessário.
4. Evitar relações sexuais até que o tratamento termine tanto o paciente e quanto o parceiro(a).
5. No tratamento com azitromicina a relação sexual deve ser evitada por pelo menos sete dias.
6. Educação sexual: Informação e prevenção, afetos e sexualidade, ensino sobre a colocação do preservativo e, se possível, fornecer preservativos.
7. Repetir sorologias para HIV, sífilis (VDRL), hepatite B e C três meses depois.
√ Falha na adesão e cumprimento do tratamento prescrito.
√ Resistência aos antibióticos.
√ Múltiplos parceiros sexuais.
√ Falha no tratamento dos parceiros (principal causa de falha terapêutica).
√ IST “mistas” (coinfecção por dois ou mais agentes).
√ Outras comorbidades infecciosas.
√ Idades mais jovens.
√ Grupos de risco.
√ Resistência aos antibióticos.
√ Múltiplos parceiros sexuais.
√ Falha no tratamento dos parceiros (principal causa de falha terapêutica).
√ IST “mistas” (coinfecção por dois ou mais agentes).
√ Outras comorbidades infecciosas.
√ Idades mais jovens.
√ Grupos de risco.
Isenção de responsabilidade
As informações contidas neste artigo são apenas para fins educacionais e não devem ser usadas para diagnóstico ou para orientar o tratamento sem o parecer de um profissional de saúde. Qualquer leitor que está preocupado com sua saúde deve entrar em contato com um médico para aconselhamento.