Manejo dos tumores neuroendócrinos retais (carcinoide retal)
O objetivo desta revisão é realizar uma avaliação abrangente do manejo dos pacientes com tumores neuroendócrinos retais (TNERs), incluindo terapias endoscópica, transanal e cirúrgica. O manejo do TNER com metástases à distância e carcinomas neuroendócrinos pouco diferenciados não são abordados.
Tumores neuroendócrinos retais (TNER) (carcinoides retais) são tumores raros, mas a prevalência está aumentando constantemente devido ao aumento da expectativa de vida e aumento da incidência relacionada ao número crescente das colonoscopias de rastreamento.
A gestão dos TNER depende da presença ou ausência dos fatores preditivos de metástases em linfonodos, incluindo tamanho do tumor, aspecto endoscópico, estágio T (profundidade de invasão da parede), grau histológico e invasão linfovascular.
Tumores neuroendócrinos retais (TNER) (carcinoides retais) são tumores raros, mas a prevalência está aumentando constantemente devido ao aumento da expectativa de vida e aumento da incidência relacionada ao número crescente das colonoscopias de rastreamento.
A gestão dos TNER depende da presença ou ausência dos fatores preditivos de metástases em linfonodos, incluindo tamanho do tumor, aspecto endoscópico, estágio T (profundidade de invasão da parede), grau histológico e invasão linfovascular.
Epidemiologia dos tumores neuroendócrinos retais
Diagnóstico dos tumores neuroendócrinos retais
Diagnóstico patológico dos tumores neuroendócrinos retais
Prognóstico dos tumores neuroendócrinos retais
Gestão inicial e investigação diagnóstica dos tumores neuroendócrinos retais
Técnicas de ressecção endoscópica dos tumores neuroendócrinos retais
Síntese: indicações de técnicas de ressecção em pacientes com tumor neuroendócrino retal
Vigilância após ressecção dos tumores neuroendócrinos retais
Conclusões sobre o manejo endoscópico dos tumores neuroendócrinos retais
TNER é responsável por aproximadamente um terço de todas as neoplasias neuroendócrinas digestivas. O reto é o local primário mais comum de TNE digestivos, com uma incidência um pouco maior do que
TNE do intestino delgado (aproximadamente 1,2/100.000).
A incidência anual de TNER tem aumentado gradualmente nas últimas décadas, de 0,15/100.000 em 1985 para 1,2/100.000 em 2012. Este aumento na incidência pode ser devido ao aumento do número de colonoscopia de triagem realizadas, detecção endoscópica aprimorada, melhor consciência clínica e relatório mais sistemático nos registros.
Fatores de risco significativos de TNER são gênero masculino, história pessoal anterior de malignidade, consumo de álcool, diabetes e dislipidemia (baixo nível de colesterol de lipoproteína de alta densidade e hipertrigliceridemia.
Finalmente, TNER ocorre predominantemente durante a sexta década, provavelmente porque corresponde à idade em que os programas de colonoscopia de rastreamento predominam.
TNE do intestino delgado (aproximadamente 1,2/100.000).
A incidência anual de TNER tem aumentado gradualmente nas últimas décadas, de 0,15/100.000 em 1985 para 1,2/100.000 em 2012. Este aumento na incidência pode ser devido ao aumento do número de colonoscopia de triagem realizadas, detecção endoscópica aprimorada, melhor consciência clínica e relatório mais sistemático nos registros.
Fatores de risco significativos de TNER são gênero masculino, história pessoal anterior de malignidade, consumo de álcool, diabetes e dislipidemia (baixo nível de colesterol de lipoproteína de alta densidade e hipertrigliceridemia.
Finalmente, TNER ocorre predominantemente durante a sexta década, provavelmente porque corresponde à idade em que os programas de colonoscopia de rastreamento predominam.
TNER são predominantemente detectados fortuitamente na colonoscopia. Varia de 0,17% e 0,98% das colonoscopias realizadas. TNER são geralmente diagnosticados em um estágio inicial e localizado.
Metástases linfonodais (MLN) e metástases à distância são raramente encontradas no momento do diagnóstico, sendo responsáveis por 2% e 8% respectivamente. A taxa de pacientes com sintomas no diagnóstico é altamente variável entre as séries, mas varia de 10 a 15%. Os sintomas mais frequentemente presentes no diagnóstico inclui hematoquezia e alteração do hábito intestinal.
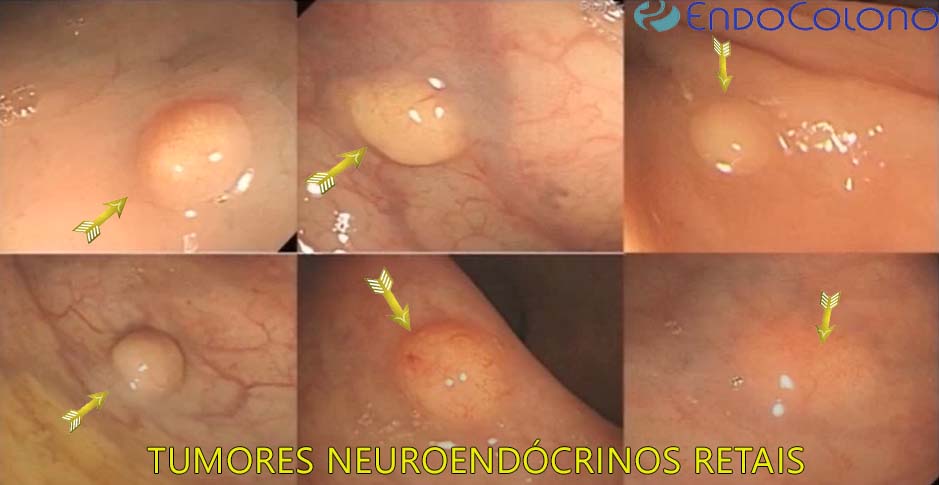
O aspecto endoscópico do TNER é geralmente como pequena lesão subepitelial no reto inferior ou médio. A maioria são polipoides (elevadas), arredondadas e com coloração amarelada (31% dos casos). Metade mede menos que 5 mm, enquanto as lesões medindo 11 e 19 mm ou > 20 mm representam aproximadamente 8% cada. Uma proporção limitada (<10%) de TNER pode apresentar depressão central ou úlcera.
Metástases linfonodais (MLN) e metástases à distância são raramente encontradas no momento do diagnóstico, sendo responsáveis por 2% e 8% respectivamente. A taxa de pacientes com sintomas no diagnóstico é altamente variável entre as séries, mas varia de 10 a 15%. Os sintomas mais frequentemente presentes no diagnóstico inclui hematoquezia e alteração do hábito intestinal.
O aspecto endoscópico do TNER é geralmente como pequena lesão subepitelial no reto inferior ou médio. A maioria são polipoides (elevadas), arredondadas e com coloração amarelada (31% dos casos). Metade mede menos que 5 mm, enquanto as lesões medindo 11 e 19 mm ou > 20 mm representam aproximadamente 8% cada. Uma proporção limitada (<10%) de TNER pode apresentar depressão central ou úlcera.
Todas as amostras patológicas devem ser examinadas por um patologista especialista. Sinaptofisina é positiva em quase 100% dos casos, enquanto a coloração com cromogranina A é positiva apenas em 28% e 58% dos casos, porque TNER com mais frequência expressa cromogranina B. Em caso de problemas de diagnóstico, a imunocoloração de CD56 pode ser útil.
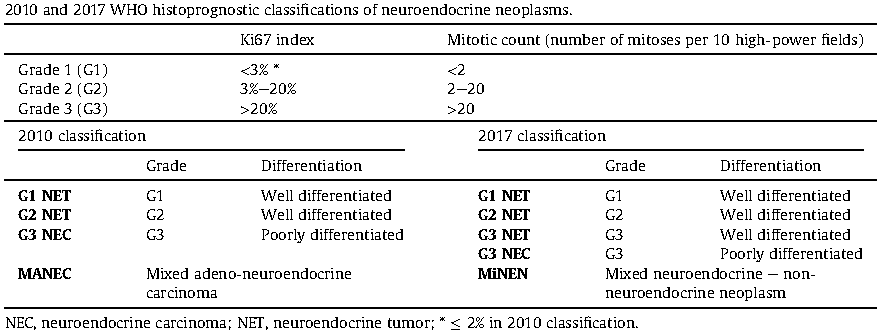
O grau histo-prognóstico é essencial para a caracterização prognóstica e decisão terapêutica. A classificação da OMS de 2017 subdividiu a categoria de alto grau (G3) em TNE bem diferenciada e mal diferenciada.
O grau histo-prognóstico é essencial para a caracterização prognóstica e decisão terapêutica. A classificação da OMS de 2017 subdividiu a categoria de alto grau (G3) em TNE bem diferenciada e mal diferenciada.
Numerosos estudos exploraram os fatores de risco para disseminação metastática. O prognóstico do TNER depende do estágio da doença. Em tumores aparentemente localizados, os principais fatores associados é a invasão da camada muscular (estágio T2) ou além, o tamanho do tumor, depressão ou ulceração da lesão, grau histoprognóstico e invasão linfovascular (ILV). Globalmente, todos os casos de TNER com linfonodos positivos têm pelo menos um fator de risco.
Estágio do tumor neuroendócrino retal
O estágio do tumor é o principal fator prognóstico dos TNEs retais. TNER deve ser classificado de acordo
a 8ª edição da classificação TNM, que se aplica apenas a TNER bem diferenciado. O carcinoma pouco diferenciado deve ser classificado como o adenocarcinoma retal.
A taxa de sobrevida específica da doença em 5 anos é de 99,3%, 96,7% e 44,1%, para pacientes com TNERs local, com comprometimento de linfonodo regional e com metástase a distância, respectivamente.
A maioria dos TNERs são limitados à submucosa, embora 8% e 19% deles possam invadir a muscular própria (T2). O estágio T2 está associado a um aumento independente do risco de metástase linfonodal.
Classificação UICC Tumor-Node-Metastases de TNER, 8ª edição.
TX - O status do tumor primário não pode ser avaliado
T0 - Sem evidência de tumor primário
T1a - Invade a lâmina própria ou submucosa e tamanho <1 cm
T1b - Invade a lâmina própria ou submucosa e tamanho 1 e 2 cm
T2 - Invade a lâmina própria ou submucosa e tamanho >2 cm ou invade muscular própria
T3 - Invade o tecido subseroso sem invadir a serosa
T4 - Invade o peritônio ou outros órgãos
NX - Status do linfonodo regional não avaliável
N0 - Sem metástase de linfonodo regional
N1 - Metástases de linfonodos regionais
Mx - Status metastático não avaliável
M0 - Sem metástase distante
M1 - Metástases distantes
M1a - Metástase hepática apenas
M1b - Metástase extra-hepática apenas
M1c - Metástases hepáticas e extra-hepáticas
Tamanho do tumor neuroendócrino retal
Entre 70% e 85% do TNERs tem um tamanho <10 mm quando diagnosticados. O risco de metástases é muito baixo (<3%) em TNER <10 mm e muito alto (30% e 80%) em >20 mm de tamanho. Entre esses dois extremos, 4% e 20% dos pacientes com TNER medindo entre 10 e 19 mm têm metástases sincrônicas ou metacrônicas.
Características endoscópicas atípicas do tumor neuroendócrino retal
Características endoscópicas atípicas (hiperemia, erosões, depressão e ulcerações) são relatadas em 6% a 22% de TNERs. Embora os dados da literatura sejam controversos, tais atipias são mais frequentes nos tumores maiores quando o risco de metástases linfonodais é aumentado.
Grau de histológico e prognóstico do tumor neuroendócrino retal
A grande maioria dos TNER são G1. Entre 2% e 13% dos TNER são classificados como G2 ou G3 quando existe um risco significativamente aumentado de metástases em comparação com G1 TNER.
São descritas taxas de MLN de 6% e 75% no G1 e G2 TNER, respectivamente.
Estágio do tumor neuroendócrino retal
O estágio do tumor é o principal fator prognóstico dos TNEs retais. TNER deve ser classificado de acordo
a 8ª edição da classificação TNM, que se aplica apenas a TNER bem diferenciado. O carcinoma pouco diferenciado deve ser classificado como o adenocarcinoma retal.
A taxa de sobrevida específica da doença em 5 anos é de 99,3%, 96,7% e 44,1%, para pacientes com TNERs local, com comprometimento de linfonodo regional e com metástase a distância, respectivamente.
A maioria dos TNERs são limitados à submucosa, embora 8% e 19% deles possam invadir a muscular própria (T2). O estágio T2 está associado a um aumento independente do risco de metástase linfonodal.
Classificação UICC Tumor-Node-Metastases de TNER, 8ª edição.
TX - O status do tumor primário não pode ser avaliado
T0 - Sem evidência de tumor primário
T1a - Invade a lâmina própria ou submucosa e tamanho <1 cm
T1b - Invade a lâmina própria ou submucosa e tamanho 1 e 2 cm
T2 - Invade a lâmina própria ou submucosa e tamanho >2 cm ou invade muscular própria
T3 - Invade o tecido subseroso sem invadir a serosa
T4 - Invade o peritônio ou outros órgãos
NX - Status do linfonodo regional não avaliável
N0 - Sem metástase de linfonodo regional
N1 - Metástases de linfonodos regionais
Mx - Status metastático não avaliável
M0 - Sem metástase distante
M1 - Metástases distantes
M1a - Metástase hepática apenas
M1b - Metástase extra-hepática apenas
M1c - Metástases hepáticas e extra-hepáticas
Tamanho do tumor neuroendócrino retal
Entre 70% e 85% do TNERs tem um tamanho <10 mm quando diagnosticados. O risco de metástases é muito baixo (<3%) em TNER <10 mm e muito alto (30% e 80%) em >20 mm de tamanho. Entre esses dois extremos, 4% e 20% dos pacientes com TNER medindo entre 10 e 19 mm têm metástases sincrônicas ou metacrônicas.
Características endoscópicas atípicas do tumor neuroendócrino retal
Características endoscópicas atípicas (hiperemia, erosões, depressão e ulcerações) são relatadas em 6% a 22% de TNERs. Embora os dados da literatura sejam controversos, tais atipias são mais frequentes nos tumores maiores quando o risco de metástases linfonodais é aumentado.
Grau de histológico e prognóstico do tumor neuroendócrino retal
A grande maioria dos TNER são G1. Entre 2% e 13% dos TNER são classificados como G2 ou G3 quando existe um risco significativamente aumentado de metástases em comparação com G1 TNER.
São descritas taxas de MLN de 6% e 75% no G1 e G2 TNER, respectivamente.
Invasão linfovascular do tumor neuroendócrino retal
Invasão linfovascular (ILV) tem sido frequentemente, mas inconstantemente, relatado como um fator de prognóstico em TNER, porque sua avaliação sofre variações interobservador e porque existem duas metodologias. ILV está correlacionada com o tamanho do tumor em vários estudos, mas a especificidade pode não ser ideal para prever a existência de metástase linfonodal.
Status das margens de ressecção do tumor neuroendócrino retal
As margens de ressecção de TNEs retais após a ressecção endoscópica às vezes são positivas nos exames de anatomopatológico. No entanto, a positividade da margem de ressecção não é totalmente preditiva de tumor residual nem recidiva, uma vez que a destruição das células tumorais vizinhas pela cauterização durante a ressecção endoscópica pode esterilizar o local da ressecção.
De fato, em quatro séries analisadas juntas, quando foi realizada ressecções de toda a espessura da parede retal pela microcirurgia endoscópica transanal (TEM) ou cirurgia radical após ressecção endoscópica incompleta, tumor residual foi detectado em apenas 26 dos 104 pacientes (25%).
Sendo assim, um estado R1 determinado patologicamente (margens positivas) pode resultar em desnecessário (e potencialmente mórbido) sobretratamento cirúrgico. No entanto, a ressecção R1 não pode ser considerada como curativa e terapia complementar deve ser discutida. A estratégia mais preconizada consiste em realizar biópsias na área da ressecção antes de considerar um tratamento de resgate adicional.
Invasão linfovascular (ILV) tem sido frequentemente, mas inconstantemente, relatado como um fator de prognóstico em TNER, porque sua avaliação sofre variações interobservador e porque existem duas metodologias. ILV está correlacionada com o tamanho do tumor em vários estudos, mas a especificidade pode não ser ideal para prever a existência de metástase linfonodal.
Status das margens de ressecção do tumor neuroendócrino retal
As margens de ressecção de TNEs retais após a ressecção endoscópica às vezes são positivas nos exames de anatomopatológico. No entanto, a positividade da margem de ressecção não é totalmente preditiva de tumor residual nem recidiva, uma vez que a destruição das células tumorais vizinhas pela cauterização durante a ressecção endoscópica pode esterilizar o local da ressecção.
De fato, em quatro séries analisadas juntas, quando foi realizada ressecções de toda a espessura da parede retal pela microcirurgia endoscópica transanal (TEM) ou cirurgia radical após ressecção endoscópica incompleta, tumor residual foi detectado em apenas 26 dos 104 pacientes (25%).
Sendo assim, um estado R1 determinado patologicamente (margens positivas) pode resultar em desnecessário (e potencialmente mórbido) sobretratamento cirúrgico. No entanto, a ressecção R1 não pode ser considerada como curativa e terapia complementar deve ser discutida. A estratégia mais preconizada consiste em realizar biópsias na área da ressecção antes de considerar um tratamento de resgate adicional.
A primeira etapa do manejo do TNE retal é o seu reconhecimento pelo endoscopista durante a colonoscopia.
O TNE retal pode ser diagnosticado apenas no anatomopatológico após a ressecção endoscópica de um pólipo retal duvidoso por polipectomia convencional ou mucosectomia que pode não atingir margens de ressecção suficientes. Os fatores preditivos de metástase linfonodal e recorrência local devem ser avaliados para decidir se um tratamento adicional de resgate deve ser realizado e qual é o mais apropriado.
Uma lesão ou pólipo retal com suspeita endoscópica de TNE pode ser biopsiada (idealmente, realizar biópsias superficiais) e fotografada quando maiores que 2 cm e/ou com superfície irregular ou apenas documentada sugerindo exames de imagem para melhor definição. Em ambos os casos um exame adequado de imagem deve ser realizado para avaliar o risco de metástases e grau de invasão da parede retal para que o tratamento mais adequado seja determinado.
O reconhecimento ou suspeita de TNER durante a colonoscopia é, portanto, de grande importância, pois permite evitar algumas ressecções inadequadas e fazer um plano para a ressecção endoscópica adequada no primeiro procedimento, aumentando as chances de ressecção curativa.
EUS endorretal dos tumores neuroendócrinos retais
A ultrassonografia endoscópica endorretal (USE) tem alto desempenho diagnóstico para TNER, incluindo valores preditivos positivos e negativos e precisão diagnóstica de 81%, 92% e 85%, respectivamente.
No USE, o TNER geralmente tem um aspecto redondo (51%) ou nodular (32%). Seu padrão de ecogenicidade pode ser hipoecoico (19%) ou intermediário (78%) e costuma ser homogêneo. A precisão do USE para a determinar a profundidade de invasão, principalmente da muscular própria, é superior a 90%. Finalmente, USE deve avaliar os linfonodos regionais, a fim de identificar sinais de possível malignidade, embora a penetração do ultrassom seja muito limitada para examinar todo o espaço perirretal.
Portanto, USE deve ser parte da investigação inicial de todos os TNEs retais, com exceção daqueles <5 mm que geralmente são ressecados na totalidade pela colonoscopia e não existe risco de metástase em linfonodo.
Finalmente, a colonoscopia completa é obrigatória para todos os pacientes com TNER para excluir câncer de cólon concomitante e outra NEN colorretal, que pode ocorrer em até 8% dos casos.
Imagem transversal pélvica (ressonância magnética e tomografia computadorizada)
Os objetivos da ressonância magnética da pelve (MRI) são avaliar o estágio T, a extensão perirretal e
envolvimento de linfonodos regionais. No entanto, os critérios de suspeita de linfonodo mesorretal são
mal definidos.
No geral, a ressonância magnética é clinicamente relevante para avaliação da infiltração da parede, especialmente em caso de TNER> T1 (muscular própria) e suspeitar de MLN no caso de linfonodos aumentados (>3 mm). Portanto, é recomendável realizar a ressonância magnética pélvica ou tomografia computadorizada como parte da investigação inicial de todo TNER >10 mm. No entanto, na ausência de linfonodos aumentados (>3 mm), a MLN não pode ser descartada e, portanto, a tomada de decisão terapêutica deve levar em consideração os outros fatores preditivos de MLN.
Avaliação à distância: imagens morfológicas e isotópicas convencionais
Explorações adicionais são justificadas para todos os TNER >20 mm de tamanho, no caso de MLN ou fatores de alto risco de MLN. Deve incluir TC torácico-abdominal-pélvica com contraste, ressonância magnética do fígado e PET-CT (imagem isotópica do receptor de somatostatina (tomografia com emissão de pósitrons).
Devido ao seu aspecto tipicamente hipervascular, as metástases associadas a TNER geralmente aumentam após injeção de contraste na fase arterial, com eliminação na fase portal. Ressonância magnética especialmente com sequências de difusão ponderada tem melhor sensibilidade do que tomografia computadorizada e PET-CT com receptor de somatostatina para a detecção de lesões à distância, especialmente metástases hepáticas.
A maioria dos TNER apresentam receptores de somatostatina e, portanto, são identificados pela cintilografia do receptor de somatostatina (Octreoscan®) ou tomografia de emissão de pósitrons de gálio 68. Este último deve ser preferido por ter maior afinidade e resolução espacial, requer menor tempo e expõe o paciente a menos radiação. A imagem do receptor da somatostatina permite identificar metástases à distância com excelente sensibilidade.
O TNE retal pode ser diagnosticado apenas no anatomopatológico após a ressecção endoscópica de um pólipo retal duvidoso por polipectomia convencional ou mucosectomia que pode não atingir margens de ressecção suficientes. Os fatores preditivos de metástase linfonodal e recorrência local devem ser avaliados para decidir se um tratamento adicional de resgate deve ser realizado e qual é o mais apropriado.
Uma lesão ou pólipo retal com suspeita endoscópica de TNE pode ser biopsiada (idealmente, realizar biópsias superficiais) e fotografada quando maiores que 2 cm e/ou com superfície irregular ou apenas documentada sugerindo exames de imagem para melhor definição. Em ambos os casos um exame adequado de imagem deve ser realizado para avaliar o risco de metástases e grau de invasão da parede retal para que o tratamento mais adequado seja determinado.
O reconhecimento ou suspeita de TNER durante a colonoscopia é, portanto, de grande importância, pois permite evitar algumas ressecções inadequadas e fazer um plano para a ressecção endoscópica adequada no primeiro procedimento, aumentando as chances de ressecção curativa.
EUS endorretal dos tumores neuroendócrinos retais
A ultrassonografia endoscópica endorretal (USE) tem alto desempenho diagnóstico para TNER, incluindo valores preditivos positivos e negativos e precisão diagnóstica de 81%, 92% e 85%, respectivamente.
No USE, o TNER geralmente tem um aspecto redondo (51%) ou nodular (32%). Seu padrão de ecogenicidade pode ser hipoecoico (19%) ou intermediário (78%) e costuma ser homogêneo. A precisão do USE para a determinar a profundidade de invasão, principalmente da muscular própria, é superior a 90%. Finalmente, USE deve avaliar os linfonodos regionais, a fim de identificar sinais de possível malignidade, embora a penetração do ultrassom seja muito limitada para examinar todo o espaço perirretal.
Portanto, USE deve ser parte da investigação inicial de todos os TNEs retais, com exceção daqueles <5 mm que geralmente são ressecados na totalidade pela colonoscopia e não existe risco de metástase em linfonodo.
Finalmente, a colonoscopia completa é obrigatória para todos os pacientes com TNER para excluir câncer de cólon concomitante e outra NEN colorretal, que pode ocorrer em até 8% dos casos.
Imagem transversal pélvica (ressonância magnética e tomografia computadorizada)
Os objetivos da ressonância magnética da pelve (MRI) são avaliar o estágio T, a extensão perirretal e
envolvimento de linfonodos regionais. No entanto, os critérios de suspeita de linfonodo mesorretal são
mal definidos.
No geral, a ressonância magnética é clinicamente relevante para avaliação da infiltração da parede, especialmente em caso de TNER> T1 (muscular própria) e suspeitar de MLN no caso de linfonodos aumentados (>3 mm). Portanto, é recomendável realizar a ressonância magnética pélvica ou tomografia computadorizada como parte da investigação inicial de todo TNER >10 mm. No entanto, na ausência de linfonodos aumentados (>3 mm), a MLN não pode ser descartada e, portanto, a tomada de decisão terapêutica deve levar em consideração os outros fatores preditivos de MLN.
Avaliação à distância: imagens morfológicas e isotópicas convencionais
Explorações adicionais são justificadas para todos os TNER >20 mm de tamanho, no caso de MLN ou fatores de alto risco de MLN. Deve incluir TC torácico-abdominal-pélvica com contraste, ressonância magnética do fígado e PET-CT (imagem isotópica do receptor de somatostatina (tomografia com emissão de pósitrons).
Devido ao seu aspecto tipicamente hipervascular, as metástases associadas a TNER geralmente aumentam após injeção de contraste na fase arterial, com eliminação na fase portal. Ressonância magnética especialmente com sequências de difusão ponderada tem melhor sensibilidade do que tomografia computadorizada e PET-CT com receptor de somatostatina para a detecção de lesões à distância, especialmente metástases hepáticas.
A maioria dos TNER apresentam receptores de somatostatina e, portanto, são identificados pela cintilografia do receptor de somatostatina (Octreoscan®) ou tomografia de emissão de pósitrons de gálio 68. Este último deve ser preferido por ter maior afinidade e resolução espacial, requer menor tempo e expõe o paciente a menos radiação. A imagem do receptor da somatostatina permite identificar metástases à distância com excelente sensibilidade.
Polipectomia e mucosectomia padrão do tumor neuroendócrino retal
Polipectomia e mucosectomia (ressecção endoscópica da mucosa [EMR]) consistem na ressecção com alça do TNER, realizada sem ou com injeção inicial de solução salina na submucosa (que visa reduzir os riscos de perfuração e margens de ressecção verticais incompletas), respectivamente. Deve-se evitar as ressecções em fragmento por limitar a qualidade do exame patológico e aumenta o risco de ressecção incompleta. Essas técnicas de ressecção padrão apresentam taxa de R0 de 59% em TNER >10 mm.
Técnica de ressecção endoscópica da mucosa (EMR) / mucosectomia do tumor neuroendócrino retal
Polipectomia e mucosectomia (ressecção endoscópica da mucosa [EMR]) consistem na ressecção com alça do TNER, realizada sem ou com injeção inicial de solução salina na submucosa (que visa reduzir os riscos de perfuração e margens de ressecção verticais incompletas), respectivamente. Deve-se evitar as ressecções em fragmento por limitar a qualidade do exame patológico e aumenta o risco de ressecção incompleta. Essas técnicas de ressecção padrão apresentam taxa de R0 de 59% em TNER >10 mm.
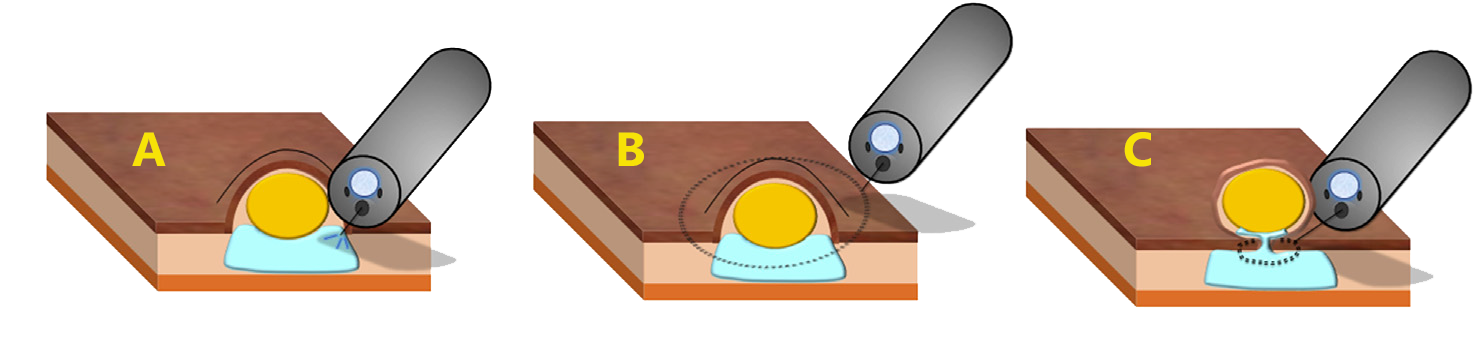
Técnica de ressecção endoscópica da mucosa (EMR) / mucosectomia do tumor neuroendócrino retal
A- Injeção na submucosa de solução salina. B, posição da alça ao redor da lesão. C- Fechamento da alça na base da lesão e ressecção da lesão com corrente mista (blend 1) do eletrocautério.
A área de polipectomia ou da mucosectomia deve ser marcada após a ressecção para facilitar a localização futura e terapia de resgate no caso de as margens serem positivas. Se a marcação não foi realizada durante a polipectomia e as margens estiverem invadidas, deve-se fazer com urgência nova retoscopia para marcar o local antes da tentativa de ressecção de resgate curativa.
A área de polipectomia ou da mucosectomia deve ser marcada após a ressecção para facilitar a localização futura e terapia de resgate no caso de as margens serem positivas. Se a marcação não foi realizada durante a polipectomia e as margens estiverem invadidas, deve-se fazer com urgência nova retoscopia para marcar o local antes da tentativa de ressecção de resgate curativa.
Técnicas avançadas de ressecção endoscópica do tumor neuroendócrino retal
A ressecção endoscópica da submucosa assistida por ligadura (EMR-L) é descrita a fim de melhorar a eficácia da remoção endoscópica.
Técnica de ressecção endoscópica da submucosa assistida por ligadura elástica (EMR-L)
A ressecção endoscópica da submucosa assistida por ligadura (EMR-L) é descrita a fim de melhorar a eficácia da remoção endoscópica.
Técnica de ressecção endoscópica da submucosa assistida por ligadura elástica (EMR-L)
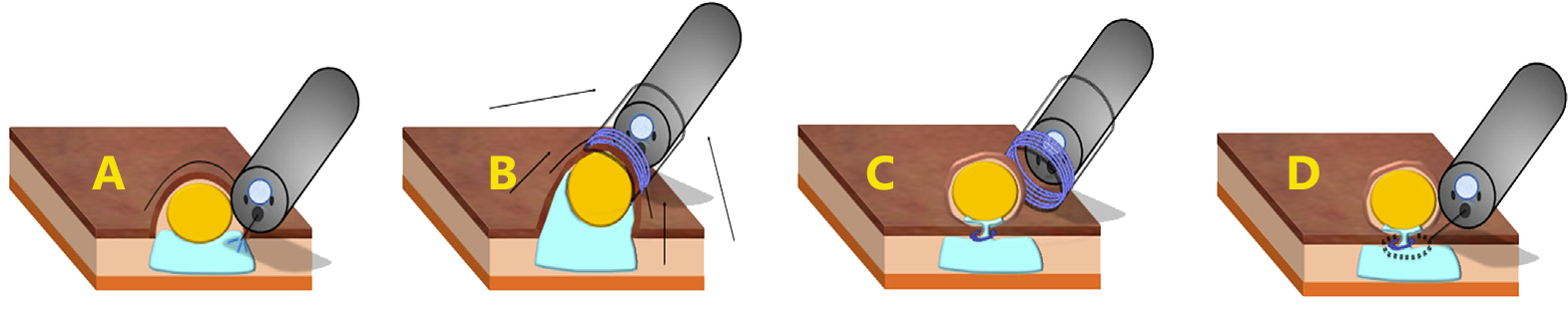
A- Injeção na submucosa de solução salina. B- Posição do sistema de ligadura elástica na parte superior do endoscópio (semelhante ao usado para a ligadura de varizes esofágicas) e aspiração da lesão para o seu interior. C- Implantação da banda elástica abaixo da lesão. D- Ressecção com alça da lesão com corrente mista (blend 1) do eletrocautério.
Técnica de dissecção endoscópica da submucosa (ESD)
Mais recentemente, o uso de dissecção endoscópica da submucosa (ESD) tem sido cada vez mais relatado para TNER, mas apresenta um risco maior de perfuração e sangramento retal do que outras técnicas. Curiosamente, as taxas de ressecção incompleta e complicações são relatadas em 71% e 78%, respectivamente, ao longo de um período de 5 anos. Portanto, ESD requer habilidade específica, experiência, maior tempo operatório e só deve ser realizado em centros especializados.
Mais recentemente, o uso de dissecção endoscópica da submucosa (ESD) tem sido cada vez mais relatado para TNER, mas apresenta um risco maior de perfuração e sangramento retal do que outras técnicas. Curiosamente, as taxas de ressecção incompleta e complicações são relatadas em 71% e 78%, respectivamente, ao longo de um período de 5 anos. Portanto, ESD requer habilidade específica, experiência, maior tempo operatório e só deve ser realizado em centros especializados.
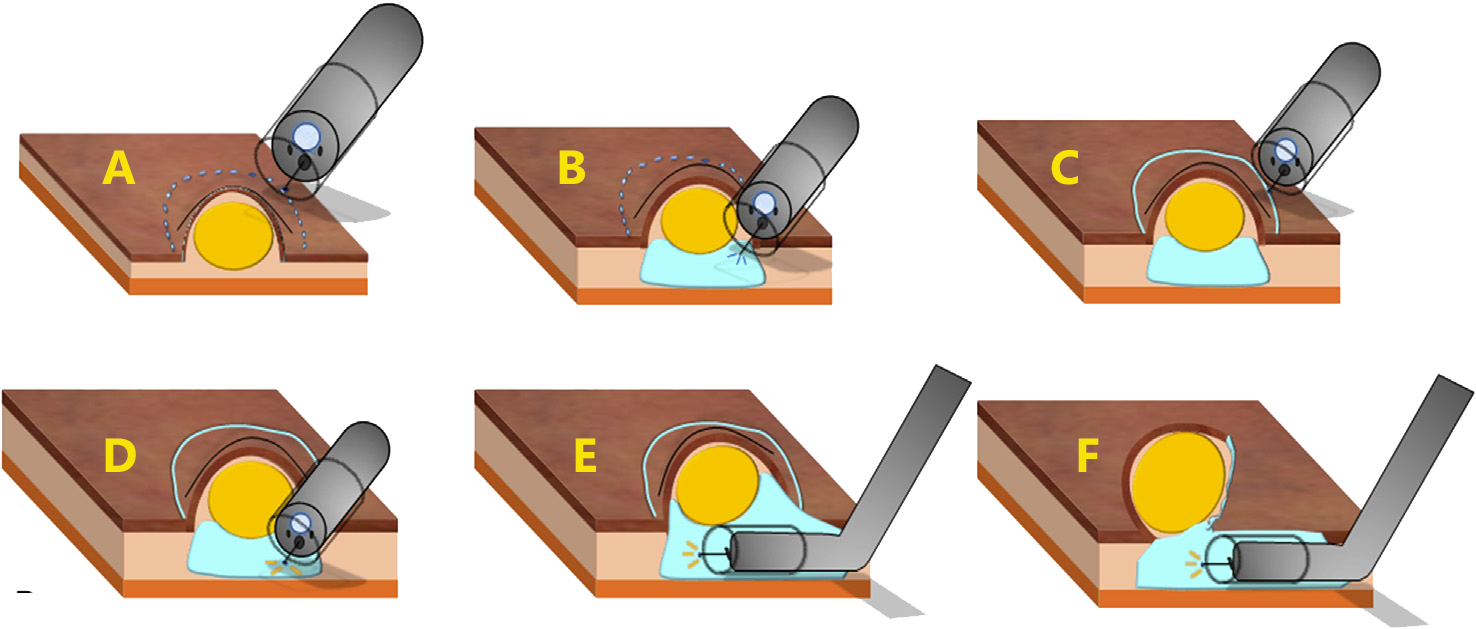
A- Delimitação da circunferência externa mínima da zona de excisão ao redor da lesão por meio da marcação de pontos de eletrocauterização. B- Injeção submucosa de solução salina. C- Incisão circunferencial em torno da superfície delimitada pelos pontos. DEF- Dissecção abaixo da lesão, ao longo do plano submucoso sob visualização direta.
Comparação das técnicas de ressecção endoscópica do tumor neuroendócrino retal
As comparações entre as técnicas de ressecção endoscópica são limitadas, porque os estudos são poucos, heterógenos, quase todos retrospectivos e com acompanhamento limitado.
Em uma metanálise anterior de 25 estudos incluindo 1.094 pacientes, relataram que a EMR-L e ESD foram as técnicas mais eficazes, com respectivas taxas R0 médias de 94,8% e 89,6% (vs. 59,1% e 72,4% para polipectomia e EMR, respectivamente) e taxas de recorrência muito baixas, mas com acompanhamento limitado (<5 anos).
Da mesma forma, outra metanálise de 14 estudos comparativos (782 pacientes), relataram que a EMR-L e ESD alcançaram ressecção completa significativamente maior do que EMR simples, mas sem diferença entre elas.
Sobre TNER <10 mm, estudos mais recentes relataram eficácia semelhante de ESD e EMR-L., No entanto, uma metanálise que reagrupou 7 estudos (386 pacientes) relatou que EMR-L alcançou maior taxa de R0 do que ESD (96,1% vs. 83%) para TNER <10 mm. Além disso, ESD demorou significativamente mais tempo operatório e tendeu a causar mais complicações (p ¼ 0,11).
Portanto, EMR-L parece ser a técnica mais apropriada de ressecção endoscópica de TNER <10 mm.
Os dados são mais limitados em relação aos TNER >10 mm. EMR-L requer aspiração para o interior do aplicador de elástico, o que pode ser mais difícil neste cenário. Por outro lado, a taxa R0 da ESD mostrou não ser diferente nos TNER >10 mm quando comparados aos TNER >10mm.
A Técnica ESD parece ser a técnica mais adequada para ressecção endoscópica de TNER >10 mm.
Terapia endoscópica de resgate após polipectomia incompleta do tumor neuroendócrino retal
A ressecção endoscópica induz fibrose com endurecimento do tecido subjacente, o que pode fazer futura EMR de resgate mais difícil e menos bem sucedido. O EMR-C adjuvante atingiu 100% de margens de ressecção livres em várias séries reagrupando 43 pequenos TNER ressecados incompletamente por polipectomia e EMR.
As comparações entre as técnicas de ressecção endoscópica são limitadas, porque os estudos são poucos, heterógenos, quase todos retrospectivos e com acompanhamento limitado.
Em uma metanálise anterior de 25 estudos incluindo 1.094 pacientes, relataram que a EMR-L e ESD foram as técnicas mais eficazes, com respectivas taxas R0 médias de 94,8% e 89,6% (vs. 59,1% e 72,4% para polipectomia e EMR, respectivamente) e taxas de recorrência muito baixas, mas com acompanhamento limitado (<5 anos).
Da mesma forma, outra metanálise de 14 estudos comparativos (782 pacientes), relataram que a EMR-L e ESD alcançaram ressecção completa significativamente maior do que EMR simples, mas sem diferença entre elas.
Sobre TNER <10 mm, estudos mais recentes relataram eficácia semelhante de ESD e EMR-L., No entanto, uma metanálise que reagrupou 7 estudos (386 pacientes) relatou que EMR-L alcançou maior taxa de R0 do que ESD (96,1% vs. 83%) para TNER <10 mm. Além disso, ESD demorou significativamente mais tempo operatório e tendeu a causar mais complicações (p ¼ 0,11).
Portanto, EMR-L parece ser a técnica mais apropriada de ressecção endoscópica de TNER <10 mm.
Os dados são mais limitados em relação aos TNER >10 mm. EMR-L requer aspiração para o interior do aplicador de elástico, o que pode ser mais difícil neste cenário. Por outro lado, a taxa R0 da ESD mostrou não ser diferente nos TNER >10 mm quando comparados aos TNER >10mm.
A Técnica ESD parece ser a técnica mais adequada para ressecção endoscópica de TNER >10 mm.
Terapia endoscópica de resgate após polipectomia incompleta do tumor neuroendócrino retal
A ressecção endoscópica induz fibrose com endurecimento do tecido subjacente, o que pode fazer futura EMR de resgate mais difícil e menos bem sucedido. O EMR-C adjuvante atingiu 100% de margens de ressecção livres em várias séries reagrupando 43 pequenos TNER ressecados incompletamente por polipectomia e EMR.
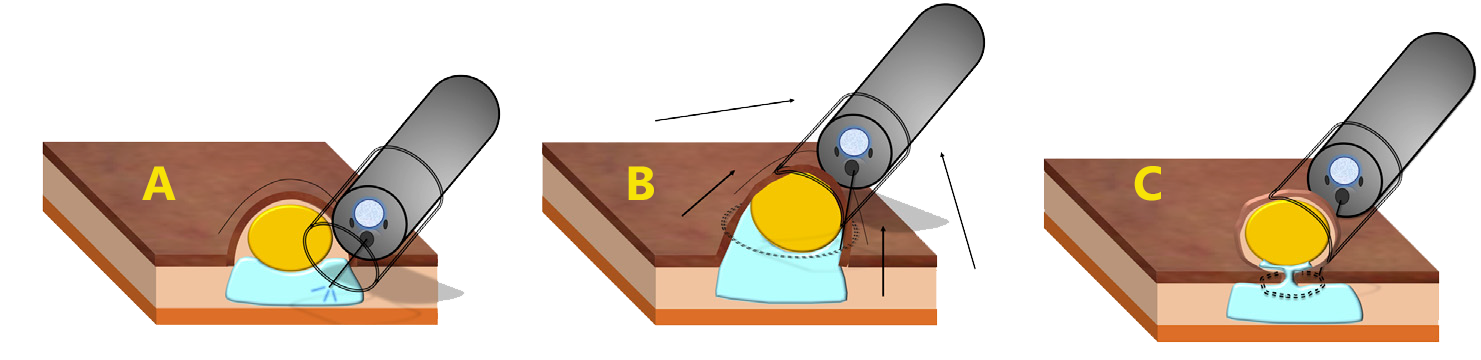
A- Cap é colocado cap na ponta do endoscópio e injeção na submucosa de solução salina. B- Inserção de uma alça assimétrica no interior do cap pelo canal de aspiração do aparelho seguido de seu posicionamento ao redor da lesão que é aspirada para seu interior. C- Fechamento da alça assimétrica na base da lesão e ressecção com corrente mista (blend 1) do eletrocautério.
ESD foi avaliado de forma menos abrangente nesta indicação, parece viável, embora as taxas de ressecção completa são de aproximadamente 80%. Digno de nota, é que as terapias endoscópicas de resgate aumentam o risco de sangramento, que pode ocorrer em até 23% dos pacientes.
No geral, EMR-C e ESD são viáveis para tratamento adjuvante após ressecção endoscópica primária incompleta, especialmente para TNER <10 mm. No entanto, estudos confirmatórios são necessários para confirmar as eficácias. Além do mais, a ESD não foi adequadamente comparada à microcirurgia endoscópica transanal (TEM) no contexto da terapia de resgate. Este último poderia alcançar melhores resultados, especialmente para TNER >10 mm.
No geral, EMR-C e ESD são viáveis para tratamento adjuvante após ressecção endoscópica primária incompleta, especialmente para TNER <10 mm. No entanto, estudos confirmatórios são necessários para confirmar as eficácias. Além do mais, a ESD não foi adequadamente comparada à microcirurgia endoscópica transanal (TEM) no contexto da terapia de resgate. Este último poderia alcançar melhores resultados, especialmente para TNER >10 mm.
Microcirurgia endoscópica transanal (TEM)
|
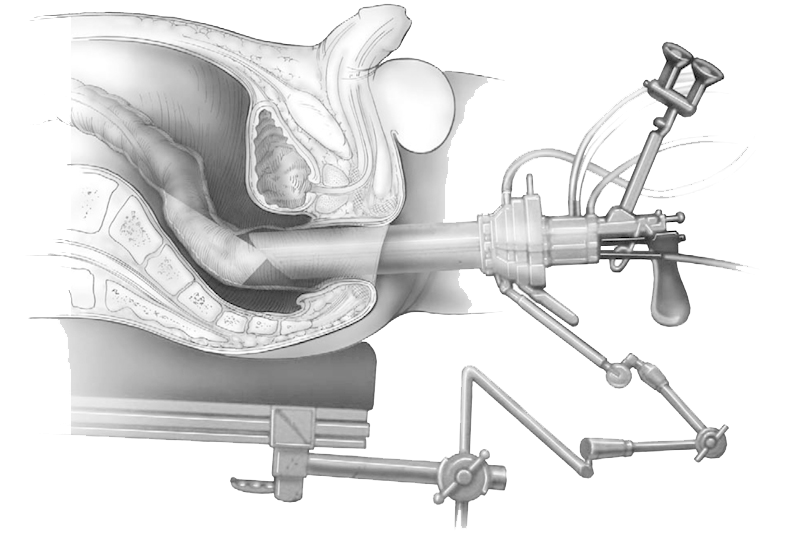
Princípios do TE. TEM é uma técnica cirúrgica minimamente invasiva que requer equipamento específico, consistindo em um porta multicanal descartável posicionada transanalmente, controlando continuamente a pressão endoluminal retal e permitindo o uso combinado de um retoscópio rígido com visão tridimensional ampliada e uso instrumentos endocirúrgicos.
|
Após a marcação da área de ressecção programada por eletropontos de cautério, a ressecção RNET geralmente consiste em uma ressecção de espessura total, até a gordura externa tecido. O tempo médio de operação relatado na literatura varia de 45 a 80 min. O defeito retal é geralmente fechado por uma sutura contínua, pois demonstrou diminuir o período pós-operatório morbidade, embora isso fosse contraditório com outra série que relatou morbidade semelhante.
A vantagem do TEM sobre as técnicas endoscópicas é a ressecção de espessura total de grandes lesões,
daí resultando uma taxa teórica de ressecção completa de 100%. É particularmente relevante para lesões da porções baixas ou intermediárias do reto, onde pode evitar a necessidade de ressecção segmentar
cirurgia e suas morbidades associadas para lesões passíveis de excisão local.
O TEM se tornou o técnica de ressecção de referência para lesões retais malignas T1 (sm1-2), como uma alternativa para ESD.
A vantagem do TEM sobre as técnicas endoscópicas é a ressecção de espessura total de grandes lesões,
daí resultando uma taxa teórica de ressecção completa de 100%. É particularmente relevante para lesões da porções baixas ou intermediárias do reto, onde pode evitar a necessidade de ressecção segmentar
cirurgia e suas morbidades associadas para lesões passíveis de excisão local.
O TEM se tornou o técnica de ressecção de referência para lesões retais malignas T1 (sm1-2), como uma alternativa para ESD.
Resultados do TEM nos TNERs
Estudos sobre os resultados de TEM nos TNERs são limitados e heterogêneos. Três séries relataram um total de 107 TNERs tratados por TEM, que alcançaram uma taxa de R0 de 100%, enquanto duas outras séries relataram margens R1 em 3/16 e 2/23 pacientes, respectivamente. A taxa de recorrência foi muito limitada, embora a duração do acompanhamento fosse frequentemente curta. A média de internação hospitalar é geralmente de 2 a 3 dias e os eventos adversos mais frequentes são retenção aguda de urina (até 20%), dor anal pós-operatória e sangramento ocasional.
O TEM parece muito apropriado para ressecção de resgate após excisão endoscópica incompleta, com
resultados tão favoráveis quanto à ressecção primária. De fato, quatro séries relataram uma taxa de ressecção R0 de 100% em 68 pacientes no total, em que TEM foi realizado após polipectomia incompleta, sem notável morbidade.
O TEM requer experiência, embora a curva de aprendizado relacionada possa ser relativamente curta, com um estudo estimando que um mínimo de 10 casos é necessário para um cirurgião ser proficiente com esta técnica. Ainda assim, o TEM não é amplamente aplicável e deve ser reservado a centros especializados.
No geral, o TEM parece eficaz e seguro para TNERs <20 mm com características típicas, evitando a necessidade de extensas ressecções cirúrgicas.
Cirurgia radical, incluindo abordagem laparoscópica e transabdominal
Princípios da cirurgia radical para RNET
A cirurgia retal radical com linfadenectomia deve ser discutida em todos os casos de TNERs com suspeita ou com alto risco de metástase linfonodal (LNM). Para esses pacientes, é recomendável realizar a ressecção anterior baixa oncológica (LAR) com excisão mesorretal total (TME). Por analogia com o câncer retal, a cirurgia laparoscópica se tornou a abordagem cirúrgica padrão porque alcança melhores resultados de curto e longo prazo em comparação com a cirurgia transabdominal.
Selecionar os pacientes para a cirurgia com base nos critérios propostos acima parece apropriado e conveniente, pois pode identificar adequadamente os pacientes com metástase linfonodal. Os resultados a longo prazo são favoráveis, com uma taxa de R0 de 100% em pacientes não metastáticos e muito baixo taxa de recorrência (3% e10% após um acompanhamento de 42-68 meses). A cirurgia laparoscópica radical não parece menos eficaz nem mais tecnicamente difícil no caso de ressecção endoscópica incompleta anterior, portanto, é um procedimento de terapia de resgate apropriado.
Estudos sobre os resultados de TEM nos TNERs são limitados e heterogêneos. Três séries relataram um total de 107 TNERs tratados por TEM, que alcançaram uma taxa de R0 de 100%, enquanto duas outras séries relataram margens R1 em 3/16 e 2/23 pacientes, respectivamente. A taxa de recorrência foi muito limitada, embora a duração do acompanhamento fosse frequentemente curta. A média de internação hospitalar é geralmente de 2 a 3 dias e os eventos adversos mais frequentes são retenção aguda de urina (até 20%), dor anal pós-operatória e sangramento ocasional.
O TEM parece muito apropriado para ressecção de resgate após excisão endoscópica incompleta, com
resultados tão favoráveis quanto à ressecção primária. De fato, quatro séries relataram uma taxa de ressecção R0 de 100% em 68 pacientes no total, em que TEM foi realizado após polipectomia incompleta, sem notável morbidade.
O TEM requer experiência, embora a curva de aprendizado relacionada possa ser relativamente curta, com um estudo estimando que um mínimo de 10 casos é necessário para um cirurgião ser proficiente com esta técnica. Ainda assim, o TEM não é amplamente aplicável e deve ser reservado a centros especializados.
No geral, o TEM parece eficaz e seguro para TNERs <20 mm com características típicas, evitando a necessidade de extensas ressecções cirúrgicas.
Cirurgia radical, incluindo abordagem laparoscópica e transabdominal
Princípios da cirurgia radical para RNET
A cirurgia retal radical com linfadenectomia deve ser discutida em todos os casos de TNERs com suspeita ou com alto risco de metástase linfonodal (LNM). Para esses pacientes, é recomendável realizar a ressecção anterior baixa oncológica (LAR) com excisão mesorretal total (TME). Por analogia com o câncer retal, a cirurgia laparoscópica se tornou a abordagem cirúrgica padrão porque alcança melhores resultados de curto e longo prazo em comparação com a cirurgia transabdominal.
Selecionar os pacientes para a cirurgia com base nos critérios propostos acima parece apropriado e conveniente, pois pode identificar adequadamente os pacientes com metástase linfonodal. Os resultados a longo prazo são favoráveis, com uma taxa de R0 de 100% em pacientes não metastáticos e muito baixo taxa de recorrência (3% e10% após um acompanhamento de 42-68 meses). A cirurgia laparoscópica radical não parece menos eficaz nem mais tecnicamente difícil no caso de ressecção endoscópica incompleta anterior, portanto, é um procedimento de terapia de resgate apropriado.
TNER sem fatores preditivos de metástase linfonodal (LNM)
✓ TNER <15 mm de tamanho sem característica desfavorável estão associados a um risco muito baixo de LNM e podem ser ressecados adequadamente por excisão local. A polipectomia ou mucosectomia padrão não deve ser realizada na suspeita de TNER ou quando realizada deve sempre marcar o local de ressecção.
✓ Se o tamanho do tumor for <10 mm, a mucosectomia assistida por ligadura (EMR-L) aparece como a técnica endoscópica mais apropriada, quando atinge taxas de ressecção completa em mais de 95% dos casos.
✓ Em relação ao TNER medindo 10 a 15 mm, as duas técnicas mais relevantes parecem ser ESD e
TEM, que pode ser superior ao EMR-L, embora não tenham sido comparados de forma adequada. Na ausência de comparação prospectiva, ambos podem ser realizados neste indicação, dependendo da experiência local.
✓ Em caso de ressecção incompleta após a ressecção endoscópica inicial, atualmente não está claro
se a terapia de resgate é necessária, mas em caso afirmativo, TEM e ESD aparecem como a tecnologia mais apropriada, com TEM provavelmente sendo preferível no caso de tamanho do tumor > 10 mm e/ou margem de profundidade incompleta.
✓ TNER associado a fatores preditivos de LNM. TNER > 15 mm de tamanho, e/ou aqueles com características desfavoráveis, são bons candidatos para cirurgia radical com linfadenectomia. No entanto, em pacientes com comorbidades, os riscos associados a a cirurgia radical pode superar seus benefícios. Neste cenário, ESD ou TEM podem ser considerados, embora não permita o reconhecimento do status do linfonodo, portanto, o acompanhamento deve ser adaptado com intervalos mais curtos.
✓ TNER <15 mm de tamanho sem característica desfavorável estão associados a um risco muito baixo de LNM e podem ser ressecados adequadamente por excisão local. A polipectomia ou mucosectomia padrão não deve ser realizada na suspeita de TNER ou quando realizada deve sempre marcar o local de ressecção.
✓ Se o tamanho do tumor for <10 mm, a mucosectomia assistida por ligadura (EMR-L) aparece como a técnica endoscópica mais apropriada, quando atinge taxas de ressecção completa em mais de 95% dos casos.
✓ Em relação ao TNER medindo 10 a 15 mm, as duas técnicas mais relevantes parecem ser ESD e
TEM, que pode ser superior ao EMR-L, embora não tenham sido comparados de forma adequada. Na ausência de comparação prospectiva, ambos podem ser realizados neste indicação, dependendo da experiência local.
✓ Em caso de ressecção incompleta após a ressecção endoscópica inicial, atualmente não está claro
se a terapia de resgate é necessária, mas em caso afirmativo, TEM e ESD aparecem como a tecnologia mais apropriada, com TEM provavelmente sendo preferível no caso de tamanho do tumor > 10 mm e/ou margem de profundidade incompleta.
✓ TNER associado a fatores preditivos de LNM. TNER > 15 mm de tamanho, e/ou aqueles com características desfavoráveis, são bons candidatos para cirurgia radical com linfadenectomia. No entanto, em pacientes com comorbidades, os riscos associados a a cirurgia radical pode superar seus benefícios. Neste cenário, ESD ou TEM podem ser considerados, embora não permita o reconhecimento do status do linfonodo, portanto, o acompanhamento deve ser adaptado com intervalos mais curtos.
✓ TNER <10 mm completamente ressecado por ressecção R0 local ou radical que não estão associados a fatores preditivo de LNM:
Retoscopia flexível de vigilância em 1 ano, 3 anos e a cada 5 anos. A vigilância é recomendada por analogia com o câncer retal.
✓ TNER ≥ 10 mm ou com ressecção endoscópica com características desfavoráveis ou ressecção R1 sem terapia de resgate:
Retoscopia flexível e ultrassom endoscópico a cada 6 a 12 meses por pelo menos 5 anos.
Biópsias sistemáticas da área de ressecção, se identificada, durante a retoscopia flexível pode ser relevante para detectar recidiva local precoce, mas isso ainda não foi avaliado.
Ressonância magnética abdominal e pélvica anual deve ser realizada para detectar recorrências perirretais e/ou distantes (fígado).
A duração do acompanhamento permanece desconhecida, pois os dados sobre o monitoramento a longo prazo dos TNERs são escassos. A colonoscopia total deve ser realizada a cada 5 anos.
Retoscopia flexível de vigilância em 1 ano, 3 anos e a cada 5 anos. A vigilância é recomendada por analogia com o câncer retal.
✓ TNER ≥ 10 mm ou com ressecção endoscópica com características desfavoráveis ou ressecção R1 sem terapia de resgate:
Retoscopia flexível e ultrassom endoscópico a cada 6 a 12 meses por pelo menos 5 anos.
Biópsias sistemáticas da área de ressecção, se identificada, durante a retoscopia flexível pode ser relevante para detectar recidiva local precoce, mas isso ainda não foi avaliado.
Ressonância magnética abdominal e pélvica anual deve ser realizada para detectar recorrências perirretais e/ou distantes (fígado).
A duração do acompanhamento permanece desconhecida, pois os dados sobre o monitoramento a longo prazo dos TNERs são escassos. A colonoscopia total deve ser realizada a cada 5 anos.
TNERs são neoplasias raras, mas com prevalência em constante aumento. Sua gestão deve ser adaptada dependendo da presença ou ausência de metástase linfonodal, estágio T (tamanho do tumor), aspecto endoscópico atípico, grau histológico e invasão linfovascular.
TNERs de baixo risco pode ser tratado localmente, usando ESMR-L para lesões < 10 mm e ESD ou TEM para lesões entre 10 e 15 mm em centros especializados porque exigem técnica e experiência. Essas técnicas também são importantes no salvamento após o tratamento endoscópico de TNER de baixo risco ressecado incompletamente. Por outro lado, cirurgia radical com linfadenectomia deve ser proposta na presença de qualquer fator desfavorável.
O reconhecimento do TNER durante a colonoscopia inicial é de suma importância para a tomada de decisão da gestão apropriada. Se houver suspeita de TNER, a polipectomia padrão ou mucosectomia (EMR) não deve ser realizada, mas se for ressecada o local da ressecção deve ser tatuado.
Os principais fatores associados ao risco de metástases em linfonodos (LNM) em TNER são a invasão da muscular própria (T2), tamanho do tumor (> 15 mm), aspecto endoscópico atípico, grau de diferenciação 2 ou 3 e invasão linfovascular. A sua identificação depende da análise histopatológica especializada, US endoscópico e ressonância magnética pélvica.
TNERs de baixo risco pode ser tratado localmente, usando ESMR-L para lesões < 10 mm e ESD ou TEM para lesões entre 10 e 15 mm em centros especializados porque exigem técnica e experiência. Essas técnicas também são importantes no salvamento após o tratamento endoscópico de TNER de baixo risco ressecado incompletamente. Por outro lado, cirurgia radical com linfadenectomia deve ser proposta na presença de qualquer fator desfavorável.
O reconhecimento do TNER durante a colonoscopia inicial é de suma importância para a tomada de decisão da gestão apropriada. Se houver suspeita de TNER, a polipectomia padrão ou mucosectomia (EMR) não deve ser realizada, mas se for ressecada o local da ressecção deve ser tatuado.
Os principais fatores associados ao risco de metástases em linfonodos (LNM) em TNER são a invasão da muscular própria (T2), tamanho do tumor (> 15 mm), aspecto endoscópico atípico, grau de diferenciação 2 ou 3 e invasão linfovascular. A sua identificação depende da análise histopatológica especializada, US endoscópico e ressonância magnética pélvica.
Isenção de responsabilidade
As informações contidas neste artigo são apenas para fins educacionais e não devem ser usadas para diagnóstico ou para orientar o tratamento sem o parecer de um profissional de saúde. Qualquer leitor que está preocupado com sua saúde deve entrar em contato com um médico para aconselhamento.
As informações contidas neste artigo são apenas para fins educacionais e não devem ser usadas para diagnóstico ou para orientar o tratamento sem o parecer de um profissional de saúde. Qualquer leitor que está preocupado com sua saúde deve entrar em contato com um médico para aconselhamento.