Síndrome do Intestino Irritável
A síndrome do intestino irritável (SII) é um distúrbio funcional crônico do trato gastrointestinal caracterizado por dor abdominal crônica associada a alterações na forma fezes e/ou frequência das evacuações na ausência de qualquer causa orgânica. Por esta razão, tem sido referido como um distúrbio gastrointestinal "funcional". A condição afeta indivíduos saudáveis em qualquer momento e, na maioria das pessoas, apresenta um curso recidivante e remitente.
Definição da síndrome do intestino irritável
Epidemiologia (frequência e a distribuição) da síndrome do intestino irritável
Etiologia e patogênese da síndrome do intestino irritável
Fatores de risco para a síndrome do intestino irritável
Manifestações clínicas da síndrome do intestino irritável
Critérios de diagnóstico de Roma IV para a síndrome do intestino irritável
Abordagem diagnóstica e diagnóstico diferencial da síndrome do intestino irritável
Tratamento e manejo da síndrome do intestino irritável
Dieta no tratamento da síndrome do intestino irritável
Fibra no tratamento da síndrome do intestino irritável
PEG 4.000 no tratamento da síndrome do intestino irritável
Atividade física no tratamento da síndrome do intestino irritável
Probióticos no tratamento da síndrome do intestino irritável (SII)
Tratamento farmacológico da síndrome do intestino irritável (SII)
Antidepressivos no tratamento da síndrome do intestino irritável (SII)
Antibióticos no tratamento da síndrome do intestino irritável (SII)
Tratamento da síndrome do intestino irritável com constipação (SII-C)
Tratamento da síndrome do intestino irritável com dor e inchaço abdominal sem predominância de diarreia e constipação (SII-M)
Tratamento da síndrome do intestino irritável com diarreia (SII-D)
Tratamento da síndrome do intestino irritável (SII) em pacientes refratários
Infecção por Helicobacter pylori (H. pylori) na síndrome do intestino irritável
RESUMO DE RECOMENDAÇÕES NA SÍNDROME DO INTESTINO IRRITÁVEL
Epidemiologia (frequência e a distribuição) da síndrome do intestino irritável
Etiologia e patogênese da síndrome do intestino irritável
Fatores de risco para a síndrome do intestino irritável
Manifestações clínicas da síndrome do intestino irritável
Critérios de diagnóstico de Roma IV para a síndrome do intestino irritável
Abordagem diagnóstica e diagnóstico diferencial da síndrome do intestino irritável
Tratamento e manejo da síndrome do intestino irritável
Dieta no tratamento da síndrome do intestino irritável
Fibra no tratamento da síndrome do intestino irritável
PEG 4.000 no tratamento da síndrome do intestino irritável
Atividade física no tratamento da síndrome do intestino irritável
Probióticos no tratamento da síndrome do intestino irritável (SII)
Tratamento farmacológico da síndrome do intestino irritável (SII)
Antidepressivos no tratamento da síndrome do intestino irritável (SII)
Antibióticos no tratamento da síndrome do intestino irritável (SII)
Tratamento da síndrome do intestino irritável com constipação (SII-C)
Tratamento da síndrome do intestino irritável com dor e inchaço abdominal sem predominância de diarreia e constipação (SII-M)
Tratamento da síndrome do intestino irritável com diarreia (SII-D)
Tratamento da síndrome do intestino irritável (SII) em pacientes refratários
Infecção por Helicobacter pylori (H. pylori) na síndrome do intestino irritável
RESUMO DE RECOMENDAÇÕES NA SÍNDROME DO INTESTINO IRRITÁVEL
A síndrome do intestino irritável (SII) é um distúrbio funcional crônico do trato gastrointestinal caracterizado por dor abdominal crônica associada a alterações na forma fezes e/ou frequência das evacuações na ausência de qualquer causa orgânica. Por esta razão, tem sido referido como um distúrbio gastrointestinal "funcional". A condição afeta indivíduos saudáveis em qualquer momento e, na maioria das pessoas, apresenta um curso recidivante e remitente.
A síndrome do intestino irritável (SII) é um distúrbio gastrointestinal funcional que tem um impacto substancial na qualidade de vida e no funcionamento social de algumas pessoas.
A maioria dos pacientes com síndrome do intestino irritável (SII) apresenta sintomas crônicos que variam em gravidade ao longo do tempo. Os pacientes também podem sofrer uma mudança no subtipo de SII ao longo do tempo, sendo a mudança mais frequente a partir de constipação predominante ou diarreia para hábito intestinal misto.
A SII está agrupada nas síndromes somáticas funcionais. Os critérios diagnósticos são focados nos sintomas gastrointestinais, mas deve-se notar que os sintomas extra-intestinais são comuns na SII e a análise de agrupamento sugere que distúrbios como SII, disfunção da articulação temporomandibular (DTM), dor pélvica crônica, cefaleia tensional, fibromialgia, doença do refluxo gastroesofágico, dispepsia funcional, dor torácica não cardíaca e distúrbios psiquiátricos, incluindo depressão, ansiedade e somatização, entre outras, coexistem com mais frequência do que ocorreria ao acaso.
A síndrome do intestino irritável (SII) é um distúrbio gastrointestinal funcional que tem um impacto substancial na qualidade de vida e no funcionamento social de algumas pessoas.
A maioria dos pacientes com síndrome do intestino irritável (SII) apresenta sintomas crônicos que variam em gravidade ao longo do tempo. Os pacientes também podem sofrer uma mudança no subtipo de SII ao longo do tempo, sendo a mudança mais frequente a partir de constipação predominante ou diarreia para hábito intestinal misto.
A SII está agrupada nas síndromes somáticas funcionais. Os critérios diagnósticos são focados nos sintomas gastrointestinais, mas deve-se notar que os sintomas extra-intestinais são comuns na SII e a análise de agrupamento sugere que distúrbios como SII, disfunção da articulação temporomandibular (DTM), dor pélvica crônica, cefaleia tensional, fibromialgia, doença do refluxo gastroesofágico, dispepsia funcional, dor torácica não cardíaca e distúrbios psiquiátricos, incluindo depressão, ansiedade e somatização, entre outras, coexistem com mais frequência do que ocorreria ao acaso.
A SII é a doença gastrointestinal mais diagnosticada sendo responsável por aproximadamente 30% de todos os atendimentos em gastroenterologia. No entanto, apenas uma pequena porcentagem das pessoas afetadas procura atendimento médico.
A SII tem uma prevalência muito alta, aproximadamente 10 a 15% da população adulta. Os pacientes com SII são mais propensos a procurar cuidados de saúde e realizar exames para sintomas não relacionados à SII. A procura por cuidados de saúde também está provavelmente associada ao acesso aos cuidados de saúde e é maior entre aqueles empregados e com plano de saúde.
É difícil tirar conclusões sobre a prevalência dos diferentes subtipos do hábito intestinal, uma vez que os estudos utilizam critérios diferentes em diferentes populações. Em estudos de base populacional usando os critérios de Roma IV, as taxas de prevalência de SII com diarreia (SII-D) e SII com sintomas mistos (SII-M) são semelhantes e representam 70-80% da SII. Menos de 5% são não subtipados (SII-U) e o restante (+/-25%) são SII com constipação (SII-C).
A SII é mais prevalente em mulheres. Um estudo de Roma IV encontrou um aumento duas vezes maior na prevalência de SII em mulheres vs homens. Mulheres com SII são mais propensas a ter SII-C e menos propensas a ter SII-D.
A SII é mais comumente diagnosticada em pacientes com menos de 50 anos, sendo mais prevalente entre aqueles com menor renda. O nível socioeconômico mais baixo também está associado ao aumento da prevalência de ansiedade e depressão na SII.
Aproximadamente 40% dos indivíduos que atendem aos critérios de diagnóstico de SII não têm um diagnóstico formal. A SII está associada ao aumento dos custos com assistência médica e é a segunda maior causa de absenteísmo no trabalho.
Pacientes com SII consistentemente demonstram ter uma qualidade de vida ruim. O comprometimento é comparável a outras doenças crônicas, como a doença do refluxo gastroesofágico (DRGE), diabetes, hipertensão e depressão.
A SII tem uma prevalência muito alta, aproximadamente 10 a 15% da população adulta. Os pacientes com SII são mais propensos a procurar cuidados de saúde e realizar exames para sintomas não relacionados à SII. A procura por cuidados de saúde também está provavelmente associada ao acesso aos cuidados de saúde e é maior entre aqueles empregados e com plano de saúde.
É difícil tirar conclusões sobre a prevalência dos diferentes subtipos do hábito intestinal, uma vez que os estudos utilizam critérios diferentes em diferentes populações. Em estudos de base populacional usando os critérios de Roma IV, as taxas de prevalência de SII com diarreia (SII-D) e SII com sintomas mistos (SII-M) são semelhantes e representam 70-80% da SII. Menos de 5% são não subtipados (SII-U) e o restante (+/-25%) são SII com constipação (SII-C).
A SII é mais prevalente em mulheres. Um estudo de Roma IV encontrou um aumento duas vezes maior na prevalência de SII em mulheres vs homens. Mulheres com SII são mais propensas a ter SII-C e menos propensas a ter SII-D.
A SII é mais comumente diagnosticada em pacientes com menos de 50 anos, sendo mais prevalente entre aqueles com menor renda. O nível socioeconômico mais baixo também está associado ao aumento da prevalência de ansiedade e depressão na SII.
Aproximadamente 40% dos indivíduos que atendem aos critérios de diagnóstico de SII não têm um diagnóstico formal. A SII está associada ao aumento dos custos com assistência médica e é a segunda maior causa de absenteísmo no trabalho.
Pacientes com SII consistentemente demonstram ter uma qualidade de vida ruim. O comprometimento é comparável a outras doenças crônicas, como a doença do refluxo gastroesofágico (DRGE), diabetes, hipertensão e depressão.
A fisiopatologia da SII permanece incerta. É visto como um distúrbio resultante de uma interação entre vários fatores. Apesar de várias investigações, os dados são conflitantes e não foi encontrada nenhuma anormalidade específica para esse distúrbio. O foco tradicional nos estudos tem sido as alterações na motilidade gastrointestinal e na hipersensibilidade visceral. Estudos mais contemporâneos consideraram o papel da inflamação, alterações na flora fecal e crescimento bacteriano. Também está sendo considerado o papel da sensibilidade alimentar. A existência de uma predisposição genética também está sendo investigada.
Embora anormalidades motoras do trato gastrointestinal (contrações intestinais aumentadas e irregulares e tempo de trânsito colônico anormal) sejam detectáveis em alguns pacientes com SII, nenhum padrão predominante de atividade motora emergiu como um marcador para a SII.
A hipersensibilidade (quando a resposta a estímulos intestinais está aumentada, ou seja, estímulos que normalmente passariam despercebidos como: consciência e a dor causadas pela distensão intestinal e aumento mensurável na circunferência abdominal associada ao inchaço [sensação de plenitude abdominal], embora isso possa não estar relacionado a quantidade de gás intestinal) seletiva dos nervos viscerais no intestino foi observada em pacientes com SII e é uma explicação para os sintomas da SII.
Inflamação intestinal com ativação do sistema imunológico da mucosa caracterizada por alterações em determinadas células imunes e marcadores em alguns pacientes com síndrome do intestino irritável como o aumento do número de linfócitos e mastócitos no cólon e no intestino delgado.
Alguns pacientes relacionam o aparecimento dos sintomas da SII após uma gastroenterite infecciosa (diarreia aguda). A causa dos sintomas intestinais após infecção aguda é incerta, embora várias teorias (má absorção, aumento de células enteroendócrinas/linfócitos e uso de antibióticos) tenham sido propostas.
Existem especulações de que mudanças na composição da flora intestinal (microflora fecal) estariam associadas a síndrome do intestino irritável (SII). Dados sugerem que a microbiota fecal em indivíduos com SII difere de controles saudáveis e varia de acordo com o sintoma predominante. Estudos encontraram, em alguns pacientes, redução de lactobacillus e bifidobacteria e aumento das concentrações de espécies como enterobacteriaceae, coliformes e bacteroides, particularmente nos pacientes com diarreia ou constipação.
O supercrescimento bacteriano do intestino delgado está associado a um aumento do número e/ou tipo de bactérias no intestino delgado. No entanto, dados relatando associação entre síndrome do intestino irritável (SII) e supercrescimento bacteriano do intestino delgado têm sido conflitantes.
O papel dos alimentos na fisiopatologia da SII não está claro. As investigações se concentraram no desenvolvimento de anticorpos específicos para alimentos, má absorção de carboidratos e sensibilidade ao glúten. Alguns pacientes com SII relatam piora dos sintomas após comer e percebem intolerância alimentar a certos alimentos. Má absorção de carboidratos fermentáveis (frutose, sorbitol e lactose) no cólon levariam aos sintomas da SII, no entanto, o papel da má absorção de carboidratos continua sendo um tópico de investigação. Sensibilidade ao glúten, vários estudos sugerem alguma sobreposição entre doença celíaca e SII, sendo assim, devem ser tomadas medidas para confirmar a ausência de doença celíaca antes do diagnóstico de SII em um paciente com testes sorológicos sugestivos de doença celíaca.
A suscetibilidade genética à SII é sugerida por vários estudos com gêmeos, embora os padrões familiares também possam refletir fatores sociais subjacentes. Associações entre genes específicos e SII estão sob investigação.
Fatores psicossociais podem influenciar a expressão dos sintomas da SII. Uma hipótese unificadora sobre o papel na SII do estresse e do neuroticismo psicológico (nível crônico de desajustamento e instabilidade emocional). As pessoas passam a apresentar padrões emocionais associados a um desconforto psicológico causado por aflições, angústias e sofrimentos.
É frequente a associação entre as crises da SII e o estresse e também a coexistência de distúrbios psiquiátricos ou psicológicos. A prevalência de distúrbios psiquiátricos e psicológicos (depressão, ansiedade e insônia) varia de 40% a 90%, portanto estão fortemente associados à SII. A depressão, relativamente mais comum, apresenta prevalência de 30% na SII em comparação com 18% na população em geral. Também é observada em alguns pacientes a transição para outras manifestações funcionais digestivas, como a dispepsia funcional e proctalgia.
Embora anormalidades motoras do trato gastrointestinal (contrações intestinais aumentadas e irregulares e tempo de trânsito colônico anormal) sejam detectáveis em alguns pacientes com SII, nenhum padrão predominante de atividade motora emergiu como um marcador para a SII.
A hipersensibilidade (quando a resposta a estímulos intestinais está aumentada, ou seja, estímulos que normalmente passariam despercebidos como: consciência e a dor causadas pela distensão intestinal e aumento mensurável na circunferência abdominal associada ao inchaço [sensação de plenitude abdominal], embora isso possa não estar relacionado a quantidade de gás intestinal) seletiva dos nervos viscerais no intestino foi observada em pacientes com SII e é uma explicação para os sintomas da SII.
Inflamação intestinal com ativação do sistema imunológico da mucosa caracterizada por alterações em determinadas células imunes e marcadores em alguns pacientes com síndrome do intestino irritável como o aumento do número de linfócitos e mastócitos no cólon e no intestino delgado.
Alguns pacientes relacionam o aparecimento dos sintomas da SII após uma gastroenterite infecciosa (diarreia aguda). A causa dos sintomas intestinais após infecção aguda é incerta, embora várias teorias (má absorção, aumento de células enteroendócrinas/linfócitos e uso de antibióticos) tenham sido propostas.
Existem especulações de que mudanças na composição da flora intestinal (microflora fecal) estariam associadas a síndrome do intestino irritável (SII). Dados sugerem que a microbiota fecal em indivíduos com SII difere de controles saudáveis e varia de acordo com o sintoma predominante. Estudos encontraram, em alguns pacientes, redução de lactobacillus e bifidobacteria e aumento das concentrações de espécies como enterobacteriaceae, coliformes e bacteroides, particularmente nos pacientes com diarreia ou constipação.
O supercrescimento bacteriano do intestino delgado está associado a um aumento do número e/ou tipo de bactérias no intestino delgado. No entanto, dados relatando associação entre síndrome do intestino irritável (SII) e supercrescimento bacteriano do intestino delgado têm sido conflitantes.
O papel dos alimentos na fisiopatologia da SII não está claro. As investigações se concentraram no desenvolvimento de anticorpos específicos para alimentos, má absorção de carboidratos e sensibilidade ao glúten. Alguns pacientes com SII relatam piora dos sintomas após comer e percebem intolerância alimentar a certos alimentos. Má absorção de carboidratos fermentáveis (frutose, sorbitol e lactose) no cólon levariam aos sintomas da SII, no entanto, o papel da má absorção de carboidratos continua sendo um tópico de investigação. Sensibilidade ao glúten, vários estudos sugerem alguma sobreposição entre doença celíaca e SII, sendo assim, devem ser tomadas medidas para confirmar a ausência de doença celíaca antes do diagnóstico de SII em um paciente com testes sorológicos sugestivos de doença celíaca.
A suscetibilidade genética à SII é sugerida por vários estudos com gêmeos, embora os padrões familiares também possam refletir fatores sociais subjacentes. Associações entre genes específicos e SII estão sob investigação.
Fatores psicossociais podem influenciar a expressão dos sintomas da SII. Uma hipótese unificadora sobre o papel na SII do estresse e do neuroticismo psicológico (nível crônico de desajustamento e instabilidade emocional). As pessoas passam a apresentar padrões emocionais associados a um desconforto psicológico causado por aflições, angústias e sofrimentos.
É frequente a associação entre as crises da SII e o estresse e também a coexistência de distúrbios psiquiátricos ou psicológicos. A prevalência de distúrbios psiquiátricos e psicológicos (depressão, ansiedade e insônia) varia de 40% a 90%, portanto estão fortemente associados à SII. A depressão, relativamente mais comum, apresenta prevalência de 30% na SII em comparação com 18% na população em geral. Também é observada em alguns pacientes a transição para outras manifestações funcionais digestivas, como a dispepsia funcional e proctalgia.
Infecção gastrointestinal e distúrbios psicológicos parecem ser fatores de risco distintos, contribuindo aditivamente para o desenvolvimento tanto da SII pós-infecção quanto dos sintomas extra-intestinais frequentemente ligados à SII, como a fadiga crônica.
Fatores de risco não modificáveis para a síndrome do intestino irritável
Vários fatores estão associados a uma maior probabilidade de SII. Alguns desses fatores não são modificáveis, como a quarta e quinta décadas de idade, ser solteiro(a) e um histórico familiar positivo de SII, parente de primeiro grau.
O sexo feminino também é fator de risco para SII. Isto pode ser justificado pelo papel do estrogénio na regulação de dois dos três princípios principais da SII, que são a motilidade GI e a dor visceral.
A infecção gastrointestinal é o fator de risco mais forte para SII e está associada a um aumento de aproximadamente quatro vezes no risco de sintomas de SII nos próximos 12 meses em comparação com indivíduos não infectados. O risco é ainda maior naqueles com condições gastrointestinais preexistentes, como DRGE ou dispepsia, história de doença diarreica mais grave, idade mais jovem, sexo feminino, eventos de vida estressantes crônicos ou comorbidades psicológicas. A SII é mais frequentemente caracterizada por diarreia ou hábito intestinal misto.
Os fatores de risco não modificáveis também incluem histórico pessoal de alergias, histórico pessoal de doenças crônicas (especialmente hipertensão e diabetes), transtorno de ansiedade generalizada e histórico de infecção por COVID-19 no ano anterior.
Fatores de risco modificáveis para a síndrome do intestino irritável
Os fatores de risco modificáveis incluem IMC anormal (alto ou baixo), tabagismo, dieta rica em proteínas ou gorduras e consumo de bebidas com cafeína.
A atividade física aceitável está associada a uma menor incidência de SII. As atividades moderadas a vigorosas de 3 a 5 dias por semana resultam em melhora clínica dos sintomas da SII.
Um estudo recente descreveu a associação entre tabagismo intenso (20 ou mais cigarros por dia) e a ocorrência de SII-diarreia. Isto pode ser explicado pelos efeitos diretos da nicotina na função motora do cólon.
Em relação à dieta, uma dieta ocidental rica em gordura tem sido associada à SII. Estudos anteriores também demonstraram que o uso de fibras solúveis (por exemplo, aveia e frutas) resulta na melhora dos sintomas. No entanto, as fibras insolúveis (por exemplo, farelo de trigo) não foram significativas e até causaram distensão abdominal.
Fatores psicossociais podem influenciar a presença e evolução dos sintomas da SII. Existe uma associação entre os sintomas da SII e o estresse de vida atual para muitos pacientes com SII, e o desenvolvimento da SII-diarreia também está associado a eventos de vida estressantes. É frequente a associação entre as crises da SII e o estresse e a coexistência de distúrbios psiquiátricos ou psicológicos (depressão, ansiedade e insônia). A depressão apresenta prevalência de 30% na SII em comparação com 18% na população em geral.
Fatores de risco não modificáveis para a síndrome do intestino irritável
Vários fatores estão associados a uma maior probabilidade de SII. Alguns desses fatores não são modificáveis, como a quarta e quinta décadas de idade, ser solteiro(a) e um histórico familiar positivo de SII, parente de primeiro grau.
O sexo feminino também é fator de risco para SII. Isto pode ser justificado pelo papel do estrogénio na regulação de dois dos três princípios principais da SII, que são a motilidade GI e a dor visceral.
A infecção gastrointestinal é o fator de risco mais forte para SII e está associada a um aumento de aproximadamente quatro vezes no risco de sintomas de SII nos próximos 12 meses em comparação com indivíduos não infectados. O risco é ainda maior naqueles com condições gastrointestinais preexistentes, como DRGE ou dispepsia, história de doença diarreica mais grave, idade mais jovem, sexo feminino, eventos de vida estressantes crônicos ou comorbidades psicológicas. A SII é mais frequentemente caracterizada por diarreia ou hábito intestinal misto.
Os fatores de risco não modificáveis também incluem histórico pessoal de alergias, histórico pessoal de doenças crônicas (especialmente hipertensão e diabetes), transtorno de ansiedade generalizada e histórico de infecção por COVID-19 no ano anterior.
Fatores de risco modificáveis para a síndrome do intestino irritável
Os fatores de risco modificáveis incluem IMC anormal (alto ou baixo), tabagismo, dieta rica em proteínas ou gorduras e consumo de bebidas com cafeína.
A atividade física aceitável está associada a uma menor incidência de SII. As atividades moderadas a vigorosas de 3 a 5 dias por semana resultam em melhora clínica dos sintomas da SII.
Um estudo recente descreveu a associação entre tabagismo intenso (20 ou mais cigarros por dia) e a ocorrência de SII-diarreia. Isto pode ser explicado pelos efeitos diretos da nicotina na função motora do cólon.
Em relação à dieta, uma dieta ocidental rica em gordura tem sido associada à SII. Estudos anteriores também demonstraram que o uso de fibras solúveis (por exemplo, aveia e frutas) resulta na melhora dos sintomas. No entanto, as fibras insolúveis (por exemplo, farelo de trigo) não foram significativas e até causaram distensão abdominal.
Fatores psicossociais podem influenciar a presença e evolução dos sintomas da SII. Existe uma associação entre os sintomas da SII e o estresse de vida atual para muitos pacientes com SII, e o desenvolvimento da SII-diarreia também está associado a eventos de vida estressantes. É frequente a associação entre as crises da SII e o estresse e a coexistência de distúrbios psiquiátricos ou psicológicos (depressão, ansiedade e insônia). A depressão apresenta prevalência de 30% na SII em comparação com 18% na população em geral.
O principal sintoma da síndrome do intestino irritável (SII) é a dor abdominal crônica ou recorrente associada a hábitos intestinais alterados.
Dor abdominal crônica na síndrome do intestino irritável
A dor abdominal na SII é geralmente descrita como uma cólica com intensidade variável e exacerbações periódicas. A localização e o caráter da dor são muito variáveis, mas a maioria dos pacientes descreve a dor como cólica localizada no abdome inferior. A gravidade da dor pode variar de leve a grave. A dor está frequentemente relacionada à evacuação, enquanto em alguns pacientes a dor abdominal é aliviada com a evacuação, outro relatam piora da dor com a evacuação. O estresse emocional e as refeições podem agravar a dor. Pacientes com SII também relatam frequentemente inchaço abdominal e aumento da produção de gases na forma de flatulência ou arroto.
Alteração do hábito intestinal na síndrome do intestino irritável
Os sintomas da SII incluem diarreia, constipação, diarreia e constipação alternadas ou hábito intestinal normal alternado com diarreia e/ou constipação.
A diarreia é geralmente caracterizada pela evacuação amolecida, frequente e em volume pequeno a moderado. As evacuações geralmente ocorrem durante o horário de vigília, mais frequentemente pela manhã ou após as refeições. A maioria das evacuações é precedida por cólica abdominal e acompanhada de urgência fecal e sensação de evacuação incompleta ou tenesmo. Aproximadamente metade dos pacientes com SII se queixam da eliminação de muco com fezes. Diarreia volumosa, sangue, diarreia noturna e fezes oleosas não são características da SII.
A constipação é caracterizada por fezes geralmente endurecidas e podem ser descritas na forma de cíbalos (fragmentadas em bolas). Os pacientes também podem queixar-se de tenesmo mesmo quando o reto está vazio.
Suspeita-se da síndrome do intestino irritável (SII) em pacientes com dor abdominal crônica associado a alteração do hábito intestinal (constipação e/ou diarreia). O diagnóstico clínico da SII requer a presença dos critérios de diagnóstico baseados nos sintomas e na exclusão de doenças orgânicas subjacentes.
Dor abdominal crônica na síndrome do intestino irritável
A dor abdominal na SII é geralmente descrita como uma cólica com intensidade variável e exacerbações periódicas. A localização e o caráter da dor são muito variáveis, mas a maioria dos pacientes descreve a dor como cólica localizada no abdome inferior. A gravidade da dor pode variar de leve a grave. A dor está frequentemente relacionada à evacuação, enquanto em alguns pacientes a dor abdominal é aliviada com a evacuação, outro relatam piora da dor com a evacuação. O estresse emocional e as refeições podem agravar a dor. Pacientes com SII também relatam frequentemente inchaço abdominal e aumento da produção de gases na forma de flatulência ou arroto.
Alteração do hábito intestinal na síndrome do intestino irritável
Os sintomas da SII incluem diarreia, constipação, diarreia e constipação alternadas ou hábito intestinal normal alternado com diarreia e/ou constipação.
A diarreia é geralmente caracterizada pela evacuação amolecida, frequente e em volume pequeno a moderado. As evacuações geralmente ocorrem durante o horário de vigília, mais frequentemente pela manhã ou após as refeições. A maioria das evacuações é precedida por cólica abdominal e acompanhada de urgência fecal e sensação de evacuação incompleta ou tenesmo. Aproximadamente metade dos pacientes com SII se queixam da eliminação de muco com fezes. Diarreia volumosa, sangue, diarreia noturna e fezes oleosas não são características da SII.
A constipação é caracterizada por fezes geralmente endurecidas e podem ser descritas na forma de cíbalos (fragmentadas em bolas). Os pacientes também podem queixar-se de tenesmo mesmo quando o reto está vazio.
Suspeita-se da síndrome do intestino irritável (SII) em pacientes com dor abdominal crônica associado a alteração do hábito intestinal (constipação e/ou diarreia). O diagnóstico clínico da SII requer a presença dos critérios de diagnóstico baseados nos sintomas e na exclusão de doenças orgânicas subjacentes.
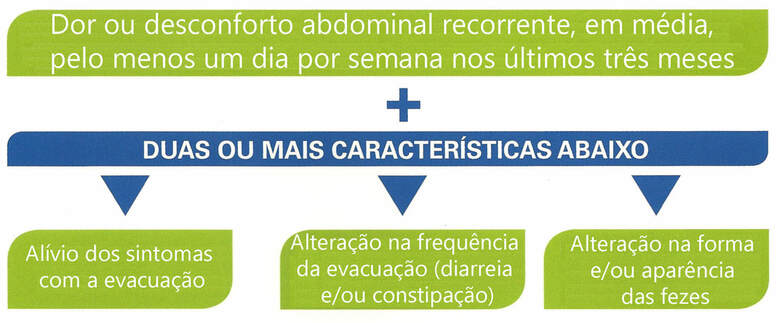
Os critérios de Roma IV são os mais utilizados. É definido como dor ou desconforto abdominal recorrente, em média, pelo menos um dia por semana nos últimos três meses, associado a dois ou mais dos seguintes critérios:
- Associado ao alívio dos sintomas com a evacuação;
- Associado a alteração na frequência da evacuação (diarreia e/ou constipação);
- Associado a alteração na forma e/ou aparência das fezes.
O “desconforto abdominal” é a distensão abdominal e/ou sensação de estufamento abdominal não descrita como dor pelo paciente.
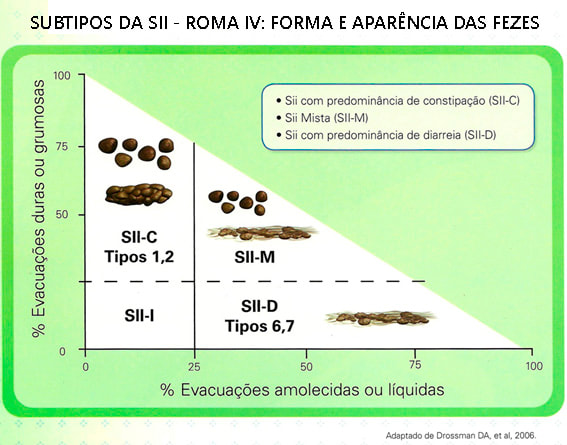
Subtipos da síndrome do intestino irritável
A síndrome do intestino irritável é subagrupada pelo hábito intestinal predominante. A forma das fezes é o melhor preditor do hábito intestinal predominante na SII, forma de fezes em vez de frequência, determina a subclassificação do hábito intestinal de acordo com os critérios de Roma IV. Além disso, um padrão intestinal imprevisível (≥3 tipos diferentes de fezes/semana) reforça o diagnóstico de SII-D, enquanto dias consecutivos sem evacuação estão associados à SII-C. A Escala de Bristol deve ser usada para classificar a forma das fezes
A síndrome do intestino irritável é subagrupada pelo hábito intestinal predominante. A forma das fezes é o melhor preditor do hábito intestinal predominante na SII, forma de fezes em vez de frequência, determina a subclassificação do hábito intestinal de acordo com os critérios de Roma IV. Além disso, um padrão intestinal imprevisível (≥3 tipos diferentes de fezes/semana) reforça o diagnóstico de SII-D, enquanto dias consecutivos sem evacuação estão associados à SII-C. A Escala de Bristol deve ser usada para classificar a forma das fezes
- SII com constipação predominante (SII-C) - mais de 25% das evacuações são de fezes endurecidas tipo 1 e 2 da Escala de Bristol. Mais comum no sexo feminino.
- SII com diarreia predominante (SII-D) - mais de 25% das evacuações são de fezes amolecidas tipo 6 e 7 da Escala de Bristol. Mais comum no sexo masculino.
- SII com hábitos intestinais mistos (SII-M) - mais de 25% das evacuações alternam fezes endurecidas tipo 1 e 2 da Escala de Bristol com fezes amolecidas tipo 6 e 7 da Escala de Bristol.
- SII não classificada (SII-NC) – quando os pacientes preenchem os critérios de diagnóstico para SII, mas não podem ser categorizados com precisão em um dos outros três subtipos.
Escala de Bristol da forma das fezes. O aspecto visual das fezes e dividido em sete tipos distintos:
Os sintomas intestinais flutuam frequentemente com o passar do tempo para muitos pacientes com SII, isto é, os sintomas podem estar presentes durante algum tempo e melhorar parcial ou totalmente por algum período. No entanto, estudos com períodos mais longos mostram maior estabilidade da forma fecal.
É comum os pacientes com SII apresentar sintomas de gases, distensão abdominal, dor ou plenitude abdominal e plenitude no reto. Alguns pacientes cursam com dor torácica e náuseas. É comum na SII que os sintomas como flatulência, dor abdominal e diarreia estejam associados a refeições com alimentos ricos em carboidratos ou gorduras, bem como café, álcool e alimentos condimentados.
É comum os pacientes com SII apresentar sintomas de gases, distensão abdominal, dor ou plenitude abdominal e plenitude no reto. Alguns pacientes cursam com dor torácica e náuseas. É comum na SII que os sintomas como flatulência, dor abdominal e diarreia estejam associados a refeições com alimentos ricos em carboidratos ou gorduras, bem como café, álcool e alimentos condimentados.
Sintomas extra-intestinais da síndrome do intestino irritável
Mais da metade das visitas e custos adicionais incorridos por pacientes com SII são para preocupações não gastrointestinais. Os sintomas não gastrointestinais que são mais comuns na SII do que nos controles e incluem o seguinte (prevalência): cefaleia (23–45%), dor nas costas (27–81%), fadiga (36–63%), mialgia (29–36%), dispareunia (9–42%), frequência urinária (21–61%), outros sintomas urinários e tontura (11–27%). O aumento da prevalência de alguns desses sintomas pode ser decorrente da coexistência de defecação dissinérgica. Sintomas extra-intestinais e psicológicos ocorrem mais frequentemente em mulheres do que em homens com SII. Pacientes com SII relatam fadiga e dificuldade para dormir.
Sexo e gênero nos sintomas da síndrome do intestino irritável
Em comparação com homens com SII, as mulheres com SII relatam maior gravidade geral dos sintomas da SII, intensidade da dor abdominal e distensão abdominal, impacto dos sintomas na vida diária e menor qualidade de vida. Não se sabe se isso é causado por diferenças na sensação de dor, resposta cognitiva à dor ou viés de relato. As mulheres também relatam mais sintomas extra-intestinais, como náuseas, urgência urinária e dispareunia, e são mais propensas a relatar sintomas de constipação e distensão abdominal.
Os sintomas em mulheres variam de acordo com o ciclo menstrual, com aumento do relato de sintomas gastrointestinais nas fases lútea tardia e menstrual, em comparação com a fase médio-folicular. Em particular, as mulheres relatam fezes mais soltas e mais sintomas gastrointestinais pouco antes e durante a menstruação e a sensibilidade retal demonstrou ser maior em mulheres com SII na menstruação em comparação com mulheres com SII em outras fases do ciclo menstrual.
Gravidade da síndrome do intestino irritável
A Fundação Roma propôs a categorização dos pacientes com SII em subgrupos de gravidade:
Mais da metade das visitas e custos adicionais incorridos por pacientes com SII são para preocupações não gastrointestinais. Os sintomas não gastrointestinais que são mais comuns na SII do que nos controles e incluem o seguinte (prevalência): cefaleia (23–45%), dor nas costas (27–81%), fadiga (36–63%), mialgia (29–36%), dispareunia (9–42%), frequência urinária (21–61%), outros sintomas urinários e tontura (11–27%). O aumento da prevalência de alguns desses sintomas pode ser decorrente da coexistência de defecação dissinérgica. Sintomas extra-intestinais e psicológicos ocorrem mais frequentemente em mulheres do que em homens com SII. Pacientes com SII relatam fadiga e dificuldade para dormir.
Sexo e gênero nos sintomas da síndrome do intestino irritável
Em comparação com homens com SII, as mulheres com SII relatam maior gravidade geral dos sintomas da SII, intensidade da dor abdominal e distensão abdominal, impacto dos sintomas na vida diária e menor qualidade de vida. Não se sabe se isso é causado por diferenças na sensação de dor, resposta cognitiva à dor ou viés de relato. As mulheres também relatam mais sintomas extra-intestinais, como náuseas, urgência urinária e dispareunia, e são mais propensas a relatar sintomas de constipação e distensão abdominal.
Os sintomas em mulheres variam de acordo com o ciclo menstrual, com aumento do relato de sintomas gastrointestinais nas fases lútea tardia e menstrual, em comparação com a fase médio-folicular. Em particular, as mulheres relatam fezes mais soltas e mais sintomas gastrointestinais pouco antes e durante a menstruação e a sensibilidade retal demonstrou ser maior em mulheres com SII na menstruação em comparação com mulheres com SII em outras fases do ciclo menstrual.
Gravidade da síndrome do intestino irritável
A Fundação Roma propôs a categorização dos pacientes com SII em subgrupos de gravidade:
- Pacientes com SII leve apresentam sintomas de baixa intensidade e boa qualidade de vida.
- Pacientes com SII de gravidade moderada apresentam sintomas mais persistentes, com mais desconforto e algum comprometimento da qualidade de vida.
- Pacientes com SII grave têm aumento da frequência, intensidade e persistência dos sintomas e apresentam comprometimento da qualidade de vida. Eles também têm mais comorbidade psicossocial, são mais frequentemente atendidos por especialistas e passam por mais testes diagnósticos. As mulheres são mais propensas a relatar sintomas mais graves do que os homens.
A maioria dos clínicos é capaz de reconhecer os sintomas da SII e se sentir confortável para fazer o diagnóstico. Apesar da disponibilidade de diretrizes, exames são frequentemente solicitados, sugerindo que muitos médicos ainda acreditam que a SII é um diagnóstico de exclusão.
A prevalência de doença orgânica, com exceção da doença celíaca e intolerância à lactose, na população com sintomas de SII (particularmente naquelas sem sinais de alarme) é semelhante à da população geral.
O diagnóstico diferencial para os sintomas da SII (Quadro 2) é muito amplo. No entanto, o uso dos critérios de Roma IV baseada em sintomas e a avaliação de sinais ou sintomas de alarme, bem como a exclusão da doença celíaca em algumas populações, são suficientes para fazer o diagnóstico de SII.
A prevalência de doença orgânica, com exceção da doença celíaca e intolerância à lactose, na população com sintomas de SII (particularmente naquelas sem sinais de alarme) é semelhante à da população geral.
O diagnóstico diferencial para os sintomas da SII (Quadro 2) é muito amplo. No entanto, o uso dos critérios de Roma IV baseada em sintomas e a avaliação de sinais ou sintomas de alarme, bem como a exclusão da doença celíaca em algumas populações, são suficientes para fazer o diagnóstico de SII.
Quadro 2 |
SII com constipação (IBS-C) Hipotiroidismo A constipação pode ser secundária a doença orgânica, anismo (contratura anal paradoxal) ou trânsito colônico lento (inércia colônica). |
SII com diarreia/sintomas mistos (IBS-D/M) Doença celíaca Má digestão de carboidratos Má absorção de ácidos biliares Pancreatite crônica Infecção gastrointestinal Doença inflamatória intestinal (DII) Colite microscópica Hipertiroidismo Tumor carcinoide Supercrescimento bacteriano do intestino delgado |
SII-múltiplos subtipos Intolerância alimentar Supercrescimento bacteriano do intestino delgado Neuropatia entérica ou miopatia Malignidade Efeitos colaterais dos medicamentos Condições ginecológicas (por exemplo, endometriose) Condições psicológicas (por exemplo, depressão, ansiedade) Outros distúrbios gastrointestinais funcionais (por exemplo, síndrome da dor abdominal funcional, dispepsia funcional) Doença do tecido conjuntivo |
Na prática clínica, pacientes que preenchem os critérios de Roma IV podem e devem ser diagnosticados com SII. Os critérios de Roma IV são atualmente os mais utilizados para o diagnóstico da SII e são aceitos por agências reguladoras e entidades de classes.
A história deve incluir o uso de medicamentos que podem causar sintomas semelhantes (tabela 1 e tabela 2). A avaliação do histórico familiar deve incluir a presença de doença inflamatória intestinal, câncer colorretal e doença celíaca.
O exame físico geralmente é normal em pacientes com SII. No entanto, os pacientes podem apresentar leve sensibilidade abdominal à palpação. Em pacientes com constipação, o toque retal pode ser útil para afastar a presença do anismo (contratura anal paradoxal).
Exames complementares no diagnóstico diferencial da síndrome do intestino irritável
O objetivo dos exames complementares laboratoriais e de imagem é excluir o diagnóstico de doença orgânica, uma vez que a SII não pode ser diagnosticada por exames complementares.
A combinação de critérios clínicos de Roma com hemograma completo e PCR normais é uma abordagem razoável para a avaliação da suspeita de SII. Essa abordagem diagnóstica limitada exclui doenças orgânicas em mais de 95% dos pacientes.
Pacientes refratários ao tratamento inicial com dieta e medicamentos, principalmente em jovens e mulheres, podem se beneficiar de exames para afastar as síndromes de intolerância/má absorção alimentar.
Avaliação adicional com base na presença de sinais de alarme “red flags”
Os sinais de alarme incluem:
Embora a presença de "sinais de alarme" possa indicar a necessidade de investigação diagnóstica adicional, estes pacientes não devem ser excluídos do diagnóstico da SII.
Sintomas noturnos (40%) e início acima dos 50 anos (32%) são os sinais de alarme mais comuns. Os sinais de alarme mais úteis para o diagnóstico de doença orgânica são a idade de início >50 anos e relato de sangue no papel higiênico. Os sinais de alarme têm boa especificidade para excluir doença orgânica e, portanto, na sua ausência o diagnóstico da SII é tranquilizador.
Em pacientes com sinais de alarme é recomendado avaliações adicionais para excluir outras doenças com quadro clínico semelhante. A avaliação diagnóstica é baseada na apresentação clínica e geralmente inclui a colonoscopia em todos os pacientes e exames de imagens (tomografia computadorizada ou ressonância magnética) em casos selecionados. Em pacientes com diarreia, é necessário a colonoscopia para avaliar a presença de DII e biópsias para excluir colite microscópica.
A história deve incluir o uso de medicamentos que podem causar sintomas semelhantes (tabela 1 e tabela 2). A avaliação do histórico familiar deve incluir a presença de doença inflamatória intestinal, câncer colorretal e doença celíaca.
O exame físico geralmente é normal em pacientes com SII. No entanto, os pacientes podem apresentar leve sensibilidade abdominal à palpação. Em pacientes com constipação, o toque retal pode ser útil para afastar a presença do anismo (contratura anal paradoxal).
Exames complementares no diagnóstico diferencial da síndrome do intestino irritável
O objetivo dos exames complementares laboratoriais e de imagem é excluir o diagnóstico de doença orgânica, uma vez que a SII não pode ser diagnosticada por exames complementares.
- Hemograma completo deve ser solicitado em todos os pacientes com suspeita de SII.
- Em pacientes com diarreia, deve-se solicitar o seguinte:
- Calprotectina fecal: calprotectina fecal acima de 50 mcg/g apresentou sensibilidade e especificidade combinadas para DII (doença inflamatória intestinal) de 81 e 87%, respectivamente);
- Exames de fezes para giárdia e outras parasitoses;
- Exames sorológico para doença celíaca;
- Proteína C reativa (PCR), somente se calprotectina fecal não puder ser realizada, porque o exame de PCR não é eficaz na triagem da DII.
- Glicemia de jejum, exames tireoidianos (T4 livre, TSH), e provas de função hepática (fosfatase alcalina, gamaGT, bilirrubinas, amilase, TGO e TGP) raramente são anormais em pacientes que apresentam sintomas de SII, e raramente levam a diagnósticos alternativos.
- Colonoscopia para rastreamento do câncer colorretal para pacientes com ≥45 anos.
- Manometria anorretal em pacientes com constipação grave refratária para descartar anismo (contratura anal paradoxal).
A combinação de critérios clínicos de Roma com hemograma completo e PCR normais é uma abordagem razoável para a avaliação da suspeita de SII. Essa abordagem diagnóstica limitada exclui doenças orgânicas em mais de 95% dos pacientes.
Pacientes refratários ao tratamento inicial com dieta e medicamentos, principalmente em jovens e mulheres, podem se beneficiar de exames para afastar as síndromes de intolerância/má absorção alimentar.
- Doença celíaca (DC) - pesquisa de anticorpos transglutaminase tecidual IgA.Má absorção de frutose (MF) - teste respiratório H2.
- Intolerância à lactose (ITL) - teste respiratório H2.
- Intolerância à histamina (IHT) - medição sérica da atividade sérica da diamina oxidase.
- Infecção pelo H. Pylori (IHP) - pesquisa de anticorpos IgA.
Avaliação adicional com base na presença de sinais de alarme “red flags”
Os sinais de alarme incluem:
- Idade de início após os 45 anos;
- Sangramento anorretal ou melena;
- Sintomas noturnos;
- Dor abdominal progressiva;
- Perda de peso inexplicável;
- Alterações laboratoriais (anemia por deficiência de ferro, proteína C reativa elevada e calprotectina fecal elevada);
- História familiar de DII, doença celíaca e câncer colorretal.
Embora a presença de "sinais de alarme" possa indicar a necessidade de investigação diagnóstica adicional, estes pacientes não devem ser excluídos do diagnóstico da SII.
Sintomas noturnos (40%) e início acima dos 50 anos (32%) são os sinais de alarme mais comuns. Os sinais de alarme mais úteis para o diagnóstico de doença orgânica são a idade de início >50 anos e relato de sangue no papel higiênico. Os sinais de alarme têm boa especificidade para excluir doença orgânica e, portanto, na sua ausência o diagnóstico da SII é tranquilizador.
Em pacientes com sinais de alarme é recomendado avaliações adicionais para excluir outras doenças com quadro clínico semelhante. A avaliação diagnóstica é baseada na apresentação clínica e geralmente inclui a colonoscopia em todos os pacientes e exames de imagens (tomografia computadorizada ou ressonância magnética) em casos selecionados. Em pacientes com diarreia, é necessário a colonoscopia para avaliar a presença de DII e biópsias para excluir colite microscópica.
O estabelecimento de uma relação médico-paciente e a continuidade dos cuidados pelo mesmo profissional são fundamentais para o manejo de todos os pacientes com síndrome do intestino irritável (SII).
Avaliar a gravidade e o impacto dos sintomas na qualidade de vida do paciente é importante, pois isso moldará a estratégia de manejo e tratamento. Alguns pacientes procuram atendimento por medo de ter uma doença com risco de vida, como o câncer de intestino. Esses pacientes podem encontrar alívio ao receber um diagnóstico positivo pelos critérios de Roma IV da SII e podem não necessitar de farmacoterapia. No entanto, pacientes com sintomas moderados a graves frequentemente necessitam de terapias farmacológicas e/ou psicológicas.
Em pacientes com sintomas leves e intermitentes que não comprometem a qualidade de vida, inicialmente é recomendado modificações no estilo de vida e na dieta, em vez de agentes farmacológicos específicos.
Em pacientes com sintomas leves a moderados que não respondem ao tratamento inicial e em pacientes com sintomas moderados a graves que afetam a qualidade de vida, é recomendado o tratamento farmacológico complementar.
Avaliar a gravidade e o impacto dos sintomas na qualidade de vida do paciente é importante, pois isso moldará a estratégia de manejo e tratamento. Alguns pacientes procuram atendimento por medo de ter uma doença com risco de vida, como o câncer de intestino. Esses pacientes podem encontrar alívio ao receber um diagnóstico positivo pelos critérios de Roma IV da SII e podem não necessitar de farmacoterapia. No entanto, pacientes com sintomas moderados a graves frequentemente necessitam de terapias farmacológicas e/ou psicológicas.
Em pacientes com sintomas leves e intermitentes que não comprometem a qualidade de vida, inicialmente é recomendado modificações no estilo de vida e na dieta, em vez de agentes farmacológicos específicos.
Em pacientes com sintomas leves a moderados que não respondem ao tratamento inicial e em pacientes com sintomas moderados a graves que afetam a qualidade de vida, é recomendado o tratamento farmacológico complementar.
Dieta saudável e equilibrada com um padrão regular de refeições (café da manhã, almoço e jantar com lanches conforme apropriado nos intervalos). Bom estilo de vida alimentar inclui separar um tempo para as refeições, sentar-se para comer, mastigar bem e não comer tarde da noite.
É sensato fornecer orientação sobre um bom estilo de vida alimentar e um padrão regular de refeições, considerando que 60% dos pacientes com SII relatam piora dos sintomas após as refeições, 20% dentro de 15 minutos e 93% em até três horas.
Embora a maioria dos pacientes não consiga controlar completamente os sintomas apenas com alterações na dieta, uma grande parte consegue minimizar as crises desencadeadas pelos alimentos. Os alimentos comumente responsáveis pelas crises da SII são aqueles ricos em gordura, alimentos picantes, álcool e bebidas cafeinadas.
O álcool (cerveja e o vinho) afeta a motilidade gastrointestinal, absorção e permeabilidade intestinal. A cafeína aumenta a secreção de ácido gástrico e a atividade motora colônica em indivíduos saudáveis e o café também aumentou rapidamente a atividade motora retossigmoide. Alimentos picantes contém capsaicina responsável pela aceleração do trânsito gastrointestinal causando dor abdominal e sensações de queimação em indivíduos saudáveis. A gordura estimula o reflexo gastrocólico e afeta a motilidade do intestino delgado.
Os gatilhos dietéticos são comuns, com até nove em cada 10 pacientes relatando que alimentos geram sintomas. Dois terços das pessoas com SII iniciam por conta própria restrições alimentares para melhorar os sintomas e, portanto, sempre devemos considerar a dieta no tratamento da SII.
Pacientes com SII podem se beneficiar da exclusão de alimentos produtores de gases e da dieta pobre em FODMAPs (oligossacarídeos, dissacarídeos, monossacarídeos e polióis fermentáveis); e em casos selecionados, eliminação de lactose e glúten (tabela 1). Não há evidências suficientes para apoiar o teste de alergia alimentar de rotina em pacientes com SII.
Recomenda-se evitar uma dieta muito rigorosa, porque é mais difícil de seguir, restringe muito o convívio social e o resultado não diferem muito da dieta baixa em FODMAPs e exclusão de produtores de gases.
A infecção por Helicobacter pylori pode potencialmente promover o desenvolvimento de SII e, diante de um caso de sintomas semelhantes aos da SII e dispepsia, deve ser acrescentada uma pesquisa de intolerância/má absorção e H. pylori.
Dieta de eliminação na síndrome do intestino irritável
A dieta de eliminação é uma abordagem dietética em que os indivíduos, devido ao alívio dos sintomas subjetivamente esperado, excluem voluntariamente determinados alimentos. Os sintomas pós-prandiais da SII estão frequentemente relacionados ao consumo de glúten/trigo ou leite/produtos lácteos. No entanto, os pacientes que realizam uma dieta de eliminação geralmente não são testados para doença celíaca ou intolerância à lactose.
Alguns indivíduos desenvolvem estratégias dietéticas personalizadas para a exclusão de fibras, ou iniciam intervenções dietéticas holísticas e/ou alimentos funcionais. Os efeitos a longo prazo da dieta de eliminação na saúde dependem do tipo de alimento excluído.
No geral, sabe-se, no entanto, que as dietas de eliminação influenciam a composição da microbiota intestinal e, subsequentemente, podem afetar os sintomas da SII. Uma dieta de eliminação em pacientes sem intolerância/má absorção alimentar causal conhecida e clinicamente diagnosticada não é útil como dieta no controle dos sintomas dentro do espectro da SII.
Avaliar a ingestão de álcool em relação aos sintomas (fezes amolecidas, dor abdominal, náuseas, indigestão e diarreia) para determinar se uma redução pode aliviar os sintomas e garantir que a ingestão esteja dentro dos limites de segurança recomendados.
Avaliar a ingestão de cafeína e, se relacionado aos sintomas (refluxo gastresofágico, dor abdominal e fezes amolecidas), considerar a redução da ingestão.
Avaliar a ingestão de alimentos picantes e pimenta e, se relacionado aos sintomas ((refluxo gastresofágico, dor abdominal e queimação oral), considerar a eliminação.
Uma diminuição na ingestão de gordura pode ser benéfica no alívio dos sintomas da SII, em particular dor abdominal relacionada à refeição e desconforto associado à hipersensibilidade visceral.
É sensato fornecer orientação sobre um bom estilo de vida alimentar e um padrão regular de refeições, considerando que 60% dos pacientes com SII relatam piora dos sintomas após as refeições, 20% dentro de 15 minutos e 93% em até três horas.
Embora a maioria dos pacientes não consiga controlar completamente os sintomas apenas com alterações na dieta, uma grande parte consegue minimizar as crises desencadeadas pelos alimentos. Os alimentos comumente responsáveis pelas crises da SII são aqueles ricos em gordura, alimentos picantes, álcool e bebidas cafeinadas.
O álcool (cerveja e o vinho) afeta a motilidade gastrointestinal, absorção e permeabilidade intestinal. A cafeína aumenta a secreção de ácido gástrico e a atividade motora colônica em indivíduos saudáveis e o café também aumentou rapidamente a atividade motora retossigmoide. Alimentos picantes contém capsaicina responsável pela aceleração do trânsito gastrointestinal causando dor abdominal e sensações de queimação em indivíduos saudáveis. A gordura estimula o reflexo gastrocólico e afeta a motilidade do intestino delgado.
Os gatilhos dietéticos são comuns, com até nove em cada 10 pacientes relatando que alimentos geram sintomas. Dois terços das pessoas com SII iniciam por conta própria restrições alimentares para melhorar os sintomas e, portanto, sempre devemos considerar a dieta no tratamento da SII.
Pacientes com SII podem se beneficiar da exclusão de alimentos produtores de gases e da dieta pobre em FODMAPs (oligossacarídeos, dissacarídeos, monossacarídeos e polióis fermentáveis); e em casos selecionados, eliminação de lactose e glúten (tabela 1). Não há evidências suficientes para apoiar o teste de alergia alimentar de rotina em pacientes com SII.
Recomenda-se evitar uma dieta muito rigorosa, porque é mais difícil de seguir, restringe muito o convívio social e o resultado não diferem muito da dieta baixa em FODMAPs e exclusão de produtores de gases.
A infecção por Helicobacter pylori pode potencialmente promover o desenvolvimento de SII e, diante de um caso de sintomas semelhantes aos da SII e dispepsia, deve ser acrescentada uma pesquisa de intolerância/má absorção e H. pylori.
Dieta de eliminação na síndrome do intestino irritável
A dieta de eliminação é uma abordagem dietética em que os indivíduos, devido ao alívio dos sintomas subjetivamente esperado, excluem voluntariamente determinados alimentos. Os sintomas pós-prandiais da SII estão frequentemente relacionados ao consumo de glúten/trigo ou leite/produtos lácteos. No entanto, os pacientes que realizam uma dieta de eliminação geralmente não são testados para doença celíaca ou intolerância à lactose.
Alguns indivíduos desenvolvem estratégias dietéticas personalizadas para a exclusão de fibras, ou iniciam intervenções dietéticas holísticas e/ou alimentos funcionais. Os efeitos a longo prazo da dieta de eliminação na saúde dependem do tipo de alimento excluído.
No geral, sabe-se, no entanto, que as dietas de eliminação influenciam a composição da microbiota intestinal e, subsequentemente, podem afetar os sintomas da SII. Uma dieta de eliminação em pacientes sem intolerância/má absorção alimentar causal conhecida e clinicamente diagnosticada não é útil como dieta no controle dos sintomas dentro do espectro da SII.
Avaliar a ingestão de álcool em relação aos sintomas (fezes amolecidas, dor abdominal, náuseas, indigestão e diarreia) para determinar se uma redução pode aliviar os sintomas e garantir que a ingestão esteja dentro dos limites de segurança recomendados.
Avaliar a ingestão de cafeína e, se relacionado aos sintomas (refluxo gastresofágico, dor abdominal e fezes amolecidas), considerar a redução da ingestão.
Avaliar a ingestão de alimentos picantes e pimenta e, se relacionado aos sintomas ((refluxo gastresofágico, dor abdominal e queimação oral), considerar a eliminação.
Uma diminuição na ingestão de gordura pode ser benéfica no alívio dos sintomas da SII, em particular dor abdominal relacionada à refeição e desconforto associado à hipersensibilidade visceral.
Os pacientes com SII devem ser aconselhados a excluir alimentos que aumentam a produção de gases (por exemplo, feijão, cebola, aipo, cenoura, passas, bananas, damascos, ameixas secas, couve de Bruxelas, gérmen de trigo, pretzels e bagels), álcool e cafeína. A hipersensibilidade visceral subjacente pode explicar o desconforto exagerado experimentado por pacientes com SII com o consumo de alimentos produtores de gases.
Modificação da dieta e do estilo de vida – A abordagem para o tratamento do inchaço e distensão abdominal é semelhante à usada em pacientes com SII.
Modificação da dieta e do estilo de vida – A abordagem para o tratamento do inchaço e distensão abdominal é semelhante à usada em pacientes com SII.
- Dieta saudável e equilibrada com um padrão regular de refeições (café da manhã, almoço e jantar com lanches conforme apropriado nos intervalos). Bom estilo de vida alimentar inclui separar um tempo para as refeições, sentar-se para comer, mastigar bem e não comer tarde da noite;
- Procure não falar muito durante as refeições para diminuir o volume de ar deglutido;
- Fique assentado ou em pé após as refeições, por alguns minutos, para facilitar a eructação (arroto);
- Exercícios leves como caminhadas é sempre saudável, pois estimula os movimentos intestinais.
- Evite o uso de roupas apertadas.
- Evite a salivação excessiva provocada pelos chicletes, doces, balas e cigarro;
Leite e produtos lácteos |
Leite, sorvete, queijo (pode ou não estar relacionado à lactose). |
Vegetais |
Brócolis, couve-flor, couve-de-bruxelas, cebola, alho-poró, nabo, aipo, rabanete, aspargo, repolho, couve-rábano, pepino, batata, nabo. |
Frutas |
Ameixas, damascos, maçãs, peras, pêssegos, passas, bananas. |
Grãos integrais |
Trigo e aveia, bagels, gérmen de trigo e cereais. |
Legumes |
Feijão, ervilha, feijão cozido, soja. |
Comidas gordurosas |
Alimentos fritos. |
Líquidos |
Bebidas carbonatadas (refrigerantes), cerveja, medicamentos carbonatados. |
Diversos |
Gomas de mascar e adoçantes artificiais (sorbitol e frutose). |
Prefira alimentos ricos em fibras e beba bastante líquido, pois isso facilita o trânsito intestinal. A constipação retarda o trânsito provocando maior produção de gases. Preste atenção, no seu caso específico, aos alimentos que podem estar associados a gases. Algumas pessoas reagem mal à farinha (pães, massas etc.), batata doce, cebola, rabanete,
VEJA MAIS! BAIXE A DIETA COMPLETA!
VEJA MAIS! BAIXE A DIETA COMPLETA!
Dieta sem lactose na síndrome do intestino irritável (SII)
Pacientes com conhecida intolerância à lactose devem restringir ou eliminar a lactose da dieta de acordo o nível de intolerância. Recomenda-se também uma dieta sem lactose para os pacientes que se queixam de inchaço abdominal persistente, mesmo com a dieta de exclusão de alimentos produtores de gases.
Como a melhora dos sintomas não implica necessariamente má digestão da lactose, o diagnóstico de intolerância à lactose deve ser confirmado com testes respiratórios ou oral de tolerância a lactose. Indivíduos que não apresentam evidências de intolerância à lactose nos exames, mas que apresentam sintomas com a ingestão de leite, podem ter intolerância a outros componentes do leite (por exemplo, proteína do leite de vaca) e podem tolerar leite de outros mamíferos ou de soja.
Embora a incidência de má absorção de lactose não seja maior em pacientes com SII, pacientes com SII e intolerância à lactose apresentam uma resposta exagerada dos sintomas à ingestão de lactose. Pacientes com intolerância à lactose não diagnosticada podem ter melhora clínica duradoura quando submetidos a uma dieta restrita à lactose.
Assim, em indivíduos com SII, a restrição de lactose isolada só pode proporcionar benefícios marginais aos sintomas. Portanto, a restrição de lactose, em pacientes em intolerância, é geralmente considerada como parte de uma dieta baixa em FODMAP (ver seção sobre carboidratos fermentáveis abaixo). Se os indivíduos desejam seguir uma dieta sem leite, eles devem ser informados de que não há evidências de alta qualidade para que isso melhore seus sintomas da SII.
Como a melhora dos sintomas não implica necessariamente má digestão da lactose, o diagnóstico de intolerância à lactose deve ser confirmado com testes respiratórios ou oral de tolerância a lactose. Indivíduos que não apresentam evidências de intolerância à lactose nos exames, mas que apresentam sintomas com a ingestão de leite, podem ter intolerância a outros componentes do leite (por exemplo, proteína do leite de vaca) e podem tolerar leite de outros mamíferos ou de soja.
Embora a incidência de má absorção de lactose não seja maior em pacientes com SII, pacientes com SII e intolerância à lactose apresentam uma resposta exagerada dos sintomas à ingestão de lactose. Pacientes com intolerância à lactose não diagnosticada podem ter melhora clínica duradoura quando submetidos a uma dieta restrita à lactose.
Assim, em indivíduos com SII, a restrição de lactose isolada só pode proporcionar benefícios marginais aos sintomas. Portanto, a restrição de lactose, em pacientes em intolerância, é geralmente considerada como parte de uma dieta baixa em FODMAP (ver seção sobre carboidratos fermentáveis abaixo). Se os indivíduos desejam seguir uma dieta sem leite, eles devem ser informados de que não há evidências de alta qualidade para que isso melhore seus sintomas da SII.
Recomenda-se uma dieta com baixo teor de FODMAPs (oligo, di e monossacarídeos e polióis fermentáveis) em pacientes com SII com inchaço e/ou dor abdominal, apesar da exclusão de alimentos produtores de gases. VEJA MAIS! BAIXE A DIETA COMPLETA!
A evidência de alta qualidade para SII foi para a dieta baixa em FODMAPs, subtipos SII-D e SII-M. As evidências se acumularam rapidamente nos últimos anos e estão começando a se tornar reconhecida internacionalmente.
Os FODMAPs são moléculas osmoticamente ativas não absorvidas que aumentam o conteúdo de líquido luminal intestinal. Posteriormente, eles entram no intestino grosso sem serem digeridos, onde são fermentados rapidamente por bactérias do cólon aumentado a produção de gases, resultando nos sintomas de inchaço e dor abdominal da SII.
Uma dieta baixa em FODMAPs envolve a eliminação de um número maior de alimentos que não seriam excluídos na dieta que apenas evita alimentos produtores de gases.
A adesão à dieta pobre em FODMAPs é difícil, envolve custos elevados e um nutricionista é essencial para alcançar a adequação nutricional e influenciar os resultados do tratamento.
Alguns estudos recomendam a dieta baixa em FODMAPs para todos os pacientes com SII. Porém, devido à falta de personalização nos estudos realizados, a dieta com baixo teor de FODMAPs não parece ser adequada como uma dieta de longo prazo ou padrão para o tratamento dos sintomas do espectro da SII.
Uma dieta baixa em FODMAPs por 3 a 6 semanas é eficaz no tratamento da SII quando entregue por um nutricionista com experiência em educação FODMAPs. A adesão bem-sucedida e o manejo dos sintomas são alcançados pelo fornecimento de informações verbais e escritas detalhadas sobre a prevenção de alimentos ricos em FODMAPs e pela inclusão de alternativas adequadas para garantir uma dieta nutricionalmente adequada.
A dieta baixa em FODMAPs consiste em eliminar inicialmente os FODMAPs da dieta por 3 a 6 semanas. Do ponto de vista da segurança, as evidências mostram que uma dieta baixa em FODMAPs altera a microbiota intestinal e reduz a ingestão de cálcio no curto prazo. Portanto, após melhora satisfatória dos sintomas (3-6 semanas) é necessária a reintrodução de FODMAPs individuais de acordo com a tolerância pessoal.
A reintrodução do FODMAP verifica a eficácia do tratamento e a tolerância individual a alimentos específicos, ao mesmo tempo que aumenta a variedade dietética e permite a autogestão a longo prazo.
A lactose e a frutose estão entre esses carboidratos mal absorvidos e rapidamente fermentados, que se acredita desencadearem sintomas gastrointestinais.
A evidência de alta qualidade para SII foi para a dieta baixa em FODMAPs, subtipos SII-D e SII-M. As evidências se acumularam rapidamente nos últimos anos e estão começando a se tornar reconhecida internacionalmente.
Os FODMAPs são moléculas osmoticamente ativas não absorvidas que aumentam o conteúdo de líquido luminal intestinal. Posteriormente, eles entram no intestino grosso sem serem digeridos, onde são fermentados rapidamente por bactérias do cólon aumentado a produção de gases, resultando nos sintomas de inchaço e dor abdominal da SII.
Uma dieta baixa em FODMAPs envolve a eliminação de um número maior de alimentos que não seriam excluídos na dieta que apenas evita alimentos produtores de gases.
A adesão à dieta pobre em FODMAPs é difícil, envolve custos elevados e um nutricionista é essencial para alcançar a adequação nutricional e influenciar os resultados do tratamento.
Alguns estudos recomendam a dieta baixa em FODMAPs para todos os pacientes com SII. Porém, devido à falta de personalização nos estudos realizados, a dieta com baixo teor de FODMAPs não parece ser adequada como uma dieta de longo prazo ou padrão para o tratamento dos sintomas do espectro da SII.
Uma dieta baixa em FODMAPs por 3 a 6 semanas é eficaz no tratamento da SII quando entregue por um nutricionista com experiência em educação FODMAPs. A adesão bem-sucedida e o manejo dos sintomas são alcançados pelo fornecimento de informações verbais e escritas detalhadas sobre a prevenção de alimentos ricos em FODMAPs e pela inclusão de alternativas adequadas para garantir uma dieta nutricionalmente adequada.
A dieta baixa em FODMAPs consiste em eliminar inicialmente os FODMAPs da dieta por 3 a 6 semanas. Do ponto de vista da segurança, as evidências mostram que uma dieta baixa em FODMAPs altera a microbiota intestinal e reduz a ingestão de cálcio no curto prazo. Portanto, após melhora satisfatória dos sintomas (3-6 semanas) é necessária a reintrodução de FODMAPs individuais de acordo com a tolerância pessoal.
A reintrodução do FODMAP verifica a eficácia do tratamento e a tolerância individual a alimentos específicos, ao mesmo tempo que aumenta a variedade dietética e permite a autogestão a longo prazo.
A lactose e a frutose estão entre esses carboidratos mal absorvidos e rapidamente fermentados, que se acredita desencadearem sintomas gastrointestinais.
Sigla |
Palavra que corresponde à letra na sigla |
Compostos nesta categoria |
Alimentos proibidos por FODMAPs |
Alimentos permitidos por FODMAPs |
F |
Fermentáveis |
Value |
||
O |
Oligossacarídeos |
Frutanos, galacto-oligossacarídeos |
Trigo, cevada, centeio, legumes Pão e produtos de panificação (ddi), biscoitos (ddi), croissants, massas, farinha de trigo, kamut, cuscuz, muesli (ddi) |
Todas as bebidas vegetais (ddi), cenoura, abóbora, alcachofra, batata, alho, alho-poró, feijão verde, pimentão vermelho, cebola, espinafre, tomate, berinjela, broto de bambu, beterraba vermelha, chicória, aspargos, couve-flor, couve de Bruxelas, brócolis, rabanete, pimenta, nabo, erva-doce, ervilhas, produtos de soja, grão de bico, lentilhas, Amêndoas, avelãs, nozes, pinhões arroz, aveia, quinoa, painço, amaranto, trigo sarraceno, pão sem glúten e cereais (ddi), farinha de batata |
D |
Dissacarídeos |
Lactose |
Leite e derivados, creme, sorvete (ddi) e iogurte |
Sorvete (ddi) |
M |
Monossacarídeos |
"Frutose livre" (frutose em excesso de glicose) |
Maçã, pera, melancia, manga, damasco, abacate, cereja, pêssego, ameixa, caqui, lichia, sucos de frutas Frutas secas: pistache, castanha de caju |
Sorvetes de frutas, banana, mirtilo, morango, framboesa, uva, melão, toranja, kiwi, laranja, limão, lima, abacaxi, maracujá |
A |
And (e) |
Value |
Value |
Value |
P |
Polióis |
Sorbitol, manitol, maltitol e xilitol |
Nectarinas, melancia, cogumelos, goma de mascar e produtos adoçados artificialmente |
Açúcar branco, açúcar mascavo, xarope de bordo |
Legenda da tabela: ddi, dependendo dos ingredientes.
Dieta sem glúten na síndrome do intestino irritável (SII)
A sensibilidade ao glúten não celíaca (SGNC) é sugerida como um mecanismo subjacente para a geração dos sintomas em pacientes com SII, mas evidências para apoiar a eliminação do glúten em pacientes com SII são conflitantes. No entanto, as diretrizes sugerem testes sorológicos para descartar doença celíaca em pacientes com SII.
É possível que a melhora sintomática associada a uma dieta sem glúten não seja causada pela remoção da proteína do glúten, mas pela redução de frutanos (compostos orgânicos, classificados como açúcares-álcoois, polímeros da Frutose sintetizados a partir da sacarose, que ocorrem na natureza em vegetais).
A maioria dos pacientes com SGNC são autodiagnosticados e eles voluntariamente, sem diagnóstico médico de qualquer distúrbio relacionado ao trigo, decidem mudar seu comportamento alimentar para uma dieta sem glúten.
No entanto, os produtos sem glúten não só são consideravelmente mais caros, como também apresentam menor teor de proteína e fibras, maior teor de gordura e maior teor de sal em comparação com produtos que contêm glúten.
Evidências de baixa qualidade sugerem que uma ingestão baixa de glúten em comparação com uma dieta rica em glúten pode estar associada a um risco aumentado de diabetes mellitus tipo 2. No que diz respeito a outros fatores de risco cardiovascular, a diferença entre uma dieta sem glúten e uma dieta normal permanece obscura.
Portanto, com base nas evidências científicas disponíveis, o consumo de trigo é geralmente considerado seguro e saudável. Além disso, não existem evidências que sustentem que pessoas saudáveis beneficiariam de uma dieta sem glúten.
A sensibilidade ao glúten não celíaca (SGNC) é sugerida como um mecanismo subjacente para a geração dos sintomas em pacientes com SII, mas evidências para apoiar a eliminação do glúten em pacientes com SII são conflitantes. No entanto, as diretrizes sugerem testes sorológicos para descartar doença celíaca em pacientes com SII.
É possível que a melhora sintomática associada a uma dieta sem glúten não seja causada pela remoção da proteína do glúten, mas pela redução de frutanos (compostos orgânicos, classificados como açúcares-álcoois, polímeros da Frutose sintetizados a partir da sacarose, que ocorrem na natureza em vegetais).
A maioria dos pacientes com SGNC são autodiagnosticados e eles voluntariamente, sem diagnóstico médico de qualquer distúrbio relacionado ao trigo, decidem mudar seu comportamento alimentar para uma dieta sem glúten.
No entanto, os produtos sem glúten não só são consideravelmente mais caros, como também apresentam menor teor de proteína e fibras, maior teor de gordura e maior teor de sal em comparação com produtos que contêm glúten.
Evidências de baixa qualidade sugerem que uma ingestão baixa de glúten em comparação com uma dieta rica em glúten pode estar associada a um risco aumentado de diabetes mellitus tipo 2. No que diz respeito a outros fatores de risco cardiovascular, a diferença entre uma dieta sem glúten e uma dieta normal permanece obscura.
Portanto, com base nas evidências científicas disponíveis, o consumo de trigo é geralmente considerado seguro e saudável. Além disso, não existem evidências que sustentem que pessoas saudáveis beneficiariam de uma dieta sem glúten.
Dietas ricas em fibra dietética estão associadas a uma menor incidência de doenças cardiovasculares, eventos coronarianos, acidente vascular cerebral, diabetes tipo 2 e câncer colorretal. A fibra dietética tem um efeito benéfico na microbiota gastrointestinal e nos subprodutos da fermentação.
É recomendado que a ingestão de fibra dietética deve ser cerca de 25 g ao dia para mulheres e 30 g ao dia para homens. A alta ingestão de fibra dietética tem sido associada à geração de sintomas na SII, e, portanto, os fatores de risco e benefícios de alimentos específicos ricos em fibras alimentares precisam ser levados em consideração.
Considere o perfil dos sintomas do paciente antes da avaliação da ingestão de fibras alimentares para determinar se a ingestão atual é ideal para esse indivíduo. Verifique a ingestão de fibras alimentares de todas as fontes potenciais (cereais, grãos, frutas, vegetais, nozes, sementes e leguminosas).
Se for aplicável o aumento da ingestão de fibras, incentivar uma variedade de alimentos ricos em fibras (por exemplo, aveia e farelo de aveia, arroz integral, farelo de arroz, pão integral/de sementes/de centeio, massa integral, cuscuz integral, batatas com casca e quinoa). Uma grande variedade é importante levando em conta quaisquer outras restrições alimentares.
O papel da fibra em pacientes com SII é controverso, mas, dada a ausência de efeitos colaterais graves e potencial benefício, as fibras devem ser consideradas.
Recomendo iniciar psyllium e/ou semente de linhaça, principalmente em pacientes com SII cujo sintoma predominante seja a constipação. Como alguns pacientes podem apresentar aumento do inchaço e gases abdominal, sugiro uma dose inicial de metade a uma colher de sopa por dia. A dose deve ser aumentada lentamente com base na resposta ao tratamento. VEJA DETALHES DE COMO CONSUMIR O PSYLLIUM (VEJA NESTA PÁGINA) E A SEMENTE DE LINHAÇA (VEJA NESTA PÁGINA).
É recomendado que a ingestão de fibra dietética deve ser cerca de 25 g ao dia para mulheres e 30 g ao dia para homens. A alta ingestão de fibra dietética tem sido associada à geração de sintomas na SII, e, portanto, os fatores de risco e benefícios de alimentos específicos ricos em fibras alimentares precisam ser levados em consideração.
Considere o perfil dos sintomas do paciente antes da avaliação da ingestão de fibras alimentares para determinar se a ingestão atual é ideal para esse indivíduo. Verifique a ingestão de fibras alimentares de todas as fontes potenciais (cereais, grãos, frutas, vegetais, nozes, sementes e leguminosas).
Se for aplicável o aumento da ingestão de fibras, incentivar uma variedade de alimentos ricos em fibras (por exemplo, aveia e farelo de aveia, arroz integral, farelo de arroz, pão integral/de sementes/de centeio, massa integral, cuscuz integral, batatas com casca e quinoa). Uma grande variedade é importante levando em conta quaisquer outras restrições alimentares.
O papel da fibra em pacientes com SII é controverso, mas, dada a ausência de efeitos colaterais graves e potencial benefício, as fibras devem ser consideradas.
Recomendo iniciar psyllium e/ou semente de linhaça, principalmente em pacientes com SII cujo sintoma predominante seja a constipação. Como alguns pacientes podem apresentar aumento do inchaço e gases abdominal, sugiro uma dose inicial de metade a uma colher de sopa por dia. A dose deve ser aumentada lentamente com base na resposta ao tratamento. VEJA DETALHES DE COMO CONSUMIR O PSYLLIUM (VEJA NESTA PÁGINA) E A SEMENTE DE LINHAÇA (VEJA NESTA PÁGINA).
O PEG 4000 é um laxante osmótico biologicamente inerte e não absorvível, é uma opção de primeira linha altamente eficaz e bem tolerada para o tratamento da constipação idiopática/funcional crônica em adultos.
O PEG 4000 é mais eficaz do que a lactulose no aumento da frequência evacuatória e consistência das fezes e está associado a incidência menor de náuseas, vômitos e flatulências. Comparações com outros laxantes osmóticos e formadores de massa são limitados, mas sabe-se que o PEG 4000 é pelo menos tão ou mais eficaz do que o psyllium e o hidróxido de magnésio no tratamento da constipação crônica. As diretrizes atuais para o tratamento clínico da constipação recomendam o uso dos laxantes osmóticos (macrogol 3350 ou PEG 4000 ou lactulose) e formadores de massa como primeira linha.
Vantagens do PEG 4.000 (polietilenoglicol) sem eletrólitos
• Laxante osmótico biologicamente inerte e não absorvível.
• As respostas ao tratamento são duráveis sem provocar tolerância, isto é, sem a necessidade do aumento progressivo da dose para manter o efeito desejado.
• Igualmente eficaz é o macrogol 3350 associado a eletrólitos, que por sua vez são muito mais eficazes do que a lactulose.
• Melhor tolerado, com menos náuseas, vômitos e flatulências que a lactulose.
• Têm pouco efeito na composição microbiana intestinal.
• O sabor do PEG 4000 é preferido quando comparado ao macrogol 3350 com eletrólitos.
• O PEG 4000 pó para solução oral manipulado não contém eletrólitos, ao contrário das várias outras formulações de macrogol 3350 que contém sulfato de sódio, potássio e cloreto. A adição de eletrólitos não é necessária, pois o PEG 4000 não está associado a perdas entéricas desses eletrólitos.
• Como o PEG 4000 não contém sódio, pode ser usado por pacientes em dieta pobre em sódio. Além disso, como o PEG 4000 também não contém sacarose, pode ser usado por pacientes com diabetes.
O tratamento da constipação crônica idiopática ou funcional deve incluir mudanças na dieta e no estilo de vida (por exemplo, ingestão adequada de líquidos, aumento da fibra alimentar, exercícios físicos regulares e bons hábitos evacuatórios) e quando essas medidas são insuficiente, recomenda-se o tratamento adjuvante com um laxante, geralmente um agente osmótico e/ou formador de massa.
Os laxantes osmóticos, pela sua capacidade de reter água no interior do intestino, aumenta o volume das fezes e as torna amolecidas, acelera o trânsito intestinal, aumenta a frequência das evacuações e facilita a evacuação.
Dose recomendada do PEG 4000 (manipulado) ou do macrogol 3350 (industrializado) em adultos
• Um envelope (sache) de 17,5 g por dia. O ajuste de dosagem é baseado na resposta clínica e varia de um envelope em dias alternados até o máximo de dois envelopes por dia.
• De preferência em dose única pela manhã.
• Dissolver o conteúdo do(s) envelope(s) em um copo de água (200 mL) e beber imediatamente.
• Os efeitos do PEG 4000 ou macrogol 3350 ocorre em 24 a 48 horas.
• Deve ser usado como tratamento temporário junto com as medidas comportamentais, mas antes de iniciar o tratamento, uma possível causa orgânica para a constipação deve ser excluída.
• O PEG 4000 pode ser usado em pacientes diabéticos ou intolerantes a lactose ou em dieta com baixo teor de sódio e também em mulheres grávidas ou amamentando.
Contra indicações ao uso do macrogol 4000 ou 3350
• Hipersensibilidade ao macrogol (polietilenoglicol) ou a qualquer outro componente.
• Doença inflamatória intestinal grave existente (por exemplo, colite ulcerosa ou doença de Crohn); megacólon tóxico; presença ou risco de perfurações digestivas; íleo ou suspeita de estenose sintomática ou obstrução intestinal; doenças abdominais dolorosas de causa desconhecida.
Precauções especiais ao uso do macrogol 4000 ou 3350
• O uso do PEG 4000 ou macrogol 3350 poderia ter efeitos potencialmente sensíveis na absorção intestinal de alguns medicamentos, particularmente aqueles com um índice terapêutico estreito (comparação entre a quantidade de um agente terapêutico necessária para causar um efeito terapêutico desejado e a quantidade que causa efeitos tóxicos) ou meia-vida curta (por exemplo, digoxina, antiepiléticos, anticoagulantes de cumarinas e agentes imunossupressores). Diminuindo a absorção, por sua vez, pode levar à diminuição da eficácia.
• Reações alérgicas (por exemplo, choque anafilático, angioedema, urticária, erupção cutânea, prurido, eritema).
➤ Se ocorrer uma reação alérgica, pare de tomar macrogol e procure ajuda médica imediatamente.
➤ O dióxido de enxofre (presente no aroma da toranja laranja) raramente pode causar reações de hipersensibilidade grave e broncoespasmo
• Devido ao risco de diarreia durante o tratamento recomenda-se monitorar de pertos os pacientes com
• Insuficiência renal ou hepática, em uso de diurético, em idoso ou naqueles propensos a distúrbios eletrolíticos (níveis baixos de sódio ou potássio no sangue). Considere monitorar eletrólitos nesses pacientes
O PEG 4000 é mais eficaz do que a lactulose no aumento da frequência evacuatória e consistência das fezes e está associado a incidência menor de náuseas, vômitos e flatulências. Comparações com outros laxantes osmóticos e formadores de massa são limitados, mas sabe-se que o PEG 4000 é pelo menos tão ou mais eficaz do que o psyllium e o hidróxido de magnésio no tratamento da constipação crônica. As diretrizes atuais para o tratamento clínico da constipação recomendam o uso dos laxantes osmóticos (macrogol 3350 ou PEG 4000 ou lactulose) e formadores de massa como primeira linha.
Vantagens do PEG 4.000 (polietilenoglicol) sem eletrólitos
• Laxante osmótico biologicamente inerte e não absorvível.
• As respostas ao tratamento são duráveis sem provocar tolerância, isto é, sem a necessidade do aumento progressivo da dose para manter o efeito desejado.
• Igualmente eficaz é o macrogol 3350 associado a eletrólitos, que por sua vez são muito mais eficazes do que a lactulose.
• Melhor tolerado, com menos náuseas, vômitos e flatulências que a lactulose.
• Têm pouco efeito na composição microbiana intestinal.
• O sabor do PEG 4000 é preferido quando comparado ao macrogol 3350 com eletrólitos.
• O PEG 4000 pó para solução oral manipulado não contém eletrólitos, ao contrário das várias outras formulações de macrogol 3350 que contém sulfato de sódio, potássio e cloreto. A adição de eletrólitos não é necessária, pois o PEG 4000 não está associado a perdas entéricas desses eletrólitos.
• Como o PEG 4000 não contém sódio, pode ser usado por pacientes em dieta pobre em sódio. Além disso, como o PEG 4000 também não contém sacarose, pode ser usado por pacientes com diabetes.
O tratamento da constipação crônica idiopática ou funcional deve incluir mudanças na dieta e no estilo de vida (por exemplo, ingestão adequada de líquidos, aumento da fibra alimentar, exercícios físicos regulares e bons hábitos evacuatórios) e quando essas medidas são insuficiente, recomenda-se o tratamento adjuvante com um laxante, geralmente um agente osmótico e/ou formador de massa.
Os laxantes osmóticos, pela sua capacidade de reter água no interior do intestino, aumenta o volume das fezes e as torna amolecidas, acelera o trânsito intestinal, aumenta a frequência das evacuações e facilita a evacuação.
Dose recomendada do PEG 4000 (manipulado) ou do macrogol 3350 (industrializado) em adultos
• Um envelope (sache) de 17,5 g por dia. O ajuste de dosagem é baseado na resposta clínica e varia de um envelope em dias alternados até o máximo de dois envelopes por dia.
• De preferência em dose única pela manhã.
• Dissolver o conteúdo do(s) envelope(s) em um copo de água (200 mL) e beber imediatamente.
• Os efeitos do PEG 4000 ou macrogol 3350 ocorre em 24 a 48 horas.
• Deve ser usado como tratamento temporário junto com as medidas comportamentais, mas antes de iniciar o tratamento, uma possível causa orgânica para a constipação deve ser excluída.
• O PEG 4000 pode ser usado em pacientes diabéticos ou intolerantes a lactose ou em dieta com baixo teor de sódio e também em mulheres grávidas ou amamentando.
Contra indicações ao uso do macrogol 4000 ou 3350
• Hipersensibilidade ao macrogol (polietilenoglicol) ou a qualquer outro componente.
• Doença inflamatória intestinal grave existente (por exemplo, colite ulcerosa ou doença de Crohn); megacólon tóxico; presença ou risco de perfurações digestivas; íleo ou suspeita de estenose sintomática ou obstrução intestinal; doenças abdominais dolorosas de causa desconhecida.
Precauções especiais ao uso do macrogol 4000 ou 3350
• O uso do PEG 4000 ou macrogol 3350 poderia ter efeitos potencialmente sensíveis na absorção intestinal de alguns medicamentos, particularmente aqueles com um índice terapêutico estreito (comparação entre a quantidade de um agente terapêutico necessária para causar um efeito terapêutico desejado e a quantidade que causa efeitos tóxicos) ou meia-vida curta (por exemplo, digoxina, antiepiléticos, anticoagulantes de cumarinas e agentes imunossupressores). Diminuindo a absorção, por sua vez, pode levar à diminuição da eficácia.
• Reações alérgicas (por exemplo, choque anafilático, angioedema, urticária, erupção cutânea, prurido, eritema).
➤ Se ocorrer uma reação alérgica, pare de tomar macrogol e procure ajuda médica imediatamente.
➤ O dióxido de enxofre (presente no aroma da toranja laranja) raramente pode causar reações de hipersensibilidade grave e broncoespasmo
• Devido ao risco de diarreia durante o tratamento recomenda-se monitorar de pertos os pacientes com
• Insuficiência renal ou hepática, em uso de diurético, em idoso ou naqueles propensos a distúrbios eletrolíticos (níveis baixos de sódio ou potássio no sangue). Considere monitorar eletrólitos nesses pacientes
A atividade física aeróbica deve ser recomendada em pacientes com SII, com um benefício potencial em relação aos sintomas da SII e aos benefícios gerais do exercício para a saúde como um todo.
Foi demonstrado que a atividade física aeróbica é essencial para manter uma boa saúde física e mental e pode prevenir sintomas gastrointestinais em indivíduos saudáveis. Com base em pesquisas existentes, regimes de exercícios adequadamente adaptados possam ter efeitos positivos no curso da doença entre indivíduos com SII.
Recomenda-se uma atividade física aeróbica moderada a intensa de 30 a 60 minutos, 3 a 5 vezes por semana. Os pacientes com SII podem apresentar melhora do desconforto abdominal e dos sintomas extracolônicos após 12 semanas de atividade física aeróbica.
Está demonstrado que a atividade física aeróbica reduz a dor abdominal, ajuda a controlar o trânsito colônico, facilita a evacuação e alivia a ansiedade. A caminhada é uma das formas mais populares de atividade física aeróbica de intensidade moderada devido à sua acessibilidade e requisitos mínimos. Oferece uma ampla gama de benefícios à saúde cardiovascular e gastrointestinal.
Atividade física aeróbica de intensidade moderada, como a caminhada, proporciona benefícios semelhantes à corrida de alta intensidade na redução do risco de hipertensão, hipercolesterolemia e diabetes.
As atividades esportivas podem ajudar a reduzir a ansiedade e o estresse, distraindo os indivíduos das preocupações e liberando a tensão emocional.
Foi demonstrado que a atividade física aeróbica é essencial para manter uma boa saúde física e mental e pode prevenir sintomas gastrointestinais em indivíduos saudáveis. Com base em pesquisas existentes, regimes de exercícios adequadamente adaptados possam ter efeitos positivos no curso da doença entre indivíduos com SII.
Recomenda-se uma atividade física aeróbica moderada a intensa de 30 a 60 minutos, 3 a 5 vezes por semana. Os pacientes com SII podem apresentar melhora do desconforto abdominal e dos sintomas extracolônicos após 12 semanas de atividade física aeróbica.
Está demonstrado que a atividade física aeróbica reduz a dor abdominal, ajuda a controlar o trânsito colônico, facilita a evacuação e alivia a ansiedade. A caminhada é uma das formas mais populares de atividade física aeróbica de intensidade moderada devido à sua acessibilidade e requisitos mínimos. Oferece uma ampla gama de benefícios à saúde cardiovascular e gastrointestinal.
Atividade física aeróbica de intensidade moderada, como a caminhada, proporciona benefícios semelhantes à corrida de alta intensidade na redução do risco de hipertensão, hipercolesterolemia e diabetes.
As atividades esportivas podem ajudar a reduzir a ansiedade e o estresse, distraindo os indivíduos das preocupações e liberando a tensão emocional.
Os probióticos não são recomendados rotineiramente nos pacientes com SII. Embora tenham sido associados a uma melhora nos sintomas, a magnitude do benefício e as espécies mais eficazes são incertas.
Os probióticos têm potencial em impactar positivamente na condução do tratamento, mas os benefícios no tratamento da SII não estão comprovados. É possível que algum benefício clinicamente importante possa ser alcançado em certos subgrupos de pacientes, particularmente naqueles em que a diarreia predomina. Como na doença inflamatória intestinal, a abordagem pode estar na correção da microbiota alterada, em vez de usar uma preparação probiótica genérica em todos os pacientes.
Existem muitos produtos probióticos disponíveis em diferentes doses e cepas bacterianas variáveis. Indivíduos com SII que optam por experimentar probióticos devem estar cientes de que alguns produtos contêm outros ingredientes que podem aumentar os sintomas da SII (por exemplo, fibra dietética: aveia; FODMAPs: FOS, inulina, lactose, frutose, sorbitol e xilitol). Se um indivíduo usa um probiótico durante 4 semanas e apresenta melhora dos sintomas, ele pode continuar usando, mas os efeitos a longo prazo não são conhecidos.
Os probióticos têm potencial em impactar positivamente na condução do tratamento, mas os benefícios no tratamento da SII não estão comprovados. É possível que algum benefício clinicamente importante possa ser alcançado em certos subgrupos de pacientes, particularmente naqueles em que a diarreia predomina. Como na doença inflamatória intestinal, a abordagem pode estar na correção da microbiota alterada, em vez de usar uma preparação probiótica genérica em todos os pacientes.
Existem muitos produtos probióticos disponíveis em diferentes doses e cepas bacterianas variáveis. Indivíduos com SII que optam por experimentar probióticos devem estar cientes de que alguns produtos contêm outros ingredientes que podem aumentar os sintomas da SII (por exemplo, fibra dietética: aveia; FODMAPs: FOS, inulina, lactose, frutose, sorbitol e xilitol). Se um indivíduo usa um probiótico durante 4 semanas e apresenta melhora dos sintomas, ele pode continuar usando, mas os efeitos a longo prazo não são conhecidos.
O tratamento com medicamentos é recomendado para os pacientes com síndrome do intestino irritável (SII) com sintomas leves a moderados que não respondem ao tratamento inicial e em pacientes com sintomas moderados a graves que afetam a qualidade de vida. Como a SII geralmente se apresenta com vários sintomas, o tratamento deve ser baseado no sintoma predominante. As consultas de controle devem ser realizadas em 2 a 4 semanas. Laxantes, antidiarreicos e antiespasmódicos são usados como terapias de primeira linha na SII.
Ensaios randomizados avaliando agentes farmacológicos específicos demonstraram sua superioridade em comparação com o placebo. No entanto, existem poucos estudos controlados avaliando estratégias específicas de como esses medicamentos devem ser usados em conjunto com outros tipos de tratamento (por exemplo, terapia de fibras), quanto tempo eles devem ser usados ou se devem ser administrados continuamente ou conforme necessário.
Recomenda-se o tratamento medicamentoso para controlar crises de sintomas (por exemplo, antidiarreicos), mas também pode-se usar a terapia farmacológica contínua (por exemplo, medicamentos antidepressivos tricíclicos) por períodos de meses ou anos.
A maioria dos medicamentos deve ser durante 3 meses quando o resultado deve ser avaliado. (exceto o antibiótico rifaximina, que deve ser usado durante apenas 2 semanas para revisão).
Ensaios randomizados avaliando agentes farmacológicos específicos demonstraram sua superioridade em comparação com o placebo. No entanto, existem poucos estudos controlados avaliando estratégias específicas de como esses medicamentos devem ser usados em conjunto com outros tipos de tratamento (por exemplo, terapia de fibras), quanto tempo eles devem ser usados ou se devem ser administrados continuamente ou conforme necessário.
Recomenda-se o tratamento medicamentoso para controlar crises de sintomas (por exemplo, antidiarreicos), mas também pode-se usar a terapia farmacológica contínua (por exemplo, medicamentos antidepressivos tricíclicos) por períodos de meses ou anos.
A maioria dos medicamentos deve ser durante 3 meses quando o resultado deve ser avaliado. (exceto o antibiótico rifaximina, que deve ser usado durante apenas 2 semanas para revisão).
Os antidepressivos são úteis para a SII. A SII às vezes complica a depressão e os antidepressivos afetam a dor abdominal devido à hipersensibilidade visceral. Há muitas evidências da eficácia dos antidepressivos tricíclicos (ADTs) e dos inibidores seletivos da recaptação da serotonina (ISRS) no tratamento da SII.
Em uma meta-análise de 15 ensaios controlados por placebo, os ADTs e os ISRSs melhoraram significativamente a dor abdominal, a condição física geral e o escore de gravidade da SII [104]. Na análise de subgrupo, os ISRS melhoraram a condição física geral, enquanto os ADTs melhoraram a dor abdominal e a pontuação de gravidade da SII.
De acordo com revisões sistemáticas sobre o efeito dos antidepressivos na SII, embora os ADTs sejam eficazes especialmente em pacientes com SII-D, eles frequentemente causam sonolência, prisão de ventre e boca seca, fazendo com que muitos pacientes abandonem o tratamento [172]. Com base em uma meta-análise dos efeitos colaterais dos antidepressivos, os ISRS podem ser usados com segurança na maior parte do IBS-C [171].
Embora os antidepressivos, especialmente os ADTs e os ISRSs, sejam benéficos no tratamento da SII, eles apresentam vários efeitos colaterais. Os antidepressivos devem, portanto, ser usados em pacientes que não respondem à terapia padrão, levando em consideração os efeitos colaterais. Os médicos devem considerar o estado mental do paciente ao selecionar antidepressivos para terapia medicamentosa na SII.
Os antidepressivos (antidepressivos tricíclicos - ADTs e inibidores seletivos da recaptação de serotonina – ISRS) modulam a dor no sistema nervoso central e periférico com efeito analgésico independente da melhora no humor e, portanto, podem aliviar os sintomas da SII. Os efeitos adversos mais comumente relatados desses antidepressivos são sonolência e boca seca.
Antidepressivo tricíclico (ADT)
Para o tratamento da dor abdominal na SII, os ADTs devem ser iniciados com doses baixas (por exemplo, amitriptilina e nortriptilina na dose de 10 a 25 mg à noite antes de dormir) com ajustes posteriores com base na tolerância e resposta. Devido ao início tardio da ação dos antidepressivos, somente após 3-4 semanas a dose deve ser revista. Os efeitos benéficos dos ADTs nos sintomas da SII parecem ser independentes dos efeitos sobre a depressão.
O antidepressivo tricíclico, por meio de sua propriedade anticolinérgica, reduz o tempo de trânsito intestinal, o que pode fornecer benefícios no tratamento da SII predominante diarreia. Dado ao seu efeito no trânsito intestinal, o ADT devem ser usados com cautela em pacientes com constipação.
Antidepressivos inibidores seletivos de recaptação de serotonina (ISRSs).
Os ISRSs são aprovados para o tratamento de transtornos de humor, como ansiedade e depressão, mas também são usados na prática clínica para tratar condições de dor crônica. Fluoxetina 20 mg por dia, paroxetina 10 mg por dia e citalopram 20 mg, estas doses podem ser aumentadas após 3, ou 4 semanas.
Os ISRSs não melhoraram significativamente os sintomas globais ou a dor abdominal na SII, embora a certeza geral na evidência seja baixa. Em alguns pacientes, os ISRSs podem melhorar a percepção dos sintomas gerais da SII e do bem-estar, melhorando os sintomas gastrointestinais, alterações coexistentes no humor e sintomas extra-intestinais.
Em uma meta-análise de 15 ensaios controlados por placebo, os ADTs e os ISRSs melhoraram significativamente a dor abdominal, a condição física geral e o escore de gravidade da SII [104]. Na análise de subgrupo, os ISRS melhoraram a condição física geral, enquanto os ADTs melhoraram a dor abdominal e a pontuação de gravidade da SII.
De acordo com revisões sistemáticas sobre o efeito dos antidepressivos na SII, embora os ADTs sejam eficazes especialmente em pacientes com SII-D, eles frequentemente causam sonolência, prisão de ventre e boca seca, fazendo com que muitos pacientes abandonem o tratamento [172]. Com base em uma meta-análise dos efeitos colaterais dos antidepressivos, os ISRS podem ser usados com segurança na maior parte do IBS-C [171].
Embora os antidepressivos, especialmente os ADTs e os ISRSs, sejam benéficos no tratamento da SII, eles apresentam vários efeitos colaterais. Os antidepressivos devem, portanto, ser usados em pacientes que não respondem à terapia padrão, levando em consideração os efeitos colaterais. Os médicos devem considerar o estado mental do paciente ao selecionar antidepressivos para terapia medicamentosa na SII.
Os antidepressivos (antidepressivos tricíclicos - ADTs e inibidores seletivos da recaptação de serotonina – ISRS) modulam a dor no sistema nervoso central e periférico com efeito analgésico independente da melhora no humor e, portanto, podem aliviar os sintomas da SII. Os efeitos adversos mais comumente relatados desses antidepressivos são sonolência e boca seca.
Antidepressivo tricíclico (ADT)
Para o tratamento da dor abdominal na SII, os ADTs devem ser iniciados com doses baixas (por exemplo, amitriptilina e nortriptilina na dose de 10 a 25 mg à noite antes de dormir) com ajustes posteriores com base na tolerância e resposta. Devido ao início tardio da ação dos antidepressivos, somente após 3-4 semanas a dose deve ser revista. Os efeitos benéficos dos ADTs nos sintomas da SII parecem ser independentes dos efeitos sobre a depressão.
O antidepressivo tricíclico, por meio de sua propriedade anticolinérgica, reduz o tempo de trânsito intestinal, o que pode fornecer benefícios no tratamento da SII predominante diarreia. Dado ao seu efeito no trânsito intestinal, o ADT devem ser usados com cautela em pacientes com constipação.
Antidepressivos inibidores seletivos de recaptação de serotonina (ISRSs).
Os ISRSs são aprovados para o tratamento de transtornos de humor, como ansiedade e depressão, mas também são usados na prática clínica para tratar condições de dor crônica. Fluoxetina 20 mg por dia, paroxetina 10 mg por dia e citalopram 20 mg, estas doses podem ser aumentadas após 3, ou 4 semanas.
Os ISRSs não melhoraram significativamente os sintomas globais ou a dor abdominal na SII, embora a certeza geral na evidência seja baixa. Em alguns pacientes, os ISRSs podem melhorar a percepção dos sintomas gerais da SII e do bem-estar, melhorando os sintomas gastrointestinais, alterações coexistentes no humor e sintomas extra-intestinais.
Teoriza-se que o supercrescimento bacteriano do intestino delgado e a disbiose desempenham um papel na SII (discutido na seção sobre fisiopatologia). A rifaximina é um antibiótico que tem absorção sistêmica muito baixa e atividade de amplo espectro contra aeróbios e anaeróbios gram-positivos e gram-negativos.
A rifaximina na dose de 550 mg três vezes ao dia durante 14 dias é mais eficaz do que placebo na melhora global dos sintomas em pacientes com SII não constipados. A rifaximina também foi significativamente mais propensa a melhorar o inchaço/distensão abdominal do que o placebo, mas não na dor abdominal, diarreia ou constipação). Os sintomas recorrem ao longo do tempo após o tratamento com rifaximina e a eficácia da rifaximina pode diminuir com o tempo, mas o retratamento mostrou-se eficaz.
A rifaximina na dose de 550 mg três vezes ao dia por 14 dias foi aprovado pelo FDA para o tratamento de SII-D com a possibilidade de mais um curso de tratamento adicional para sintomas recorrentes da SII-D.
Os efeitos adversos foram semelhantes entre os pacientes que receberam rifaximina ou placebo em todos os estudos, sendo os mais comuns: cefaleia, infecção do trato respiratório superior, náuseas, nasofaringite, diarreia e dor abdominal. O tratamento está associado a pequenas e transitórias alterações no microbioma intestinal.
O painel fez uma recomendação condicional para tratamento inicial com rifaximina em indivíduos com SII-D e para retratamento em pacientes com SII-D que tiveram resposta inicial, mas desenvolveram sintomas recorrentes. Embora a evidência mostre que o tratamento inicial e o retratamento com rifaximina sejam eficazes, as melhorias em muitos resultados podem ser pequenas e podem não ser clinicamente significativas.
A rifaximina na dose de 550 mg três vezes ao dia durante 14 dias é mais eficaz do que placebo na melhora global dos sintomas em pacientes com SII não constipados. A rifaximina também foi significativamente mais propensa a melhorar o inchaço/distensão abdominal do que o placebo, mas não na dor abdominal, diarreia ou constipação). Os sintomas recorrem ao longo do tempo após o tratamento com rifaximina e a eficácia da rifaximina pode diminuir com o tempo, mas o retratamento mostrou-se eficaz.
A rifaximina na dose de 550 mg três vezes ao dia por 14 dias foi aprovado pelo FDA para o tratamento de SII-D com a possibilidade de mais um curso de tratamento adicional para sintomas recorrentes da SII-D.
Os efeitos adversos foram semelhantes entre os pacientes que receberam rifaximina ou placebo em todos os estudos, sendo os mais comuns: cefaleia, infecção do trato respiratório superior, náuseas, nasofaringite, diarreia e dor abdominal. O tratamento está associado a pequenas e transitórias alterações no microbioma intestinal.
O painel fez uma recomendação condicional para tratamento inicial com rifaximina em indivíduos com SII-D e para retratamento em pacientes com SII-D que tiveram resposta inicial, mas desenvolveram sintomas recorrentes. Embora a evidência mostre que o tratamento inicial e o retratamento com rifaximina sejam eficazes, as melhorias em muitos resultados podem ser pequenas e podem não ser clinicamente significativas.
O estabelecimento de uma relação médico-paciente e a continuidade dos cuidados são fundamentais para o manejo de todos os pacientes com síndrome do intestino irritável (SII).
Em pacientes com sintomas leves e intermitentes que não comprometem a qualidade de vida, inicialmente recomendo modificações no estilo de vida e na dieta, em vez de agentes farmacológicos específicos.
Em pacientes com sintomas leves a moderados que não respondem ao tratamento inicial e em pacientes com sintomas moderados a graves que afetam a qualidade de vida, recomendo terapia farmacológica como tratamento adjuvante.
Em pacientes com sintomas leves e intermitentes que não comprometem a qualidade de vida, inicialmente recomendo modificações no estilo de vida e na dieta, em vez de agentes farmacológicos específicos.
Em pacientes com sintomas leves a moderados que não respondem ao tratamento inicial e em pacientes com sintomas moderados a graves que afetam a qualidade de vida, recomendo terapia farmacológica como tratamento adjuvante.
Dieta, estilo de vida e probióticos |
Dieta saudável e equilibrada com um padrão regular de refeições |
Atividade física aeróbica |
Aumento da ingestão de fibras |
Dieta para gases e se necessário com baixo teor de FODMAP* |
Suplementação de fibra solúvel (por exemplo psyllium 20–30 g/dia) |
Probióticos, Bifidobactérias (B. infantis, B. animalis. B. lactis e B. bifidum na dose de 109 ufc) |
Terapia farmacológica de primeira linha |
Laxantes osmótico (por exemplo, polietilenoglicol, PEG 4.000, 8-13 g uma vez a dia e titulado) |
Antiespasmódico geral (hioscina 10-20 mg três vezes a dia) para o caso de cólica Antiespasmódico intestinal (otilônio 20-40 mg três vezes ao dia, pinavério 50 mg três vezes a dia, trimebutina 100 mg três vezes ao dia e mebeverina 200 mg 2 vezes ao dia) |
Terapia farmacológica de segunda linha |
Secretagogos intestinal (por exemplo, lubiprostona 8 mCg duas vezes a dia) |
Pregabalina (225 mg duas vezes a dia) |
Terapias psicológicas Terapia comportamental cognitivo ou dirigido pelo intestino hipnoterapia |
Em pacientes com SII com constipação (SII-C) que falham no tratamento inicial com fibra solúvel (por exemplo, psyllium), recomenda-se o polietilenoglicol (PEG 4.000). Nos pacientes com constipação persistente apesar do tratamento com PEG 4.000, recomenda-se a lubiprostona (Amitiza®) na dose de 8mcg (2X/dia), em ambos os sexos.
Dieta saudável e equilibrada com um padrão regular de refeições (café da manhã, almoço e jantar com lanches conforme apropriado nos intervalos). Bom estilo de vida alimentar inclui separar um tempo para as refeições, sentar-se para comer, mastigar bem e não comer tarde da noite. VEJA DETALHES ACIMA!
A atividade física aeróbica reduz a dor abdominal, ajuda a controlar o trânsito colônico, facilita a evacuação e alivia a ansiedade. Para pacientes com SII, são recomendadas atividades suaves, lentas e de baixa intensidade, como caminhada, ioga, ciclismo, natação e aeróbica. A OMS recomenda realizar exercícios aeróbicos de intensidade moderada (caminhar a passos rápidos) com duração mínima de 30 minutos por cinco dias na semana ou atividades aeróbicas mais intensas (corridas com respiração rápida), com duração de 20 minutos, três dias por semana e praticar atividades de fortalecimento muscular de intensidade moderada ou alta pelo menos duas vezes por semana. Combinações de atividade física com exercícios moderados e intensos podem ser realizadas para atingir as recomendações oficiais, que são caminhar rapidamente por 30 minutos duas vezes por semana e correr 20 minutos em outros dois dias. VEJA DETALHES ACIMA!
O aumento da ingestão de fibras deve ser individualizado levando em conta se a ingestão atual é a ideal para este indivíduo e se o consumo de fibras está associado a geração de sintomas. Se for aplicável o aumento da ingestão de fibras, incentivar uma variedade de alimentos ricos em fibras (cereais, grãos, frutas, vegetais, nozes, sementes e leguminosas). Uma grande variedade é importante levando em conta quaisquer outras restrições alimentares. VEJA DETALHES ACIMA!
O psyllium e/ou semente de linhaça deve ser considerado em pacientes com SII cujo sintoma predominante é a constipação. Como alguns pacientes podem apresentar aumento de inchaço e gases, sugere-se uma dose inicial de psyllium de metade a uma colher de sopa por dia. A dose do psyllium deve ser titulada lentamente com base na resposta ao tratamento até 20–30 g/dia. VEJA DETALHES DE COMO CONSUMIR O PSYLLIUM (VEJA NESTA PÁGINA) E A SEMENTE DE LINHAÇA (VEJA NESTA PÁGINA).
Os pacientes com inchaço/distensão abdominal e excesso de gases se beneficiam da exclusão de alimentos que aumentam a produção de gases. VEJA DETALHES ACIMA! E caso não melhorem recomenda-se a adoção de uma dieta com baixo teor de FODMAPs (oligo, di e monossacarídeos e polióis fermentáveis) que envolve a eliminação de um número maior de alimentos. VEJA DETALHES ACIMA!
Os probióticos, Bifidobactérias (B. infantis, B. animalis. B. lactis e B. bifidum na dose de 109 ufc), são condicionalmente recomendados para sintomas gerais, distensão/inchaço abdominal e flatulência na SII com a maioria dos pacientes apresentando melhora após 4-8 semanas de uso. VEJA DETALHES ACIMA!
O PEG 4.000 (laxante osmótico) é barato, amplamente disponível e tem menos efeitos colaterais (inchaço e desconforto abdominal) em comparação com outros laxantes osmóticos (por exemplo, lactulose e leite de magnésia). Inicialmente, recomenda-se a dose de 17 g de pó dissolvido em 250 mL de água uma vez ao dia ( de preferênia pela manhã) e titulamos para cima ou para baixo (até um máximo de 34 g por dia) de acordo com a resposta. Os trabalhos evidenciaram que o uso regular do PEG 4.000 melhora a constipação, mas não a dor abdominal. VEJA DETALHES ACIMA!
Os antiespasmódicos devem ser administrados conforme a necessidade e/ou em resposta a fatores desencadeantes e/ou exacerbadores sabidamente conhecidos. Os antiespasmódicos promovem alívio da dor abdominal a curto prazo nos pacientes com SII, mas sua eficácia a longo prazo não foi estabelecida.
Agentes antiespasmódicos anticolinérgicos / antimuscarínico e relaxante de músculo liso para o caso de cólica por fatores desencadeantes e/ou exacerbadores sabidamente conhecidos (escopolamina - 1 comprimido ou 20 a 40 gotas (10-20 mg), 3 a 5 vezes ao dia ou Tropinal® [dipirona 300mg + escopolamina 6,5mcg + hiosciamina 104mcg + homatropina 1.0mg] - 1 a 2 comprimidos, 3 vezes ao dia).
Agentes antiespasmódicos que agem diretamente no relaxamento do músculo liso intestinal. A inibição seletiva do músculo liso gastrointestinal reduz a atividade motora colônica e pode ser benéfica em pacientes com dor abdominal pós-prandial, inchaço abdominal, gases, flatulência e urgência fecal. Devem ser usados durante 1 a 3 meses de acordo com a resposta clínica.
Brometo de Otilônio. Em 3 estudos o otilônio 40 mg 3xs/dia diminuiu a frequência da dor e inchaço abdominal em comparação com o placebo durante as semanas 3-4 e na semana 15; no entanto, não foram observadas diferenças entre o otilônio e placebo após o tratamento.
Brometo de Pinavério. Pacientes com SII-D recebendo pinavério 50 mg 3xs/dia experimentaram melhoras significativas na dor abdominal e da consistência das fezes nas semanas 2 e 4. A combinação de pinavério 100 mg mais simeticona 300 mg duas vezes por dia melhorou significativamente a intensidade da dor e inchaço abdominal.
Maleato de Trimebutina. Em 4 pequenos estudos de trimebutina 100 ou 200 mg 3 xs/dia administrados por 2 semanas a 6 meses, a melhora da dor abdominal foi observada de forma inconsistente.
Cloridrato de Mebeverina. Um estudo revelou que a mebeverina 200 mg 2 vezes/dia é tão eficaz quanto o otilônio na melhora dos sintomas da SII, incluindo dor abdominal, flatulência e distensão abdominal.
Antidepressivos inibidores seletivos de recaptação de serotonina (ISRSs). Os ISRSs são aprovados para o tratamento de transtornos de humor, como ansiedade e depressão, mas também são usados na prática clínica para tratar condições de dor crônica. Fluoxetina 20 mg por dia, paroxetina 10 mg por dia que poderia ser aumentada e citalopram numa dose inicial de 20 mg que pode ser aumentada para 40 mg por dia após 3, ou 4 semanas. Os ISRSs não melhoraram significativamente os sintomas globais ou a dor abdominal na SII, embora a certeza geral na evidência seja baixa. Em alguns pacientes, os ISRSs podem melhorar a percepção dos sintomas gerais da SII e do bem-estar, melhorando os sintomas gastrointestinais, as alterações coexistentes no humor e os sintomas extra-intestinais. VEJA DETALHES ACIMA!
A lubiprostona (Amitiza®) é usado no tratamento da SII-constipação em mulheres com 18 anos ou mais. A dose aprovada é de 8 microgramas duas vezes ao dia. A lubiprostona não foi diretamente comparada com outras opções de tratamento para a SII-constipação e a sua segurança a longo prazo ainda deve ser estabelecida. Embora tenha havido um efeito significativamente benéfico da lubiprostona nos resultados globais e na resposta à dor abdominal em comparação com o placebo, essas diferenças não atingiram o limiar para ser clinicamente significativo.
A atividade física aeróbica reduz a dor abdominal, ajuda a controlar o trânsito colônico, facilita a evacuação e alivia a ansiedade. Para pacientes com SII, são recomendadas atividades suaves, lentas e de baixa intensidade, como caminhada, ioga, ciclismo, natação e aeróbica. A OMS recomenda realizar exercícios aeróbicos de intensidade moderada (caminhar a passos rápidos) com duração mínima de 30 minutos por cinco dias na semana ou atividades aeróbicas mais intensas (corridas com respiração rápida), com duração de 20 minutos, três dias por semana e praticar atividades de fortalecimento muscular de intensidade moderada ou alta pelo menos duas vezes por semana. Combinações de atividade física com exercícios moderados e intensos podem ser realizadas para atingir as recomendações oficiais, que são caminhar rapidamente por 30 minutos duas vezes por semana e correr 20 minutos em outros dois dias. VEJA DETALHES ACIMA!
O aumento da ingestão de fibras deve ser individualizado levando em conta se a ingestão atual é a ideal para este indivíduo e se o consumo de fibras está associado a geração de sintomas. Se for aplicável o aumento da ingestão de fibras, incentivar uma variedade de alimentos ricos em fibras (cereais, grãos, frutas, vegetais, nozes, sementes e leguminosas). Uma grande variedade é importante levando em conta quaisquer outras restrições alimentares. VEJA DETALHES ACIMA!
O psyllium e/ou semente de linhaça deve ser considerado em pacientes com SII cujo sintoma predominante é a constipação. Como alguns pacientes podem apresentar aumento de inchaço e gases, sugere-se uma dose inicial de psyllium de metade a uma colher de sopa por dia. A dose do psyllium deve ser titulada lentamente com base na resposta ao tratamento até 20–30 g/dia. VEJA DETALHES DE COMO CONSUMIR O PSYLLIUM (VEJA NESTA PÁGINA) E A SEMENTE DE LINHAÇA (VEJA NESTA PÁGINA).
Os pacientes com inchaço/distensão abdominal e excesso de gases se beneficiam da exclusão de alimentos que aumentam a produção de gases. VEJA DETALHES ACIMA! E caso não melhorem recomenda-se a adoção de uma dieta com baixo teor de FODMAPs (oligo, di e monossacarídeos e polióis fermentáveis) que envolve a eliminação de um número maior de alimentos. VEJA DETALHES ACIMA!
Os probióticos, Bifidobactérias (B. infantis, B. animalis. B. lactis e B. bifidum na dose de 109 ufc), são condicionalmente recomendados para sintomas gerais, distensão/inchaço abdominal e flatulência na SII com a maioria dos pacientes apresentando melhora após 4-8 semanas de uso. VEJA DETALHES ACIMA!
O PEG 4.000 (laxante osmótico) é barato, amplamente disponível e tem menos efeitos colaterais (inchaço e desconforto abdominal) em comparação com outros laxantes osmóticos (por exemplo, lactulose e leite de magnésia). Inicialmente, recomenda-se a dose de 17 g de pó dissolvido em 250 mL de água uma vez ao dia ( de preferênia pela manhã) e titulamos para cima ou para baixo (até um máximo de 34 g por dia) de acordo com a resposta. Os trabalhos evidenciaram que o uso regular do PEG 4.000 melhora a constipação, mas não a dor abdominal. VEJA DETALHES ACIMA!
Os antiespasmódicos devem ser administrados conforme a necessidade e/ou em resposta a fatores desencadeantes e/ou exacerbadores sabidamente conhecidos. Os antiespasmódicos promovem alívio da dor abdominal a curto prazo nos pacientes com SII, mas sua eficácia a longo prazo não foi estabelecida.
Agentes antiespasmódicos anticolinérgicos / antimuscarínico e relaxante de músculo liso para o caso de cólica por fatores desencadeantes e/ou exacerbadores sabidamente conhecidos (escopolamina - 1 comprimido ou 20 a 40 gotas (10-20 mg), 3 a 5 vezes ao dia ou Tropinal® [dipirona 300mg + escopolamina 6,5mcg + hiosciamina 104mcg + homatropina 1.0mg] - 1 a 2 comprimidos, 3 vezes ao dia).
Agentes antiespasmódicos que agem diretamente no relaxamento do músculo liso intestinal. A inibição seletiva do músculo liso gastrointestinal reduz a atividade motora colônica e pode ser benéfica em pacientes com dor abdominal pós-prandial, inchaço abdominal, gases, flatulência e urgência fecal. Devem ser usados durante 1 a 3 meses de acordo com a resposta clínica.
Brometo de Otilônio. Em 3 estudos o otilônio 40 mg 3xs/dia diminuiu a frequência da dor e inchaço abdominal em comparação com o placebo durante as semanas 3-4 e na semana 15; no entanto, não foram observadas diferenças entre o otilônio e placebo após o tratamento.
Brometo de Pinavério. Pacientes com SII-D recebendo pinavério 50 mg 3xs/dia experimentaram melhoras significativas na dor abdominal e da consistência das fezes nas semanas 2 e 4. A combinação de pinavério 100 mg mais simeticona 300 mg duas vezes por dia melhorou significativamente a intensidade da dor e inchaço abdominal.
Maleato de Trimebutina. Em 4 pequenos estudos de trimebutina 100 ou 200 mg 3 xs/dia administrados por 2 semanas a 6 meses, a melhora da dor abdominal foi observada de forma inconsistente.
Cloridrato de Mebeverina. Um estudo revelou que a mebeverina 200 mg 2 vezes/dia é tão eficaz quanto o otilônio na melhora dos sintomas da SII, incluindo dor abdominal, flatulência e distensão abdominal.
Antidepressivos inibidores seletivos de recaptação de serotonina (ISRSs). Os ISRSs são aprovados para o tratamento de transtornos de humor, como ansiedade e depressão, mas também são usados na prática clínica para tratar condições de dor crônica. Fluoxetina 20 mg por dia, paroxetina 10 mg por dia que poderia ser aumentada e citalopram numa dose inicial de 20 mg que pode ser aumentada para 40 mg por dia após 3, ou 4 semanas. Os ISRSs não melhoraram significativamente os sintomas globais ou a dor abdominal na SII, embora a certeza geral na evidência seja baixa. Em alguns pacientes, os ISRSs podem melhorar a percepção dos sintomas gerais da SII e do bem-estar, melhorando os sintomas gastrointestinais, as alterações coexistentes no humor e os sintomas extra-intestinais. VEJA DETALHES ACIMA!
A lubiprostona (Amitiza®) é usado no tratamento da SII-constipação em mulheres com 18 anos ou mais. A dose aprovada é de 8 microgramas duas vezes ao dia. A lubiprostona não foi diretamente comparada com outras opções de tratamento para a SII-constipação e a sua segurança a longo prazo ainda deve ser estabelecida. Embora tenha havido um efeito significativamente benéfico da lubiprostona nos resultados globais e na resposta à dor abdominal em comparação com o placebo, essas diferenças não atingiram o limiar para ser clinicamente significativo.
- Em pacientes com dor e inchaço abdominal devido à SII, recomenda-se usar os antiespasmódicos de acordo com a necessidade.
- Em pacientes com dor e inchaço abdominal persistente apesar dos antiespasmódicos, recomenda-se um teste com antidepressivos.
- Em pacientes com SII moderada a grave sem constipação, particularmente aqueles com inchaço abdominal, que não responderam a outras terapias, recomenda-se o tratamento com o antibiótico rifaximina por duas semanas.
Dieta, estilo de vida e probióticos |
Dieta saudável e equilibrada com um padrão regular de refeições |
Atividade física aeróbica |
Dieta para gases e se necessário com baixo teor de FODMAP |
Dieta de eliminação: álcool, cafeína, gordura e alimentos picantes |
Suplementação de psyllium e de Vit D é recomendada |
Probióticos, (Bifidobacterium infantis, Lactobacillus acidophilus, Bacillus cereus e Enterococcus faecalis na dose de 109 ufc) |
Terapia farmacológica de primeira linha |
Antiespasmódico geral (hioscina 10–20 mg três vezes a dia) para o caso de cólica |
Antiespasmódico intestinal (otilônio 20–40 mg três vezes ao dia, pinavério 50 mg três vezes a dia, trimebutina 100 mg três vezes ao dia e mebeverina 200 mg 2 vezes ao dia) |
Terapia farmacológica de segunda linha |
Antidepressivos inibidores seletivos de recaptação de serotonina (Fluoxetina 20 mg ao dia, paroxetina 10 mg ao dia e citalopram 20 mg ao dia, doses podem ser aumentadas). |
Antibiótico rifaximina (550 mg três vezes a dia) |
Pregabalina (150 mg duas vezes a dia e titulado) |
Terapia comportamental cognitivo ou dirigido pelo intestino hipnoterapia |
Dieta saudável e equilibrada com um padrão regular de refeições (café da manhã, almoço e jantar com lanches conforme apropriado nos intervalos). Bom estilo de vida alimentar inclui separar um tempo para as refeições, sentar-se para comer, mastigar bem e não comer tarde da noite. VEJA DETALHES ACIMA!
A atividade física aeróbica reduz a dor abdominal, ajuda a controlar o trânsito colônico, facilita a evacuação e alivia a ansiedade. Para pacientes com SII, são recomendadas atividades suaves, lentas e de baixa intensidade, como caminhada, ioga, ciclismo, natação e aeróbica. A OMS recomenda realizar exercícios aeróbicos de intensidade moderada (caminhar a passos rápidos) com duração mínima de 30 minutos por cinco dias na semana ou atividades aeróbicas mais intensas (corridas com respiração rápida), com duração de 20 minutos, três dias por semana e praticar atividades de fortalecimento muscular de intensidade moderada ou alta pelo menos duas vezes por semana. Combinações de atividade física com exercícios moderados e intensos podem ser realizadas para atingir as recomendações oficiais, que são caminhar rapidamente por 30 minutos duas vezes por semana e correr 20 minutos em outros dois dias. VEJA DETALHES ACIMA!
O aumento da ingestão de fibras deve ser individualizado levando em conta se a ingestão atual é a ideal para este indivíduo e se o consumo de fibras está associado a geração de sintomas. Se for aplicável o aumento da ingestão de fibras, incentivar uma variedade de alimentos ricos em fibras (cereais, grãos, frutas, vegetais, nozes, sementes e leguminosas). Uma grande variedade é importante levando em conta quaisquer outras restrições alimentares. VEJA DETALHES ACIMA!
O psyllium e/ou semente de linhaça deve ser considerado em pacientes com SII cujo sintoma predominante é a constipação. Como alguns pacientes podem apresentar aumento de inchaço e gases, sugere-se uma dose inicial de psyllium de metade a uma colher de sopa por dia. A dose do psyllium deve ser titulada lentamente com base na resposta ao tratamento até 20–30 g/dia. VEJA DETALHES DE COMO CONSUMIR O PSYLLIUM (VEJA NESTA PÁGINA) E A SEMENTE DE LINHAÇA (VEJA NESTA PÁGINA).
Os pacientes com inchaço/distensão abdominal e excesso de gases se beneficiam da exclusão de alimentos que aumentam a produção de gases. VEJA DETALHES ACIMA! E caso não melhorem recomenda-se a adoção de uma dieta com baixo teor de FODMAPs (oligo, di e monossacarídeos e polióis fermentáveis) que envolve a eliminação de um número maior de alimentos. VEJA DETALHES ACIMA!
O PEG 4.000 (laxante osmótico) é barato, amplamente disponível e tem menos efeitos colaterais (inchaço e desconforto abdominal) em comparação com outros laxantes osmóticos (por exemplo, lactulose e leite de magnésia). Inicialmente, recomenda-se a dose de 17 g de pó dissolvido em 250 mL de água uma vez ao dia ( de preferênia pela manhã) e titulamos para cima ou para baixo (até um máximo de 34 g por dia) de acordo com a resposta. Os trabalhos evidenciaram que o uso regular do PEG 4.000 melhora a constipação, mas não a dor abdominal. VEJA DETALHES ACIMA!
Os probióticos, Bifidobactérias (B. infantis, B. animalis. B. lactis e B. bifidum na dose de 109 ufc), são condicionalmente recomendados para sintomas gerais, distensão/inchaço abdominal e flatulência na SII com a maioria dos pacientes apresentando melhora após 4-8 semanas de uso. VEJA DETALHES ACIMA!
Os antiespasmódicos devem ser administrados conforme a necessidade e/ou em resposta a fatores desencadeantes e/ou exacerbadores sabidamente conhecidos. Os antiespasmódicos promovem alívio da dor abdominal a curto prazo nos pacientes com SII, mas sua eficácia a longo prazo não foi estabelecida.
Agentes antiespasmódicos anticolinérgicos / antimuscarínico e relaxante de músculo liso para o caso de cólica por fatores desencadeantes e/ou exacerbadores sabidamente conhecidos (escopolamina - 1 comprimido ou 20 a 40 gotas (10-20 mg), 3 a 5 vezes ao dia ou Tropinal® [dipirona 300mg + escopolamina 6,5mcg + hiosciamina 104mcg + homatropina 1.0mg] - 1 a 2 comprimidos, 3 vezes ao dia).
Agentes antiespasmódicos que agem diretamente no relaxamento do músculo liso intestinal. A inibição seletiva do músculo liso gastrointestinal reduz a atividade motora colônica e pode ser benéfica em pacientes com dor abdominal pós-prandial, inchaço abdominal, gases, flatulência e urgência fecal. Devem ser usados durante 1 a 3 meses de acordo com a resposta clínica.
Brometo de Otilônio. Em 3 estudos o otilônio 40 mg 3xs/dia diminuiu a frequência da dor e inchaço abdominal em comparação com o placebo durante as semanas 3-4 e na semana 15; no entanto, não foram observadas diferenças entre o otilônio e placebo após o tratamento.
Brometo de Pinavério. Pacientes com SII-D recebendo pinavério 50 mg 3xs/dia experimentaram melhoras significativas na dor abdominal e da consistência das fezes nas semanas 2 e 4. A combinação de pinavério 100 mg mais simeticona 300 mg duas vezes por dia melhorou significativamente a intensidade da dor e inchaço abdominal.
Maleato de Trimebutina. Em 4 pequenos estudos de trimebutina 100 ou 200 mg 3 xs/dia administrados por 2 semanas a 6 meses, a melhora da dor abdominal foi observada de forma inconsistente.
Cloridrato de Mebeverina. Um estudo revelou que a mebeverina 200 mg 2 vezes/dia é tão eficaz quanto o otilônio na melhora dos sintomas da SII, incluindo dor abdominal, flatulência e distensão abdominal.
Antidepressivo tricíclico (ADT) no tratamento da síndrome do intestino irritável (SII) Para o tratamento da dor abdominal na SII, os ADTs devem ser iniciados com doses baixas (por exemplo, amitriptilina e nortriptilina na dose de 10 a 25 mg à noite antes de dormir) com ajustes posteriores com base na tolerância e resposta. Devido ao início tardio da ação dos antidepressivos, somente após 3-4 semanas a dose deve ser revista. Os efeitos benéficos dos ADTs nos sintomas da SII parecem ser independentes dos efeitos sobre a depressão. O antidepressivo tricíclico, por meio de sua propriedade anticolinérgica, reduz o tempo de trânsito intestinal, o que pode fornecer benefícios no tratamento da SII predominante diarreia. Dado ao seu efeito no trânsito intestinal, o ADT devem ser usados com cautela em pacientes com constipação. VEJA DETALHES ACIMA!
Antidepressivos inibidores seletivos de recaptação de serotonina (ISRSs) no tratamento da síndrome do intestino irritável (SII)
Os ISRSs são aprovados para o tratamento de transtornos de humor, como ansiedade e depressão, mas também são usados na prática clínica para tratar condições de dor crônica. Fluoxetina 20 mg por dia, paroxetina 10 mg por dia e citalopram 20 mg, estas doses podem ser aumentadas após 3, ou 4 semanas. Os ISRSs não melhoraram significativamente os sintomas globais ou a dor abdominal na SII, embora a certeza geral na evidência seja baixa. Em alguns pacientes, os ISRSs podem melhorar a percepção dos sintomas gerais da SII e do bem-estar, melhorando os sintomas gastrointestinais, alterações coexistentes no humor e sintomas extra-intestinais. VEJA DETALHES ACIMA!
Antibióticos no tratamento da síndrome do intestino irritável (SII). Embora os antibióticos não sejam recomendados em todos os pacientes com SII, os pacientes com SII moderada a grave sem constipação, particularmente aqueles com inchaço abdominal, que falharam em responder a outros tratamentos (por exemplo, uma dieta pobre em FODMAPs, antiespasmódicos e TCAs), recomenda-se um tratamento teste por duas semanas com rifaximina.
A rifaximina (550 mg três vezes ao dia durante 14 dias) está associado a uma melhora geral dos sintomas da SII e, em especial, na diminuição do inchaço abdominal e da diarreia, quando comparados com o placebo. No entanto, a melhora no inchaço abdominal em pacientes com SII sem constipação é modesta. VEJA DETALHES ACIMA!
Os pacientes com inchaço/distensão abdominal e excesso de gases se beneficiam da exclusão de alimentos que aumentam a produção de gases. VEJA DETALHES ACIMA! E caso não melhorem recomenda-se a adoção de uma dieta com baixo teor de FODMAPs (oligo, di e monossacarídeos e polióis fermentáveis) que envolve a eliminação de um número maior de alimentos. VEJA DETALHES ACIMA!
O PEG 4.000 (laxante osmótico) é barato, amplamente disponível e tem menos efeitos colaterais (inchaço e desconforto abdominal) em comparação com outros laxantes osmóticos (por exemplo, lactulose e leite de magnésia). Inicialmente, recomenda-se a dose de 17 g de pó dissolvido em 250 mL de água uma vez ao dia ( de preferênia pela manhã) e titulamos para cima ou para baixo (até um máximo de 34 g por dia) de acordo com a resposta. Os trabalhos evidenciaram que o uso regular do PEG 4.000 melhora a constipação, mas não a dor abdominal. VEJA DETALHES ACIMA!
Os probióticos, Bifidobactérias (B. infantis, B. animalis. B. lactis e B. bifidum na dose de 109 ufc), são condicionalmente recomendados para sintomas gerais, distensão/inchaço abdominal e flatulência na SII com a maioria dos pacientes apresentando melhora após 4-8 semanas de uso. VEJA DETALHES ACIMA!
Os antiespasmódicos devem ser administrados conforme a necessidade e/ou em resposta a fatores desencadeantes e/ou exacerbadores sabidamente conhecidos. Os antiespasmódicos promovem alívio da dor abdominal a curto prazo nos pacientes com SII, mas sua eficácia a longo prazo não foi estabelecida.
Agentes antiespasmódicos anticolinérgicos / antimuscarínico e relaxante de músculo liso para o caso de cólica por fatores desencadeantes e/ou exacerbadores sabidamente conhecidos (escopolamina - 1 comprimido ou 20 a 40 gotas (10-20 mg), 3 a 5 vezes ao dia ou Tropinal® [dipirona 300mg + escopolamina 6,5mcg + hiosciamina 104mcg + homatropina 1.0mg] - 1 a 2 comprimidos, 3 vezes ao dia).
Agentes antiespasmódicos que agem diretamente no relaxamento do músculo liso intestinal. A inibição seletiva do músculo liso gastrointestinal reduz a atividade motora colônica e pode ser benéfica em pacientes com dor abdominal pós-prandial, inchaço abdominal, gases, flatulência e urgência fecal. Devem ser usados durante 1 a 3 meses de acordo com a resposta clínica.
Brometo de Otilônio. Em 3 estudos o otilônio 40 mg 3xs/dia diminuiu a frequência da dor e inchaço abdominal em comparação com o placebo durante as semanas 3-4 e na semana 15; no entanto, não foram observadas diferenças entre o otilônio e placebo após o tratamento.
Brometo de Pinavério. Pacientes com SII-D recebendo pinavério 50 mg 3xs/dia experimentaram melhoras significativas na dor abdominal e da consistência das fezes nas semanas 2 e 4. A combinação de pinavério 100 mg mais simeticona 300 mg duas vezes por dia melhorou significativamente a intensidade da dor e inchaço abdominal.
Maleato de Trimebutina. Em 4 pequenos estudos de trimebutina 100 ou 200 mg 3 xs/dia administrados por 2 semanas a 6 meses, a melhora da dor abdominal foi observada de forma inconsistente.
Cloridrato de Mebeverina. Um estudo revelou que a mebeverina 200 mg 2 vezes/dia é tão eficaz quanto o otilônio na melhora dos sintomas da SII, incluindo dor abdominal, flatulência e distensão abdominal.
Antidepressivo tricíclico (ADT) no tratamento da síndrome do intestino irritável (SII) Para o tratamento da dor abdominal na SII, os ADTs devem ser iniciados com doses baixas (por exemplo, amitriptilina e nortriptilina na dose de 10 a 25 mg à noite antes de dormir) com ajustes posteriores com base na tolerância e resposta. Devido ao início tardio da ação dos antidepressivos, somente após 3-4 semanas a dose deve ser revista. Os efeitos benéficos dos ADTs nos sintomas da SII parecem ser independentes dos efeitos sobre a depressão. O antidepressivo tricíclico, por meio de sua propriedade anticolinérgica, reduz o tempo de trânsito intestinal, o que pode fornecer benefícios no tratamento da SII predominante diarreia. Dado ao seu efeito no trânsito intestinal, o ADT devem ser usados com cautela em pacientes com constipação. VEJA DETALHES ACIMA!
Antidepressivos inibidores seletivos de recaptação de serotonina (ISRSs) no tratamento da síndrome do intestino irritável (SII)
Os ISRSs são aprovados para o tratamento de transtornos de humor, como ansiedade e depressão, mas também são usados na prática clínica para tratar condições de dor crônica. Fluoxetina 20 mg por dia, paroxetina 10 mg por dia e citalopram 20 mg, estas doses podem ser aumentadas após 3, ou 4 semanas. Os ISRSs não melhoraram significativamente os sintomas globais ou a dor abdominal na SII, embora a certeza geral na evidência seja baixa. Em alguns pacientes, os ISRSs podem melhorar a percepção dos sintomas gerais da SII e do bem-estar, melhorando os sintomas gastrointestinais, alterações coexistentes no humor e sintomas extra-intestinais. VEJA DETALHES ACIMA!
Antibióticos no tratamento da síndrome do intestino irritável (SII). Embora os antibióticos não sejam recomendados em todos os pacientes com SII, os pacientes com SII moderada a grave sem constipação, particularmente aqueles com inchaço abdominal, que falharam em responder a outros tratamentos (por exemplo, uma dieta pobre em FODMAPs, antiespasmódicos e TCAs), recomenda-se um tratamento teste por duas semanas com rifaximina.
A rifaximina (550 mg três vezes ao dia durante 14 dias) está associado a uma melhora geral dos sintomas da SII e, em especial, na diminuição do inchaço abdominal e da diarreia, quando comparados com o placebo. No entanto, a melhora no inchaço abdominal em pacientes com SII sem constipação é modesta. VEJA DETALHES ACIMA!
Em pacientes com SII propensos a diarreia, as fezes são caracteristicamente moles e frequentes, mas com volume diário total normal. Em pacientes com diarreia como sintoma predominante, recomenda-se o uso de antidiarreicos (por exemplo, loperamida) como tratamento inicial e o de sequestrador de ácidos biliares como terapia de segunda linha.
Dieta, estilo de vida e probióticos |
Dieta saudável e equilibrada com um padrão regular de refeições |
Atividade física aeróbica |
Dieta para gases e se necessário com baixo teor de FODMAP |
Dieta de eliminação: álcool, cafeína, gordura e alimentos picantes |
Suplementação de psyllium e de Vit D é recomendada |
Probióticos, (Bifidobacterium infantis, Lactobacillus acidophilus, Bacillus cereus e Enterococcus faecalis na dose de 109 ufc) |
Terapia farmacológica de primeira linha |
Antidiarreicos (loperamida 4 mg) |
Antiespasmódico geral (hioscina 10–20 mg três vezes a dia) para o caso de cólica |
Antiespasmódico intestinal (otilônio 20–40 mg três vezes ao dia, pinavério 50 mg três vezes a dia, trimebutina 100 mg três vezes ao dia e mebeverina 200 mg 2 vezes ao dia) |
Terapia farmacológica de segunda linha |
Ondansetrona (4 mg uma vez a dia e titulado) |
Antidepressivo tricíclico (Amitriptilina, nortriptilina e imipramina podem ser iniciadas na dose de 10 a 25 mg na hora de dormir) |
Antibiótico rifaximina (550 mg três vezes a dia) |
Pregabalina (150 mg duas vezes a dia e titulado) |
Colestiramina (4 g três vezes por dia e titulado) |
Terapia comportamental cognitivo ou dirigido pelo intestino hipnoterapia |
Dieta saudável e equilibrada com um padrão regular de refeições (café da manhã, almoço e jantar com lanches conforme apropriado nos intervalos). Bom estilo de vida alimentar inclui separar um tempo para as refeições, sentar-se para comer, mastigar bem e não comer tarde da noite. VEJA DETALHES ACIMA!
A atividade física aeróbica reduz a dor abdominal, ajuda a controlar o trânsito colônico, facilita a evacuação e alivia a ansiedade. Para pacientes com SII, são recomendadas atividades suaves, lentas e de baixa intensidade, como caminhada, ioga, ciclismo, natação e aeróbica. A OMS recomenda realizar exercícios aeróbicos de intensidade moderada (caminhar a passos rápidos) com duração mínima de 30 minutos por cinco dias na semana ou atividades aeróbicas mais intensas (corridas com respiração rápida), com duração de 20 minutos, três dias por semana e praticar atividades de fortalecimento muscular de intensidade moderada ou alta pelo menos duas vezes por semana. Combinações de atividade física com exercícios moderados e intensos podem ser realizadas para atingir as recomendações oficiais, que são caminhar rapidamente por 30 minutos duas vezes por semana e correr 20 minutos em outros dois dias. VEJA DETALHES ACIMA!
Dieta na SII-D. Os pacientes com diarreia que apresentam inchaço/distensão abdominal, dor abdominal e excesso de gases se beneficiam da exclusão de alimentos que aumentam a produção de gases e caso não melhorem recomenda-se a adoção de uma dieta com baixo teor de FODMAPs (oligo, di e monossacarídeos e polióis fermentáveis) que envolve a eliminação de um número maior de alimentos. VEJA MAIS! BAIXE AS RECOMENDAÇÕES DIETÉTICAS E COMPORTAMENTAIS!
Os conselhos dietéticos gerais (CDG) implica recomendações dietéticas com limitação de cafeína, álcool, alimentos condimentados, alimentos gordurosos e bebidas carbonatadas; comer pequenas refeições de frequência; comer devagar e em paz; e evitar gomas de mascar e adoçantes contendo polióis.
A dieta baixa em FODMAP melhora significativamente os sintomas gastrointestinais (dor abdominal, inchaço e diarreia) versus conselhos dietéticos gerais. Embora o grupo com os conselhos dietéticos gerais tenha mostrado uma redução significativa nos sintomas gastrointestinais após 6 semanas, mas a redução é maior no grupo de dieta baixa FODMAP. VEJA DETALHES ACIMA!
Bebidas alcoólicas. Avaliar a ingestão de álcool em relação aos sintomas (fezes amolecidas, dor abdominal, náuseas, indigestão e diarreia), considerar a redução da ingestão. Avaliar a ingestão de cafeína e, se relacionado aos sintomas (refluxo gastresofágico, dor abdominal e fezes amolecidas), considerar a redução da ingestão. Avaliar a ingestão de alimentos picantes e pimenta e, se relacionado aos sintomas (refluxo gastresofágico, dor abdominal e queimação oral), considerar a eliminação.
Alimentos gordurosos. Se os sintomas, em particular dor abdominal e distensão/inchaço abdominal, estiver relacionado a sintomas durante ou após comer alimentos gordurosos, avaliar a diminuição da ingestão de gordura.
Leite e os produtos lácteos. Use uma dieta baixa em lactose apenas em pacientes com diagnóstico por exames complementares de intolerância à lactose.
Glúten. Neste momento, nenhuma recomendação pode ser feita para tratar os sintomas da SII com uma dieta sem glúten em pacientes não celíacos.
A suplementação de psyllium é recomendada na SII com constipação e com diarreia. Em casos de constipação, amolece as fezes duras, enquanto em casos de diarreia, solidifica as fezes moles e estabiliza a frequência e a forma dos movimentos intestinais em indivíduos com SII. A dose recomendada é de pelo menos 10 g duas vezes ao dia (20 g ao dia) junto com um mínimo de 250 ml de água. Geralmente os benefícios começam em 1 a 2 semanas e se mantêm a longo prazo. É uma forma de tratamento econômica, segura e bem aceita pelo paciente. A dose do psyllium deve ser titulada lentamente com base na resposta ao tratamento até 20–30 g/dia. VEJA DETALHES DE COMO CONSUMIR O PSYLLIUM (VEJA NESTA PÁGINA)
A vitamina D é extremamente importante para cada indivíduo. Devido à síntese limitada na pele e à ingestão alimentar muito baixa, a suplementação de vitamina D é recomendada para todos. A dosagem preventiva recomendada varia de 800–2.000 UI por dia. É particularmente importante prestar atenção à ocorrência de deficiências de vitamina D entre pacientes com SII e recomendar a suplementação de vitamina D neste grupo, pois a inclusão de suplementos pode ter efeitos positivos no curso da doença. A suplementação pode aliviar os sintomas da SII e melhorar a qualidade de vida.
Os probióticos, Bifidobactérias (B. infantis, B. animalis. B. lactis e B. bifidum na dose de 109 ufc), são condicionalmente recomendados para sintomas gerais, distensão/inchaço abdominal e flatulência na SII com a maioria dos pacientes apresentando melhora após 4-8 semanas de uso. VEJA DETALHES ACIMA!
Loperamida. Em pacientes com SII-diarreia, recomenda-se a loperamida, comprimido de 2 mg, 45 minutos antes de uma refeição, em doses programadas regularmente (dose diária máxima de 16 mg/dia). Os agentes antidiarreicos inibem o peristaltismo, prolongam o tempo de trânsito intestinal e reduzem o volume fecal. No entanto, a loperamida deve ser usada em doses limitadas, conforme necessário, em pacientes com alternância entre diarreia e constipação.
Os antiespasmódicos devem ser administrados conforme a necessidade e/ou em resposta a fatores desencadeantes e/ou exacerbadores sabidamente conhecidos. Os antiespasmódicos promovem alívio da dor abdominal a curto prazo nos pacientes com SII, mas sua eficácia a longo prazo não foi estabelecida.
Agentes antiespasmódicos anticolinérgicos / antimuscarínico e relaxante de músculo liso para o caso de cólica por fatores desencadeantes e/ou exacerbadores sabidamente conhecidos (escopolamina - 1 comprimido ou 20 a 40 gotas (10-20 mg), 3 a 5 vezes ao dia ou Tropinal® [dipirona 300mg + escopolamina 6,5mcg + hiosciamina 104mcg + homatropina 1.0mg] - 1 a 2 comprimidos, 3 vezes ao dia).
Agentes antiespasmódicos que agem diretamente no relaxamento do músculo liso intestinal.
A ondansetrona (dose inicial de 4 mg uma a duas vezes ao dia) melhora significativamente em pacientes com SII-diarreia a consistência, a frequência e a urgência das fezes, mas não foi associado a uma melhora significativa dor abdominal. O efeito da ondansetrona na forma das fezes é rápido, sendo observado na primeira semana com uma melhora na consistência das fezes e redução no número de evacuações amolecidas diárias.
Antidepressivo tricíclico (ADT) no tratamento da síndrome do intestino irritável (SII). Para o tratamento da dor abdominal na SII, os ADTs devem ser iniciados com doses baixas (por exemplo, amitriptilina e nortriptilina na dose de 10 a 25 mg à noite antes de dormir) com ajustes posteriores com base na tolerância e resposta. Devido ao início tardio da ação dos antidepressivos, somente após 3-4 semanas a dose deve ser revista. Os efeitos benéficos dos ADTs nos sintomas da SII parecem ser independentes dos efeitos sobre a depressão. O antidepressivo tricíclico, por meio de sua propriedade anticolinérgica, reduz o tempo de trânsito intestinal, o que pode fornecer benefícios no tratamento da SII predominante diarreia. Dado ao seu efeito no trânsito intestinal, o ADT devem ser usados com cautela em pacientes com constipação. VEJA DETALHES ACIMA!
O antibiótico rifaximina está associado a uma melhora geral dos sintomas da SII e, em especial, na diminuição do inchaço abdominal e da diarreia (550 mg três vezes ao dia durante 14 dias). No entanto, a melhora no inchaço abdominal em pacientes com SII sem constipação é modesta. Embora os antibióticos não sejam recomendados em todos os pacientes com SII, os pacientes com SII moderada a grave sem constipação, particularmente aqueles com inchaço abdominal, que falharam em responder a outros tratamentos (por exemplo, uma dieta pobre em FODMAPs, antiespasmódicos e TCAs), recomenda-se um tratamento teste por duas semanas com rifaximina.
O painel fez uma recomendação condicional para o tratamento inicial com rifaximina em indivíduos com SII-D e para o retratamento em pacientes com IBS-D que tiveram resposta inicial, mas desenvolveu sintomas recorrentes. A eficácia do tratamento com rifaximina na melhora da dor abdominal, urgência e qualidade de vida foi maior do que o placebo, mas seu efeito sobre a consistência das fezes e inchaço não. As taxas de resposta com retratamento de rifaximina e placebo foram inferiores. VEJA DETALHES ACIMA!
A pregabalina tem efeitos analgésicos e ansiolíticos conhecidos. A pregabalina tem efeitos benéficos nos sintomas gerais da SII, bem como na dor abdominal, diarreia e distensão abdominal relacionadas à SII. Para a maioria dos pacientes, 150 mg duas vezes ao dia é a dose ideal, podendo chegar a 300 mg duas vezes ao dia.
A colestiramina, sequestrador de ácidos biliares, pode ser usada em pacientes com diarreia persistente, apesar dos antidiarreicos, na dose inicial de 4 g três vezes por dia, com ajuste posterior da dose, se necessário. No entanto, seu uso é limitado pelos efeitos colaterais gastrointestinais associados, incluindo inchaço, flatulência, desconforto abdominal e constipação. A justificativa para o uso de sequestradores de ácidos biliares em pacientes com SII-D é que até 50% dos pacientes com diarreia funcional e SII-diarreia apresentam má absorção de ácido biliar. Os ácidos biliares causam diarreia, estimulando a secreção e a motilidade do cólon.
A atividade física aeróbica reduz a dor abdominal, ajuda a controlar o trânsito colônico, facilita a evacuação e alivia a ansiedade. Para pacientes com SII, são recomendadas atividades suaves, lentas e de baixa intensidade, como caminhada, ioga, ciclismo, natação e aeróbica. A OMS recomenda realizar exercícios aeróbicos de intensidade moderada (caminhar a passos rápidos) com duração mínima de 30 minutos por cinco dias na semana ou atividades aeróbicas mais intensas (corridas com respiração rápida), com duração de 20 minutos, três dias por semana e praticar atividades de fortalecimento muscular de intensidade moderada ou alta pelo menos duas vezes por semana. Combinações de atividade física com exercícios moderados e intensos podem ser realizadas para atingir as recomendações oficiais, que são caminhar rapidamente por 30 minutos duas vezes por semana e correr 20 minutos em outros dois dias. VEJA DETALHES ACIMA!
Dieta na SII-D. Os pacientes com diarreia que apresentam inchaço/distensão abdominal, dor abdominal e excesso de gases se beneficiam da exclusão de alimentos que aumentam a produção de gases e caso não melhorem recomenda-se a adoção de uma dieta com baixo teor de FODMAPs (oligo, di e monossacarídeos e polióis fermentáveis) que envolve a eliminação de um número maior de alimentos. VEJA MAIS! BAIXE AS RECOMENDAÇÕES DIETÉTICAS E COMPORTAMENTAIS!
Os conselhos dietéticos gerais (CDG) implica recomendações dietéticas com limitação de cafeína, álcool, alimentos condimentados, alimentos gordurosos e bebidas carbonatadas; comer pequenas refeições de frequência; comer devagar e em paz; e evitar gomas de mascar e adoçantes contendo polióis.
A dieta baixa em FODMAP melhora significativamente os sintomas gastrointestinais (dor abdominal, inchaço e diarreia) versus conselhos dietéticos gerais. Embora o grupo com os conselhos dietéticos gerais tenha mostrado uma redução significativa nos sintomas gastrointestinais após 6 semanas, mas a redução é maior no grupo de dieta baixa FODMAP. VEJA DETALHES ACIMA!
Bebidas alcoólicas. Avaliar a ingestão de álcool em relação aos sintomas (fezes amolecidas, dor abdominal, náuseas, indigestão e diarreia), considerar a redução da ingestão. Avaliar a ingestão de cafeína e, se relacionado aos sintomas (refluxo gastresofágico, dor abdominal e fezes amolecidas), considerar a redução da ingestão. Avaliar a ingestão de alimentos picantes e pimenta e, se relacionado aos sintomas (refluxo gastresofágico, dor abdominal e queimação oral), considerar a eliminação.
Alimentos gordurosos. Se os sintomas, em particular dor abdominal e distensão/inchaço abdominal, estiver relacionado a sintomas durante ou após comer alimentos gordurosos, avaliar a diminuição da ingestão de gordura.
Leite e os produtos lácteos. Use uma dieta baixa em lactose apenas em pacientes com diagnóstico por exames complementares de intolerância à lactose.
Glúten. Neste momento, nenhuma recomendação pode ser feita para tratar os sintomas da SII com uma dieta sem glúten em pacientes não celíacos.
A suplementação de psyllium é recomendada na SII com constipação e com diarreia. Em casos de constipação, amolece as fezes duras, enquanto em casos de diarreia, solidifica as fezes moles e estabiliza a frequência e a forma dos movimentos intestinais em indivíduos com SII. A dose recomendada é de pelo menos 10 g duas vezes ao dia (20 g ao dia) junto com um mínimo de 250 ml de água. Geralmente os benefícios começam em 1 a 2 semanas e se mantêm a longo prazo. É uma forma de tratamento econômica, segura e bem aceita pelo paciente. A dose do psyllium deve ser titulada lentamente com base na resposta ao tratamento até 20–30 g/dia. VEJA DETALHES DE COMO CONSUMIR O PSYLLIUM (VEJA NESTA PÁGINA)
A vitamina D é extremamente importante para cada indivíduo. Devido à síntese limitada na pele e à ingestão alimentar muito baixa, a suplementação de vitamina D é recomendada para todos. A dosagem preventiva recomendada varia de 800–2.000 UI por dia. É particularmente importante prestar atenção à ocorrência de deficiências de vitamina D entre pacientes com SII e recomendar a suplementação de vitamina D neste grupo, pois a inclusão de suplementos pode ter efeitos positivos no curso da doença. A suplementação pode aliviar os sintomas da SII e melhorar a qualidade de vida.
Os probióticos, Bifidobactérias (B. infantis, B. animalis. B. lactis e B. bifidum na dose de 109 ufc), são condicionalmente recomendados para sintomas gerais, distensão/inchaço abdominal e flatulência na SII com a maioria dos pacientes apresentando melhora após 4-8 semanas de uso. VEJA DETALHES ACIMA!
Loperamida. Em pacientes com SII-diarreia, recomenda-se a loperamida, comprimido de 2 mg, 45 minutos antes de uma refeição, em doses programadas regularmente (dose diária máxima de 16 mg/dia). Os agentes antidiarreicos inibem o peristaltismo, prolongam o tempo de trânsito intestinal e reduzem o volume fecal. No entanto, a loperamida deve ser usada em doses limitadas, conforme necessário, em pacientes com alternância entre diarreia e constipação.
Os antiespasmódicos devem ser administrados conforme a necessidade e/ou em resposta a fatores desencadeantes e/ou exacerbadores sabidamente conhecidos. Os antiespasmódicos promovem alívio da dor abdominal a curto prazo nos pacientes com SII, mas sua eficácia a longo prazo não foi estabelecida.
Agentes antiespasmódicos anticolinérgicos / antimuscarínico e relaxante de músculo liso para o caso de cólica por fatores desencadeantes e/ou exacerbadores sabidamente conhecidos (escopolamina - 1 comprimido ou 20 a 40 gotas (10-20 mg), 3 a 5 vezes ao dia ou Tropinal® [dipirona 300mg + escopolamina 6,5mcg + hiosciamina 104mcg + homatropina 1.0mg] - 1 a 2 comprimidos, 3 vezes ao dia).
Agentes antiespasmódicos que agem diretamente no relaxamento do músculo liso intestinal.
- Brometo de Pinavério. Pacientes com SII-D recebendo pinavério 50 mg 3xs/dia experimentaram melhoras significativas na dor abdominal e da consistência das fezes nas semanas 2 e 4. A combinação de pinavério 100 mg mais simeticona 300 mg duas vezes por dia melhorou significativamente a intensidade da dor e inchaço abdominal.
- Maleato de Trimebutina. Em 4 pequenos estudos de trimebutina 100 ou 200 mg 3 xs/dia administrados por 2 semanas a 6 meses, a melhora da dor abdominal foi observada de forma inconsistente.
A ondansetrona (dose inicial de 4 mg uma a duas vezes ao dia) melhora significativamente em pacientes com SII-diarreia a consistência, a frequência e a urgência das fezes, mas não foi associado a uma melhora significativa dor abdominal. O efeito da ondansetrona na forma das fezes é rápido, sendo observado na primeira semana com uma melhora na consistência das fezes e redução no número de evacuações amolecidas diárias.
Antidepressivo tricíclico (ADT) no tratamento da síndrome do intestino irritável (SII). Para o tratamento da dor abdominal na SII, os ADTs devem ser iniciados com doses baixas (por exemplo, amitriptilina e nortriptilina na dose de 10 a 25 mg à noite antes de dormir) com ajustes posteriores com base na tolerância e resposta. Devido ao início tardio da ação dos antidepressivos, somente após 3-4 semanas a dose deve ser revista. Os efeitos benéficos dos ADTs nos sintomas da SII parecem ser independentes dos efeitos sobre a depressão. O antidepressivo tricíclico, por meio de sua propriedade anticolinérgica, reduz o tempo de trânsito intestinal, o que pode fornecer benefícios no tratamento da SII predominante diarreia. Dado ao seu efeito no trânsito intestinal, o ADT devem ser usados com cautela em pacientes com constipação. VEJA DETALHES ACIMA!
O antibiótico rifaximina está associado a uma melhora geral dos sintomas da SII e, em especial, na diminuição do inchaço abdominal e da diarreia (550 mg três vezes ao dia durante 14 dias). No entanto, a melhora no inchaço abdominal em pacientes com SII sem constipação é modesta. Embora os antibióticos não sejam recomendados em todos os pacientes com SII, os pacientes com SII moderada a grave sem constipação, particularmente aqueles com inchaço abdominal, que falharam em responder a outros tratamentos (por exemplo, uma dieta pobre em FODMAPs, antiespasmódicos e TCAs), recomenda-se um tratamento teste por duas semanas com rifaximina.
O painel fez uma recomendação condicional para o tratamento inicial com rifaximina em indivíduos com SII-D e para o retratamento em pacientes com IBS-D que tiveram resposta inicial, mas desenvolveu sintomas recorrentes. A eficácia do tratamento com rifaximina na melhora da dor abdominal, urgência e qualidade de vida foi maior do que o placebo, mas seu efeito sobre a consistência das fezes e inchaço não. As taxas de resposta com retratamento de rifaximina e placebo foram inferiores. VEJA DETALHES ACIMA!
A pregabalina tem efeitos analgésicos e ansiolíticos conhecidos. A pregabalina tem efeitos benéficos nos sintomas gerais da SII, bem como na dor abdominal, diarreia e distensão abdominal relacionadas à SII. Para a maioria dos pacientes, 150 mg duas vezes ao dia é a dose ideal, podendo chegar a 300 mg duas vezes ao dia.
A colestiramina, sequestrador de ácidos biliares, pode ser usada em pacientes com diarreia persistente, apesar dos antidiarreicos, na dose inicial de 4 g três vezes por dia, com ajuste posterior da dose, se necessário. No entanto, seu uso é limitado pelos efeitos colaterais gastrointestinais associados, incluindo inchaço, flatulência, desconforto abdominal e constipação. A justificativa para o uso de sequestradores de ácidos biliares em pacientes com SII-D é que até 50% dos pacientes com diarreia funcional e SII-diarreia apresentam má absorção de ácido biliar. Os ácidos biliares causam diarreia, estimulando a secreção e a motilidade do cólon.
Os probióticos não são recomendados rotineiramente nos pacientes com SII. Embora tenham sido associados a uma melhora nos sintomas, a magnitude do benefício e as espécies mais eficazes são incertas.
Os probióticos têm potencial em impactar positivamente na condução do tratamento, mas os benefícios no tratamento da SII não estão comprovados. É possível que algum benefício clinicamente importante possa ser alcançado em certos subgrupos de pacientes, particularmente naqueles em que a diarreia predomina. Como na doença inflamatória intestinal, a abordagem pode estar na correção da microbiota alterada, em vez de usar uma preparação probiótica genérica em todos os pacientes.
Existem muitos produtos probióticos disponíveis em diferentes doses e cepas bacterianas variáveis. Indivíduos com SII que optam por experimentar probióticos devem estar cientes de que alguns produtos contêm outros ingredientes que podem aumentar os sintomas da SII (por exemplo, fibra dietética: aveia; FODMAPs: FOS, inulina, lactose, frutose, sorbitol e xilitol). Se um indivíduo usa um probiótico durante 4 semanas e apresenta melhora dos sintomas, ele pode continuar usando, mas os efeitos a longo prazo não são conhecidos.
Os probióticos têm potencial em impactar positivamente na condução do tratamento, mas os benefícios no tratamento da SII não estão comprovados. É possível que algum benefício clinicamente importante possa ser alcançado em certos subgrupos de pacientes, particularmente naqueles em que a diarreia predomina. Como na doença inflamatória intestinal, a abordagem pode estar na correção da microbiota alterada, em vez de usar uma preparação probiótica genérica em todos os pacientes.
Existem muitos produtos probióticos disponíveis em diferentes doses e cepas bacterianas variáveis. Indivíduos com SII que optam por experimentar probióticos devem estar cientes de que alguns produtos contêm outros ingredientes que podem aumentar os sintomas da SII (por exemplo, fibra dietética: aveia; FODMAPs: FOS, inulina, lactose, frutose, sorbitol e xilitol). Se um indivíduo usa um probiótico durante 4 semanas e apresenta melhora dos sintomas, ele pode continuar usando, mas os efeitos a longo prazo não são conhecidos.
Pequeno subconjunto de pacientes com síndrome do intestino irritável (SII) apresenta sintomas refratários. Pacientes com sintomas contínuos, apesar da terapia farmacológica adjunta, devem ser cuidadosamente reavaliados, prestando atenção específica aos tipos de sintomas, a intensidade dos sintomas, a resposta aos medicamentos e à presença de sinais e sintomas de alarme que devem levar a uma avaliação mais aprofundada.
Pacientes com sintomas incessantes associados a comprometimento psiquiátrico podem se beneficiar da modificação de comportamento em conjunto com antidepressivos.
O uso de agentes ansiolíticos em pacientes com SII deve limitar-se à redução em curto prazo (menos de duas semanas) da ansiedade situacional aguda que pode estar contribuindo para os sintomas. Os efeitos colaterais dos ansiolíticos incluem o risco de dependência, a suspensão pode levar o efeito de rebote e interações medicamentosas. Além disso, os benzodiazepínicos podem diminuir os limiares da dor.
Pacientes com sintomas incessantes associados a comprometimento psiquiátrico podem se beneficiar da modificação de comportamento em conjunto com antidepressivos.
O uso de agentes ansiolíticos em pacientes com SII deve limitar-se à redução em curto prazo (menos de duas semanas) da ansiedade situacional aguda que pode estar contribuindo para os sintomas. Os efeitos colaterais dos ansiolíticos incluem o risco de dependência, a suspensão pode levar o efeito de rebote e interações medicamentosas. Além disso, os benzodiazepínicos podem diminuir os limiares da dor.
A ligação definitiva entre a infecção por H. pylori e a SII permanece incerta. Em vez disso, os pacientes com dispepsia funcional (DF) relacionada ao H. pylori são considerados um grupo separado de pacientes com SII. A DF é um distúrbio da interação intestino-cérebro e caracterizado por sintomas gastrointestinais superiores, incluindo síndrome de dor epigástrica e síndrome de desconforto pós-prandial relacionada à alimentação. Estas parecem diferenciar a DF da SII, embora as duas condições frequentemente coexistam.
Sugere-se que o H. pylori pode ter um efeito positivo no desenvolvimento da SII. Uma disbiose da microbiota GI, infecção por H. pylori e metabólitos da microbiota GI parecem influenciar a ocorrência de DF. Se o H. pylori for detectado, recomenda-se a terapia de erradicação de acordo com os critérios de Maastricht e foram relatadas algumas evidências de benefício da dispepsia sintomática. Embora o envolvimento do H. pylori na DF e na SII esteja sendo discutido, estudos relataram que a erradicação melhora a dispepsia.
Quando a infecção por H. pylori está presente além da intolerância/má absorção alimentar, a erradicação é obrigatória. A possível coexistência de DF e SII, o suposto efeito do H. pylori no desenvolvimento de SII, a aparente necessidade de procurar H. pylori na DF e os alimentos que desencadeiam a DF podem justificar a procura de infecção por H. pylori além de intolerância/má absorção alimentar na SII.
Sugere-se que o H. pylori pode ter um efeito positivo no desenvolvimento da SII. Uma disbiose da microbiota GI, infecção por H. pylori e metabólitos da microbiota GI parecem influenciar a ocorrência de DF. Se o H. pylori for detectado, recomenda-se a terapia de erradicação de acordo com os critérios de Maastricht e foram relatadas algumas evidências de benefício da dispepsia sintomática. Embora o envolvimento do H. pylori na DF e na SII esteja sendo discutido, estudos relataram que a erradicação melhora a dispepsia.
Quando a infecção por H. pylori está presente além da intolerância/má absorção alimentar, a erradicação é obrigatória. A possível coexistência de DF e SII, o suposto efeito do H. pylori no desenvolvimento de SII, a aparente necessidade de procurar H. pylori na DF e os alimentos que desencadeiam a DF podem justificar a procura de infecção por H. pylori além de intolerância/má absorção alimentar na SII.
Isenção de responsabilidade
As informações contidas neste artigo são apenas para fins educacionais e não devem ser usadas para diagnóstico ou para orientar o tratamento sem o parecer de um profissional de saúde. Qualquer leitor que está preocupado com sua saúde deve entrar em contato com um médico para aconselhamento.
As informações contidas neste artigo são apenas para fins educacionais e não devem ser usadas para diagnóstico ou para orientar o tratamento sem o parecer de um profissional de saúde. Qualquer leitor que está preocupado com sua saúde deve entrar em contato com um médico para aconselhamento.